Anilina: propiedades, reacciones, producción y usos
La anilina, también conocida como aminobenceno, es una amina aromática con la fórmula química C6H5NH2. Es un líquido inflamable, de incoloro a ligeramente amarillo, con un olor dulce parecido a una amina, y se vuelve marrón al exponerse al aire y a la luz.
Su aislamiento se remonta a principios del siglo XIX y su estructura fue establecida de manera concluyente por A. W. Von Hofmann en 1843 mediante la reducción de nitrobenceno.
El método industrial inicial para sintetizar anilina se estableció ya en 1854. En los últimos 145 años, la anilina se ha convertido en uno de los 100 componentes esenciales en el campo de la química.
La anilina sirve como intermediario esencial en una amplia variedad de aplicaciones, como en isocianatos, agentes de procesamiento de caucho, tintes y pigmentos, productos químicos agrícolas y productos farmacéuticos.
Table of Contents
1. Propiedades físicas de la anilina
La anilina es parcialmente soluble en agua y miscible con la mayoría de los disolventes orgánicos (por ejemplo, etanol, acetona y benceno).
Las propiedades físicas importantes de la anilina son las siguientes:
- Masa molecular (Mr) = 93,13 g/mol
- Punto de ebullición (101,3 kPa) = 184,4 °C
- Punto de solidificación = -6,2 °C
- Punto de inflamación (DIN 51758) = 76 °C
- Temperatura de ignición (DIN 51758) = 540 °C
- Umbral de olor = 0,5 ml/m3
- Densidad del líquido (20 °C) = 1,022 g/cm3
- Solubilidad (20 °C) Anilina en agua =3,6 %
- Valor de pH (3,6 g de anilina por litro, 20 °C) = 8,8
2. Reacciones químicas de la anilina
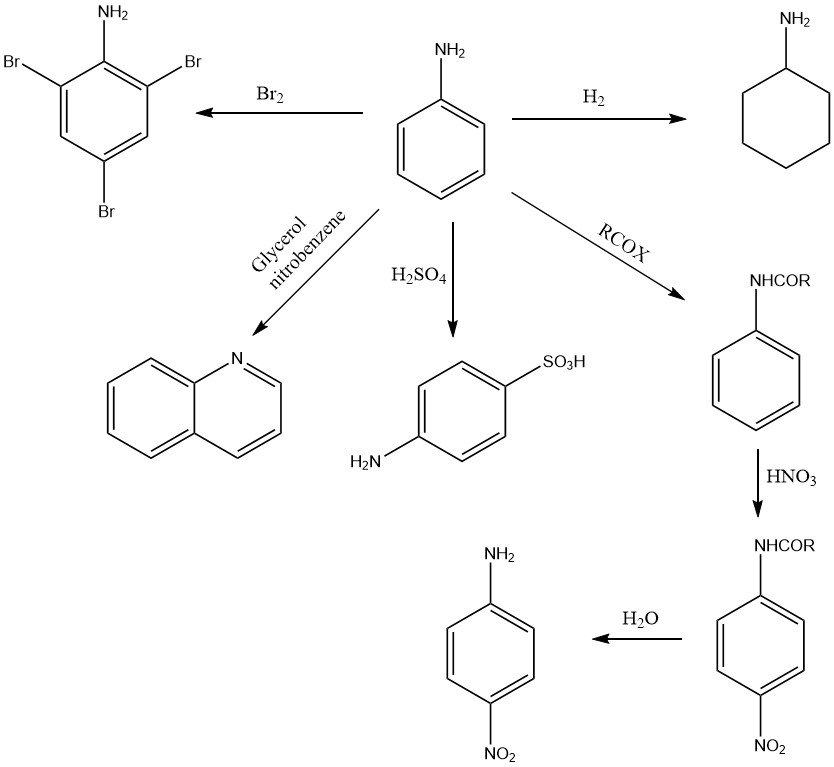
La química de la anilina está determinada por el grupo amino primario (Figura 1) y por el núcleo de benceno activado (Figura 2).
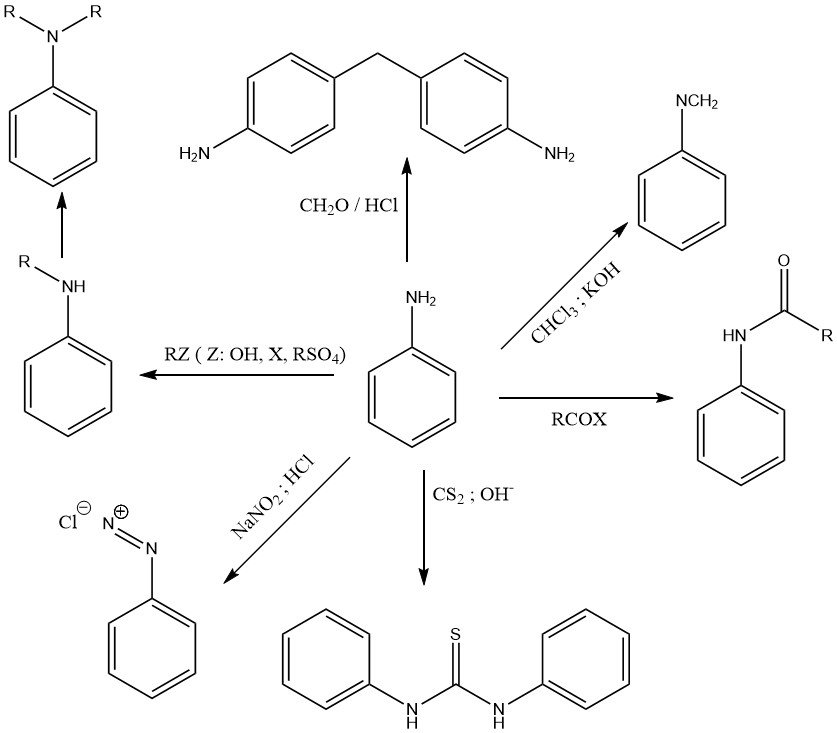
El par de electrones solitario del nitrógeno del grupo amino está parcialmente deslocalizado al sistema de anillos aromáticos. Por lo tanto, la anilina es sólo una base débil (pKa = 4,60) en comparación con aminas alifáticas como la ciclohexilamina (pKa = 10,64).
Sin embargo, la anilina forma sales estables y solubles en agua con ácidos minerales fuertes (p. ej., ácido clorhídrico o sulfúrico). La formación de sulfato de anilina se puede utilizar para proteger el grupo amino de la anilina contra la oxidación durante los pasos de síntesis posteriores.
Varios agentes alquilantes (como alcoholes, haluros de alquilo, sulfatos de alquilo y olefinas) alquilan el grupo amino para formar N-alquilo y N,N-dialquilanilina en reacciones catalizadas por ácido de Lewis a temperatura y presión elevadas.
La reacción de la anilina con cloroformo en una solución de potasa cáustica produce fenilisocianuro.
La N,N-difeniltiourea es el producto de la reacción de anilina y disulfuro de carbono en una solución de alcohol alcalino.
Una reacción característica de las aminas aromáticas primarias como la anilina es la formación de sales de diazonio con ácido nitroso.
La anilina sufre reacciones de condensación con alquilaldehídos. La reacción más importante es la formación de 4,4′-metilendianilina (MDA) por condensación de anilina con formaldehído en presencia de ácido clorhídrico.
La anilina reacciona con ácidos orgánicos y derivados ácidos para formar amidas.
La anilina sufre una variedad de reacciones de oxidación, dependiendo del agente oxidante y las condiciones. Se pueden formar productos mononucleares como la p-benzoquinona (MnO2, H2SO4), compuestos bimoleculares como el azobenceno (aire) o sustancias poliméricas como el negro de anilina (Cu o V, Na2Cr2O7 o NaClO3) (ver Fig. 2).
El anillo aromático de anilina se hidrogena catalíticamente para dar ciclohexilamina y/o diciclohexilamina a temperatura y presión elevadas, dependiendo de las condiciones y el tipo de catalizador.
La presencia del grupo amino activa las posiciones orto y para del anillo aromático y, como resultado, la anilina reacciona fácilmente con sustancias electrófilas. Por ejemplo, la bromación de anilina con bromo produce 1,3,5-tribromoanilina en condiciones suaves.
La reacción con ácido sulfúrico a alta temperatura forma casi exclusivamente ácido 4-aminobencenosulfónico (ácido 4-sulfanílico).
La nitración de la anilina (después de proteger el grupo amino contra la oxidación mediante la formación de acetanilida) forma el compuesto 4-nitro.
A partir de la anilina se pueden obtener numerosos compuestos N-heterocíclicos. Por ejemplo, la quinolina se produce en la síntesis de Skraup mediante la condensación de anilina con glicerol o acrilaldehído (acroleína) en nitrobenceno.
3. Producción de anilina
La mayoría de los procesos de síntesis de anilina utilizados en aplicaciones comerciales se inician a partir del benceno.
Aunque ha habido intentos de aminar directamente el benceno, el proceso requiere altas temperaturas y presiones, así como un exceso de amoníaco, lo que ha dificultado el desarrollo de un método económicamente viable.
En cambio, DuPont y Mitsui Toatsu han investigado la aminación oxidativa del benceno, que genera agua como subproducto.
Actualmente, todos los fabricantes mundiales, a excepción de Mitsui Petrochemicals Ind. (Japón), utilizan nitrobenceno como materia prima para la producción de anilina.
Mitsui Petrochemicals Ind. utiliza además fenol como material de partida, mientras que Aristech Chemical Corp. (Estados Unidos) utiliza exclusivamente la ruta del fenol.
3.1. Hidrogenación catalítica de nitrobenceno
La hidrogenación catalítica altamente exotérmica (DH = -544 kJ/mol a 200 °C) del nitrobenceno se realiza tanto en fase de vapor como en fase líquida en procesos utilizados comercialmente.
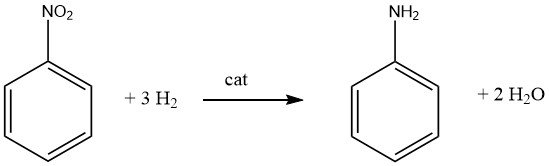
El intercambio de calor eficiente y la utilización del calor de reacción es un aspecto crucial para cualquier proceso que emplee nitrobenceno como materia prima.
3.1.1. Hidrogenación catalítica en fase de vapor
El nitrobenceno se puede convertir en anilina con altos rendimientos mediante procesos de hidrogenación.
Normalmente se emplean técnicas de lecho fijo o de lecho fluidizado en fase de vapor, siendo los catalizadores más eficaces el cobre o el paladio soportados sobre carbón activado o un sustrato oxídico, en combinación con modificadores o promotores como Pb, V, P o Cr para mejorar la actividad y la selectividad.
En el proceso Lonza, operado por First Chemical Corp., se pasa una mezcla homogeneizada de hidrógeno y nitrobenceno sobre un catalizador de lecho fijo de cobre sobre piedra pómez.
El nitrobenceno se pulveriza en una corriente de gas circulante calentada de hidrógeno fresco en una posición fija para asegurar la homogeneización.
La relación molar entre la alimentación de nitrobenceno y el hidrógeno total es de aproximadamente 1:100 en la entrada del reactor, y los productos de la reacción salen del reactor con una temperatura superior a 300°C. El calor generado por la hidrogenación se utiliza para la producción de vapor y para calentar la corriente de gas reciclado.
El exceso de hidrógeno, la anilina bruta y el agua se separan enfriando la salida del reactor en un condensador y la anilina se purifica mediante destilación.
Bayer utiliza reactores de lecho fijo convencionales que emplean un catalizador de paladio sobre un soporte de alúmina modificado mediante la adición de vanadio y plomo.
El proceso reivindica la hidrogenación adiabática de nitrobenceno sobre un catalizador de lecho fijo de 1,5 a 4 % en peso de paladio sobre coque con 0,1 a 2 % en peso de plomo como modificador.
La mezcla de nitrobenceno e hidrógeno vaporizados en una proporción molar de 1:120 a 1:200 se alimenta al reactor adiabático a una presión de 100 a 700 kPa y una temperatura de entrada de 250 a 350 °C.
El lecho del catalizador en el reactor tiene una altura de 0,1 a 1,0 m y los productos de la reacción salen del reactor sin enfriar a una temperatura máxima de 460 °C.
Después del enfriamiento se separan bajo presión la anilina bruta, las aguas residuales brutas y el hidrógeno reciclado. La anilina bruta se purifica mediante destilación.
BASF emplea un proceso de lecho fluidizado en fase de vapor, donde el nitrobenceno se evapora parcialmente mediante atomización con una corriente de gas caliente compuesta principalmente de hidrógeno.
La corriente de gas se hace circular en presencia de un catalizador fluidizado, se condensan los productos de reacción y se separa la anilina de los productos de reacción brutos. El cobre soportado sobre sílice con promotores de cromo, zinc y bario es un catalizador preferido.
La mezcla bifásica de nitrobenceno e hidrógeno se inyecta a través de boquillas a diferentes alturas en el lecho fluidizado y la hidrogenación se produce en presencia de un exceso de hidrógeno a 250 – 300 °C y 400 – 1000 kPa. El calor de la reacción se utiliza para la producción de vapor y el gas caliente del producto se enfría en un intercambiador de calor.
Después de la regeneración del catalizador, el material orgánico depositado en la superficie del catalizador se quema a una temperatura de 200 a 250 °C con aire, y el catalizador se activa nuevamente reduciendo el óxido de cobre a cobre con hidrógeno a una temperatura de 200 a 300 °C.
3.1.2. Hidrogenación catalítica en fase líquida
Los procesos de hidrogenación de anilina empleados por ICI y DuPont se llevan a cabo en fase líquida. Estos procesos normalmente se operan a temperaturas que oscilan entre 90 y 200 °C y presiones de 100 a 600 kPa.
La reacción en fase líquida se puede llevar a cabo usando reactores de lecho fluidizado o de suspensión. La conversión de nitrobenceno en anilina suele completarse después de un único paso por el reactor con rendimientos del 98 al 99%.
En la década de 1960, ICI desarrolló un proceso de hidrogenación continua que utilizaba anilina como disolvente, que comprendía más del 95 % en peso de la fase líquida.
El proceso opera cerca o en el punto de ebullición del solvente (generalmente a presiones inferiores a 100 kPa), permitiendo que la mezcla de reacción se evapore y disipe parte o todo el calor de la reacción.
Se elimina el agua junto con los vapores efluentes, mientras se devuelve suficiente anilina al reactor para mantener las condiciones de estado estable. El proceso utiliza níquel finamente dividido sobre kieselguhr como catalizador preferido.
DuPont, por otro lado, emplea un proceso de hidrogenación en fase líquida para el nitrobenceno utilizando un catalizador de platino-paladio sobre un soporte de carbono con hierro como modificador.
El modificador proporciona una buena vida útil del catalizador, alta actividad y protección contra la hidrogenación del anillo aromático. El proceso emplea un reactor de flujo pistón que logra rendimientos casi cuantitativos, con el producto que sale del reactor prácticamente libre de nitrobenceno.
La comparación de la hidrogenación catalítica en fase líquida y en fase de vapor del nitrobenceno no revela diferencias significativas en el rendimiento y la calidad del producto para ambos procesos.
El proceso en fase líquida, sin embargo, tiene un mayor rendimiento espacio-temporal y no requiere un circuito de gas reciclado, lo que resulta en menores requisitos de energía.
Por el contrario, el proceso en fase de vapor utiliza eficazmente el calor de la reacción, produciendo vapor sin la necesidad de separación del producto-catalizador y dando como resultado una vida útil más larga del catalizador.
3.2. Reducción de Nitrobenceno con Hierro y Sales de Hierro
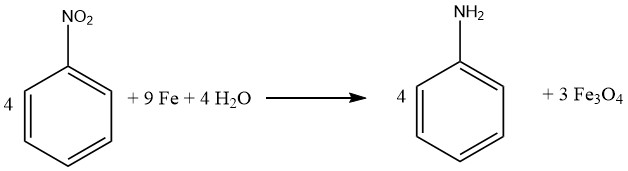
El proceso Bechamp es un método histórico para reducir el nitrobenceno, que emplea hierro y cloruro de hierro (II). A pesar de tener más de un siglo de antigüedad, el proceso todavía se utiliza en dos plantas de anilina de Bayer para producir pigmentos coloreados de óxido de hierro como subproductos.
Para llevar a cabo el proceso de Bechamp, el nitrobenceno se reduce en un recipiente de reacción agitado con una solución de cloruro de hierro (II) y rellenos de hierro molido.
El reactor se llena con agua, incluida agua de anilina procedente de la destilación de anilina, así como con un 20% del hierro, la cantidad requerida de catalizador y aproximadamente un 5-10% de la alimentación total de nitrobenceno.
La mezcla de reacción se calienta a reflujo con agitación intensa y, una vez que ha comenzado la reducción, se añaden lentamente el nitrobenceno y el hierro restantes para evitar una acumulación excesiva de temperatura y presión.
La reacción se completa en aproximadamente 8-10 horas calentando el recipiente a 100°C durante dos horas más después de la adición de hierro/nitrobenceno. Después de la neutralización con cal, la mezcla de reacción se transfiere a un separador y se retira la fase orgánica que contiene anilina.
Luego, la anilina se recupera de la fase orgánica mediante extracción con agua y destilación. Cualquier anilina restante se recupera del material que queda en el separador antes de que la suspensión de polvo de óxido de hierro se procese en un pigmento coloreado de partículas finas.
El color del subproducto de óxido de hierro se puede manipular alterando el medio de reacción con aditivos, utilizando diferentes tipos de hierro y controlando las condiciones de calcinación.
3.3. Aminación de fenol

Halcon desarrolló una ruta comercial de fenol en la que el fenol se somete a aminación en fase de vapor utilizando amoníaco junto con un catalizador de sílice-alúmina.
Debido a la naturaleza exotérmica y reversible de la reacción (ΔH = -8,4 kJ/mol), solo se pueden lograr altas tasas de conversión utilizando un exceso de amoníaco (relación molar de 20:1) y bajas temperaturas de reacción para reducir la disociación del amoníaco.
La difenilamina, la trifenilamina y el carbazol son impurezas que se producen como subproductos. El uso de exceso de amoniaco también inhibe la formación de estas impurezas. El rendimiento basado en fenol y amoníaco es ≥ 96% y 80%, respectivamente.
El proceso incluye la vaporización del fenol y del amoníaco fresco y reciclado por separado para evitar pérdidas de rendimiento. Luego se combinan en el reactor de aminación que contiene el catalizador de sílice-alúmina.
Después de la reacción, el gas se enfría y se condensa parcialmente, y el exceso de amoníaco se recupera en una columna de separación, se comprime y se recicla.
El producto de la condensación pasa a través de una columna de secado para eliminar el agua y luego a través de una columna de acabado al vacío (menos de 80 kPa) para separar la anilina del fenol residual y las impurezas. El fenol que contiene algo de anilina (mezcla azeotrópica) se recicla.
En comparación con la ruta del nitrobenceno que comienza a partir del benceno, la ruta del fenol implica cuatro pasos (cumeno a fenol a través del hidroperóxido de cumeno intermedio), mientras que la ruta del nitrobenceno implica solo dos pasos.
La ruta del nitrobenceno tiene una ventaja general en cuanto a rendimiento y menores requisitos de energía total, mientras que la ruta del fenol tiene una ventaja en una vida útil prolongada del catalizador y la calidad del producto.
Se prefiere la ruta del fenol si los productores de fenol disponen de fenol de bajo coste.
4. Usos de la anilina
La anilina se utiliza en más de 300 productos finales diferentes, siendo el más importante el componente básico de poliuretano isocianato de 4,4-metilen-di-parafenileno (MDI).
4.1. Isocianato de metileno difenileno (MDI)
El MDI es un isocianato crucial que se combina con alcoholes, como polioles y polieteroles, para formar poliuretanos (PU). Los sistemas de PU basados en MDI se emplean ampliamente en las industrias de la construcción, muebles, automoción y aislamiento.
Se prevé que estas aplicaciones, así como nuevos campos de aplicación, impulsen un fuerte crecimiento de MDI-PU, particularmente en los mercados emergentes.
Un proceso comercial típico de MDI implica la preparación de una mezcla de metilenfenilaminas poliméricas condensando anilina con formaldehído en presencia de HCl.
La reacción da como resultado la formación intermedia de clorhidratos de amina, que se neutralizan con sosa cáustica. La reacción suele tener lugar a presión subatmosférica y temperaturas entre 70 y 105°C, con un exceso de anilina. El rendimiento es aproximadamente del 96%.
A continuación, el producto de poliamina se hace reaccionar con fosgeno en un disolvente para producir una mezcla bruta de isocianatos. La temperatura de reacción es de aproximadamente 120°C y la presión es de 345 kPa, con un rendimiento de aproximadamente el 97%.
El clorobenceno se elimina mediante destilación y el crudo se separa mediante destilación al vacío en MDI puro y MDI polimérico, con la producción de cloruro de hidrógeno como subproducto de la reacción.
4.2 Productos químicos para el procesamiento del caucho
En la primera década de este siglo, se utilizó anilina pura como acelerador de vulcanización. El llamado a una mayor efectividad y un manejo más seguro llevó al desarrollo de aceleradores de mercaptotiazol y amida sulfénica a base de anilina, que actualmente representan aproximadamente el 80% de todos los aceleradores de vulcanización utilizados en todo el mundo.
La mayor importancia de la anilina dentro del sector de productos químicos para el procesamiento del caucho reside en los antidegradantes como las parafenilendiaminas (PPD), las quinolinas y la difenilamina.
La anilina es la materia prima de alrededor del 70% de todos los antidegradantes consumidos en todo el mundo. Se espera que la demanda futura de anilina en la industria del caucho crezca entre un 2% y un 3% anual, en consonancia con el crecimiento mundial de la demanda de caucho sintético y natural.
4.3 Tintes y pigmentos
La anilina sirve como materia prima para productos intermedios para tintes y pigmentos, que constituyen más del 50% de todas las formulaciones conocidas. Sin embargo, la mayoría de estas formulaciones son de menor importancia. Las clases más grandes son los compuestos mono, di y triazo.
La producción de tintes y pigmentos se ha desplazado hacia países asiáticos, como China e India. Sin embargo, algunas plantas de tintes y pigmentos a escala mundial en Europa y el TLCAN (Estados Unidos, Canadá, México) todavía utilizan anilina, por ejemplo, para la producción de índigo.
Desde la realización industrial de la síntesis química del índigo por parte de BASF a finales del siglo XIX, el índigo se ha convertido en el tinte más importante basado en anilina.
Se espera que el crecimiento mundial de esta aplicación siga siendo bajo, a una tasa del 1 al 2% anual.
4.4 Productos químicos agrícolas
Más de 40 sustancias activas para pesticidas (herbicidas, fungicidas e insecticidas) utilizan anilina como materia prima. Los más importantes son los herbicidas de amida y urea. Las empresas ubicadas en el TLCAN representan más del 50% del consumo mundial de anilina para productos químicos agrícolas.
Las sustancias activas a base de anilina se encuentran principalmente en las últimas etapas de su ciclo de vida y están a punto de ser reemplazadas. Se prevé que el consumo mundial disminuirá entre un 1% y un 2% al año.
4.5 Productos farmacéuticos
La anilina es una fuente estable, aunque menor, para la preparación de analgésicos, antipiréticos, antialérgicos y vitaminas. Aunque se espera que la producción de anilina aumente en los próximos cinco años para productos farmacéuticos, habrá una disminución correspondiente en su uso para la producción de vitaminas debido a la creciente popularidad de la tecnología de fermentación.
4.6 Ciclohexilamina/Diciclohexilamina
Durante la década de 1990, la anilina se convirtió en la materia prima preferida para la producción de ciclohexilamina y diciclohexilamina. Estas aminas se utilizan principalmente como intermediarios para aceleradores de vulcanización de sulfenamida. La ciclohexilamina también se utiliza en grandes cantidades como inhibidor de la corrosión y como materia prima para ciclamatos.
Se prevé que el uso de estas aminas en aceleradores y tratamiento de agua aumentará aproximadamente entre un 3% y un 4% anual, mientras que la demanda de ciclohexilamina para la producción de ciclamatos ha fluctuado considerablemente y es difícil de pronosticar. Si la FDA levanta la prohibición de los ciclamatos como edulcorantes artificiales en los Estados Unidos, se puede esperar un aumento de la demanda.
4.7 Varios
Entre otros usos (como la producción de alquilanilina, abrillantadores ópticos, ácidos sulfónicos, etc.), cabe mencionar el consumo de anilina para la síntesis de fibras de aramida.
Las aramidas son versátiles y pueden usarse como sustitutos del acero, con propiedades de refuerzo equivalentes con un peso significativamente menor. Las aramidas tienen tasas de crecimiento saludables debido a su aplicación en diversas industrias, como la sustitución del amianto en las pastillas de freno.
Referencia
- Aniline; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_303.pub2
