Anilin: Eigenschaften, Reaktionen, Herstellung und Verwendung
Anilin ist das Hauptmolekül innerhalb der Gruppe der aromatischen Amine. Es besitzt einen süßen, aminartigen Geruch und erscheint als farblose ölige Flüssigkeit, die bei Einwirkung von Luft und Licht eine Bräunung erfährt.
Seine Isolierung geht auf das frühe 19. Jahrhundert zurück und seine Struktur wurde 1843 von A. W. von Hofmann durch die Reduktion von Nitrobenzol endgültig aufgeklärt.
Die erste industrielle Methode zur Synthese von Anilin wurde bereits 1854 etabliert. In den letzten 145 Jahren hat sich Anilin zu einem der 100 wichtigsten Grundbausteine der Chemie entwickelt.
Anilin dient als wesentliches Zwischenprodukt in einer Vielzahl von Anwendungen, beispielsweise in Isocyanaten, Gummiverarbeitungsmitteln, Farbstoffen und Pigmenten, Agrarchemikalien und Pharmazeutika.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Anilin
Anilin ist teilweise wasserlöslich und mit den meisten organischen Lösungsmitteln (z. B. Ethanol, Aceton und Benzol) mischbar.
Wichtige physikalische Eigenschaften von Anilin sind wie folgt:
- Molekularmasse (Mr) = 93,13 g/mol
- Siedepunkt (101,3 kPa) = 184,4 °C
- Erstarrungspunkt = -6,2 °C
- Flammpunkt (DIN 51758) = 76 °C
- Zündtemperatur (DIN 51758) = 540 °C
- Geruchsschwelle = 0,5 ml/m3
- Dichte Flüssigkeit (20 °C) = 1,022 g/cm3
- Löslichkeit (20 °C) Anilin in Wasser =3,6 %
- pH-Wert (3,6 g Anilin pro Liter, 20 °C) = 8,8
2. Chemische Reaktionen von Anilin
Die Chemie von Anilin wird durch die primäre Aminogruppe (Abbildung 1) und den aktivierten Benzolkern (Abbildung 2) bestimmt.
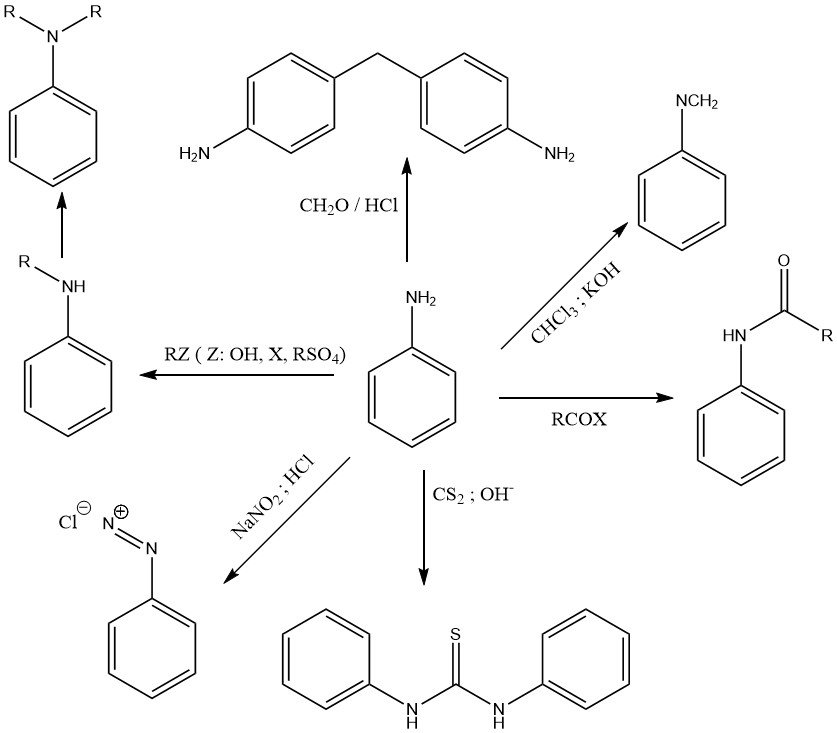
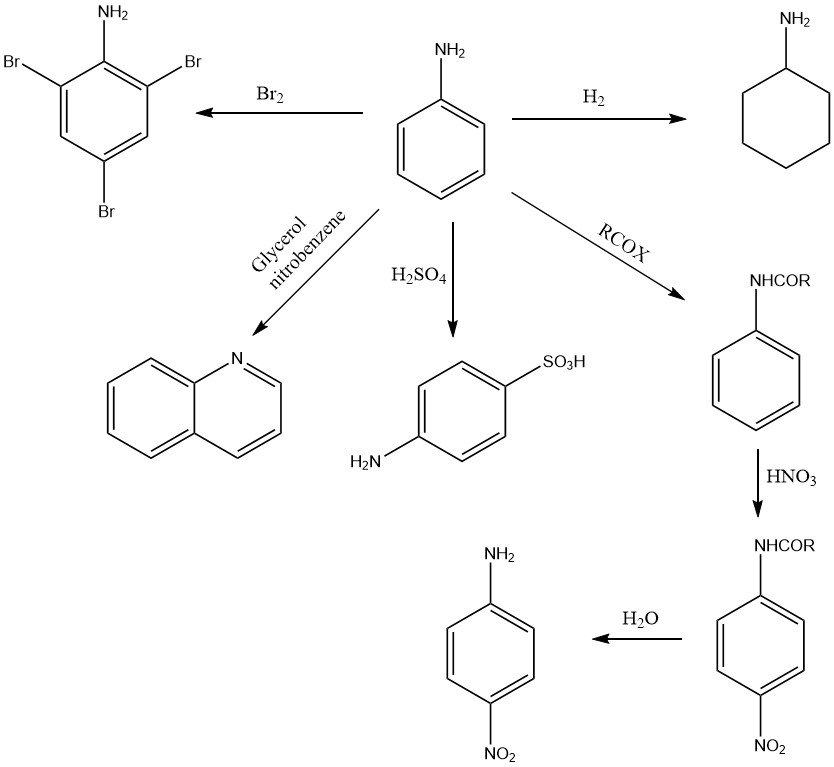
Das freie Elektronenpaar am Stickstoff der Aminogruppe ist teilweise zum aromatischen Ringsystem delokalisiert. Daher ist Anilin im Vergleich zu aliphatischen Aminen wie Cyclohexylamin (pKa = 10,64) nur eine schwache Base (pKa = 4,60).
Dennoch bildet Anilin mit starken Mineralsäuren (z. B. Salz- oder Schwefelsäure) stabile, wasserlösliche Salze. Die Bildung von Anilinsulfat kann genutzt werden, um die Aminogruppe des Anilins bei nachfolgenden Syntheseschritten vor Oxidation zu schützen.
Verschiedene Alkylierungsmittel (wie Alkohole, Alkylhalogenide, Alkylsulfate und Olefine) alkylieren die Aminogruppe unter Bildung von N-Alkyl und N,N-Dialkylanilin in Lewis-Säure-katalysierten Reaktionen bei erhöhter Temperatur und erhöhtem Druck.
Bei der Reaktion von Anilin mit Chloroform in einer Kalilauge entsteht Phenylisocyanid.
N,N-Diphenylthioharnstoff ist das Produkt der Reaktion von Anilin und Schwefelkohlenstoff in einer alkalischen Alkohollösung.
Eine charakteristische Reaktion primärer aromatischer Amine wie Anilin ist die Bildung von Diazoniumsalzen mit salpetriger Säure.
Anilin geht Kondensationsreaktionen mit Alkylaldehyden ein. Die wichtigste Reaktion ist die Bildung von 4,4′-Methylendianilin (MDA) durch Kondensation von Anilin mit Formaldehyd in Gegenwart von Salzsäure.
Anilin reagiert mit organischen Säuren und Säurederivaten unter Bildung von Amiden.
Anilin unterliegt je nach Oxidationsmittel und Bedingungen unterschiedlichen Oxidationsreaktionen. Es können einkernige Produkte wie p-Benzochinon (MnO2, H2SO4), bimolekulare Verbindungen wie Azobenzol (Luft) oder polymere Stoffe wie Anilinschwarz (Cu oder V, Na2Cr2O7 oder NaClO3) entstehen (siehe Abb. 2).
Der aromatische Anilinring wird je nach Bedingungen und Katalysatortyp bei erhöhter Temperatur und erhöhtem Druck katalytisch zu Cyclohexylamin und/oder Dicyclohexylamin hydriert.
Das Vorhandensein der Aminogruppe aktiviert die ortho- und para-Position des aromatischen Rings und als Folge davon reagiert Anilin leicht mit elektrophilen Substanzen. Beispielsweise ergibt die Bromierung von Anilin mit Brom unter milden Bedingungen 1,3,5-Tribromanilin.
Bei der Reaktion mit Schwefelsäure entsteht bei hoher Temperatur fast ausschließlich 4-Aminobenzolsulfonsäure (4-Sulfanilsäure).
Durch Nitrierung von Anilin (nach dem Schutz der Aminogruppe vor Oxidation durch die Bildung von Acetanilid) entsteht die 4-Nitroverbindung.
Aus Anilin lassen sich zahlreiche N-heterocyclische Verbindungen gewinnen. Beispielsweise wird Chinolin in der Skraup-Synthese durch Kondensation von Anilin mit Glycerin oder Acrylaldehyd (Acrolein) in Nitrobenzol hergestellt.
3. Herstellung von Anilin
Die Mehrzahl der in kommerziellen Anwendungen eingesetzten Anilinsyntheseverfahren geht von Benzol aus.
Obwohl es Versuche gab, Benzol direkt zu aminieren, erfordert das Verfahren hohe Temperaturen und Drücke sowie einen Überschuss an Ammoniak, was die Entwicklung einer wirtschaftlich sinnvollen Methode behindert hat.
Stattdessen haben DuPont und Mitsui Toatsu die oxidative Aminierung von Benzol untersucht, bei der Wasser als Nebenprodukt entsteht.
Derzeit nutzen alle globalen Hersteller, mit Ausnahme von Mitsui Petrochemicals Ind. (Japan), Nitrobenzol als Rohstoff für die Anilinproduktion.
Mitsui Petrochemicals Ind. verwendet zusätzlich Phenol als Ausgangsmaterial, während Aristech Chemical Corp. (USA) ausschließlich die Phenolroute nutzt.
3.1. Katalytische Hydrierung von Nitrobenzol
Die stark exotherme katalytische Hydrierung (ΔH = -544 kJ/mol bei 200 °C) von Nitrobenzol wird in kommerziell genutzten Verfahren sowohl in der Dampf- als auch in der Flüssigphase durchgeführt.
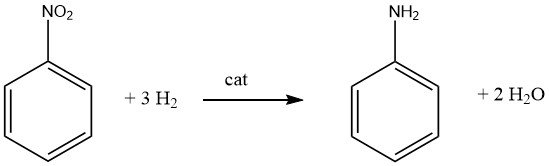
Ein effizienter Wärmeaustausch und die Nutzung der Reaktionswärme sind ein entscheidender Aspekt für jeden Prozess, der Nitrobenzol als Rohstoff verwendet.
3.1.1. Katalytische Dampfphasenhydrierung
Nitrobenzol kann durch Hydrierungsverfahren mit hohen Ausbeuten in Anilin umgewandelt werden.
Typischerweise werden Festbett- oder Wirbelschicht-Dampfphasentechniken eingesetzt, wobei die wirksamsten Katalysatoren Kupfer oder Palladium auf Aktivkohle oder einem oxidischen Substrat in Kombination mit Modifikatoren oder Promotoren wie Pb, V, P oder Cr sind Verbesserung der Aktivität und Selektivität.
Beim Lonza-Verfahren, das von First Chemical Corp. betrieben wird, wird eine homogenisierte Mischung aus Wasserstoff und Nitrobenzol über einen Festbettkatalysator aus Kupfer auf Bimsstein geleitet.
Nitrobenzol wird an einer festen Position in einen erhitzten zirkulierenden Gasstrom aus frischem Wasserstoff gesprüht, um eine Homogenisierung sicherzustellen.
Das Molverhältnis von Nitrobenzoleinsatz zu Gesamtwasserstoff beträgt am Reaktoreingang etwa 1:100 und die Reaktionsprodukte verlassen den Reaktor mit einer Temperatur über 300 °C. Die bei der Hydrierung entstehende Wärme wird zur Dampferzeugung und zur Erwärmung des Kreisgasstroms genutzt.
Überschüssiger Wasserstoff, Rohanilin und Wasser werden durch Kühlung des Reaktorauslasses in einem Kondensator abgetrennt und Anilin durch Destillation gereinigt.
Bayer nutzt herkömmliche Festbettreaktoren mit einem Palladiumkatalysator auf einem Aluminiumoxidträger, der durch die Zugabe von Vanadium und Blei modifiziert ist.
Das Verfahren sieht die adiabatische Hydrierung von Nitrobenzol an einem Festbettkatalysator aus 1,5 bis 4 Gew.-% Palladium auf Koks mit 0,1 bis 2 Gew.-% Blei als Modifikator vor.
Das Gemisch aus verdampftem Nitrobenzol und Wasserstoff im Molverhältnis 1:120 bis 1:200 wird dem adiabatischen Reaktor bei einem Druck von 100 – 700 kPa und einer Eintrittstemperatur von 250 – 350 °C zugeführt.
Das Katalysatorbett im Reaktor ist 0,1 bis 1,0 m hoch und die Reaktionsprodukte verlassen den Reaktor ohne Kühlung mit einer maximalen Temperatur von 460 °C.
Nach dem Abkühlen werden Rohanilin, Rohabwasser und recycelter Wasserstoff unter Druck getrennt. Das Rohanilin wird durch Destillation gereinigt.
BASF setzt ein Dampfphasen-Fließbettverfahren ein, bei dem Nitrobenzol durch Zerstäubung mit einem heißen Gasstrom, der hauptsächlich aus Wasserstoff besteht, teilweise verdampft.
Der Gasstrom wird in Gegenwart eines Wirbelkatalysators zirkuliert, die Reaktionsprodukte werden kondensiert und Anilin wird von den rohen Reaktionsprodukten abgetrennt. Kupfer auf Siliciumdioxid mit Chrom-, Zink- und Barium-Promotoren ist ein bevorzugter Katalysator.
Das zweiphasige Gemisch aus Nitrobenzol und Wasserstoff wird durch Düsen in verschiedenen Höhen in das Wirbelbett eingeblasen und die Hydrierung erfolgt in Gegenwart von überschüssigem Wasserstoff bei 250 – 300 °C und 400 – 1000 kPa. Die Reaktionswärme wird zur Dampferzeugung genutzt und das heiße Produktgas in einem Wärmetauscher abgekühlt.
Nach der Katalysatorregeneration wird das auf der Katalysatoroberfläche abgelagerte organische Material bei 200 bis 250 °C mit Luft abgebrannt und der Katalysator durch Reduktion des Kupferoxids zu Kupfer mit Wasserstoff bei 200 bis 300 °C wieder aktiviert.
3.1.2. Katalytische Flüssigphasenhydrierung
Die von ICI und DuPont eingesetzten Hydrierungsprozesse für Anilin werden in der flüssigen Phase durchgeführt. Diese Prozesse werden typischerweise bei Temperaturen im Bereich von 90 bis 200 °C und Drücken von 100 bis 600 kPa durchgeführt.
Die Flüssigphasenreaktion kann unter Verwendung von Aufschlämmungs- oder Wirbelschichtreaktoren durchgeführt werden. Die Umwandlung von Nitrobenzol zu Anilin ist typischerweise nach einem einzigen Reaktordurchgang mit Ausbeuten von 98 bis 99 % abgeschlossen.
In den 1960er Jahren entwickelte ICI ein kontinuierliches Hydrierungsverfahren, bei dem Anilin als Lösungsmittel verwendet wurde, das über 95 Gew.-% der flüssigen Phase ausmachte.
Der Prozess läuft in der Nähe oder am Siedepunkt des Lösungsmittels ab (normalerweise bei Drücken unter 100 kPa), wodurch die Reaktionsmischung verdampfen und einen Teil oder die gesamte Reaktionswärme abführen kann.
Wasser wird zusammen mit den Abgasdämpfen entfernt, während ausreichend Anilin in den Reaktor zurückgeführt wird, um stationäre Bedingungen aufrechtzuerhalten. Das Verfahren verwendet fein verteiltes Nickel auf Kieselgur als bevorzugten Katalysator.
DuPont hingegen nutzt ein Flüssigphasen-Hydrierungsverfahren für Nitrobenzol unter Verwendung eines Platin-Palladium-Katalysators auf einem Kohlenstoffträger mit Eisen als Modifikator.
Der Modifikator sorgt für eine gute Katalysatorlebensdauer, hohe Aktivität und Schutz gegen Hydrierung des aromatischen Rings. Das Verfahren verwendet einen Plug-Flow-Reaktor, der nahezu quantitative Ausbeuten erzielt, wobei das Produkt den Reaktor praktisch frei von Nitrobenzol verlässt.
Der Vergleich der katalytischen Flüssigphasen- und Dampfphasenhydrierung von Nitrobenzol zeigt bei beiden Verfahren keine signifikanten Unterschiede in Ausbeute und Produktqualität.
Der Flüssigphasenprozess hat jedoch eine höhere Raum-Zeit-Ausbeute und erfordert keinen Kreisgaskreislauf, was zu einem geringeren Energiebedarf führt.
Umgekehrt nutzt das Dampfphasenverfahren die Reaktionswärme effektiv aus, erzeugt Dampf, ohne dass eine Produkt-Katalysator-Trennung erforderlich ist, und führt zu einer längeren Lebensdauer des Katalysators.
3.2. Reduktion von Nitrobenzol mit Eisen und Eisensalzen
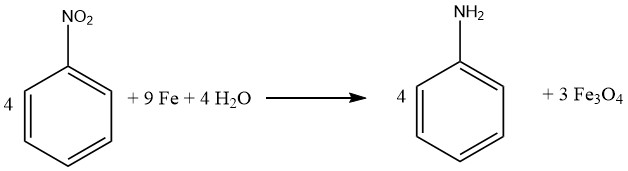
Das Bechamp-Verfahren ist eine historische Methode zur Reduktion von Nitrobenzol, bei der Eisen und Eisen(II)-chlorid zum Einsatz kommen. Obwohl das Verfahren bereits über ein Jahrhundert alt ist, wird es noch immer in zwei Bayer-Anilinanlagen eingesetzt, um als Nebenprodukte farbige Eisenoxidpigmente herzustellen.
Zur Durchführung des Bechamp-Verfahrens wird Nitrobenzol in einem Rührreaktionsgefäß mit einer Lösung aus Eisen(II)-chlorid und gemahlenen Eisenfüllungen reduziert.
Der Reaktor ist mit Wasser, einschließlich Anilinwasser aus der Anilindestillation, sowie 20 % des Eisens, der erforderlichen Katalysatormenge und etwa 5–10 % der gesamten Nitrobenzolbeschickung gefüllt.
Das Reaktionsgemisch wird unter intensivem Rühren zum Rückfluss erhitzt und nach Beginn der Reduktion werden das restliche Nitrobenzol und Eisen langsam zugegeben, um einen übermäßigen Temperatur- und Druckaufbau zu verhindern.
Die Reaktion ist in etwa 8 bis 10 Stunden abgeschlossen, indem das Gefäß nach der Eisen-/Nitrobenzolzugabe weitere zwei Stunden lang auf 100 °C erhitzt wird. Nach der Neutralisation mit Kalk wird das Reaktionsgemisch in einen Abscheider überführt und die anilinhaltige organische Phase abgezogen.
Anschließend wird das Anilin aus der organischen Phase durch Wasserstripping und Destillation zurückgewonnen. Eventuell verbleibendes Anilin wird aus dem im Separator verbleibenden Material zurückgewonnen, bevor die Eisenoxidpulveraufschlämmung zu einem feinteiligen, farbigen Pigment verarbeitet wird.
Die Farbe des Eisenoxid-Nebenprodukts kann manipuliert werden, indem man das Reaktionsmedium mit Zusatzstoffen verändert, verschiedene Eisenarten verwendet und die Kalzinierungsbedingungen kontrolliert.
3.3. Aminierung von Phenol

Halcon hat eine kommerzielle Phenolroute entwickelt, bei der Phenol in der Dampfphase unter Verwendung von Ammoniak zusammen mit einem Siliciumdioxid-Aluminiumoxid-Katalysator einer Aminierung unterzogen wird.
Aufgrund der exothermen und reversiblen Natur der Reaktion (ΔH = -8,4 kJ/mol) können hohe Umwandlungsraten nur mit überschüssigem Ammoniak (Molverhältnis 20:1) und niedrigen Reaktionstemperaturen zur Reduzierung der Ammoniakdissoziation erreicht werden.
Diphenylamin, Triphenylamin und Carbazol sind Verunreinigungen, die als Nebenprodukte entstehen. Auch die Verwendung von überschüssigem Ammoniak hemmt die Bildung dieser Verunreinigungen. Die Ausbeute bezogen auf Phenol und Ammoniak beträgt ≥ 96 % bzw. 80 %.
Der Prozess umfasst die getrennte Verdampfung von Phenol sowie frischem und recyceltem Ammoniak, um Ertragsverluste zu vermeiden. Anschließend werden sie im Aminierungsreaktor kombiniert, der den Siliciumdioxid-Aluminiumoxid-Katalysator enthält.
Nach der Reaktion wird das Gas abgekühlt und teilweise kondensiert, und das überschüssige Ammoniak wird in einer Trennkolonne zurückgewonnen, komprimiert und recycelt.
Das Kondensationsprodukt durchläuft eine Trocknungskolonne zur Entfernung von Wasser und anschließend eine Endkolonne im Vakuum (weniger als 80 kPa), um Anilin von restlichem Phenol und Verunreinigungen zu trennen. Das etwas Anilin enthaltende Phenol (azeotrope Mischung) wird recycelt.
Im Vergleich zur Nitrobenzol-Route, die von Benzol ausgeht, umfasst die Phenol-Route vier Schritte (Cumol zu Phenol über das Zwischenprodukt Cumolhydroperoxid), während die Nitrobenzol-Route nur zwei Schritte umfasst.
Die Nitrobenzol-Route bietet insgesamt einen Vorteil bei der Ausbeute und einen geringeren Gesamtenergiebedarf, wohingegen die Phenol-Route einen Vorteil hinsichtlich einer längeren Katalysatorlebensdauer und Produktqualität bietet.
Der Phenolweg wird bevorzugt, wenn kostengünstiges Phenol von Phenolherstellern erhältlich ist.
4. Verwendung von Anilin
Anilin wird in mehr als 300 verschiedenen Endprodukten eingesetzt, das wichtigste davon ist der Polyurethan-Baustein 4,4-Methylen-di-paraphenylenisocyanat (MDI).
4.1 Methylendiphenylenisocyanat (MDI)
MDI ist ein wichtiges Isocyanat, das mit Alkoholen wie Polyolen und Polyetherolen zu Polyurethanen (PU) kombiniert wird. Die MDI-basierten PU-Systeme werden häufig in der Bau-, Möbel-, Automobil- und Isolierindustrie eingesetzt.
Diese Anwendungen sowie neue Anwendungsfelder werden voraussichtlich zu einem starken Wachstum von MDI-PU führen, insbesondere in Schwellenländern.
Ein typisches kommerzielles MDI-Verfahren beinhaltet die Herstellung einer Mischung aus polymeren Methylenphenylaminen durch Kondensation von Anilin mit Formaldehyd in Gegenwart von HCl.
Die Reaktion führt zur Zwischenbildung von Aminhydrochloriden, die mit Natronlauge neutralisiert werden. Die Reaktion findet üblicherweise bei Unterdruck und Temperaturen zwischen 70 und 105 °C mit einem Überschuss an Anilin statt. Die Ausbeute beträgt ca. 96 %.
Das Polyaminprodukt wird dann mit Phosgen in einem Lösungsmittel umgesetzt, um eine Rohmischung aus Isocyanaten zu erzeugen. Die Reaktionstemperatur beträgt etwa 120 °C und der Druck 345 kPa, mit einer Ausbeute von etwa 97 %.
Chlorbenzol wird durch Destillation entfernt und das Rohöl wird durch Vakuumdestillation in reines MDI und polymeres MDI getrennt, wobei als Nebenprodukt der Reaktion Chlorwasserstoff entsteht.
4.2 Chemikalien zur Gummiverarbeitung
Im ersten Jahrzehnt dieses Jahrhunderts wurde reines Anilin als Vulkanisationsbeschleuniger eingesetzt. Der Ruf nach höherer Wirksamkeit und sicherer Handhabung führte zur Entwicklung von Mercaptothiazol- und Sulfenamid-Beschleunigern auf Anilinbasis, die derzeit etwa 80 % aller weltweit verwendeten Vulkanisationsbeschleuniger ausmachen.
Die größere Bedeutung von Anilin im Bereich der Kautschukverarbeitungschemikalien liegt in Antiabbaumitteln wie Paraphenylendiaminen (PPD), Chinolinen und Diphenylamin.
Anilin ist der Ausgangsstoff für etwa 70 % aller weltweit verbrauchten Antiabbaumittel. Die zukünftige Nachfrage nach Anilin in der Kautschukindustrie wird voraussichtlich um 2–3 % pro Jahr steigen, was im Einklang mit dem weltweiten Wachstum der Nachfrage nach synthetischem und natürlichem Kautschuk steht.
4.3 Farbstoffe und Pigmente
Anilin dient als Rohstoff für Zwischenprodukte für Farbstoffe und Pigmente, die mehr als 50 % aller bekannten Formulierungen ausmachen. Allerdings sind die meisten dieser Formulierungen von untergeordneter Bedeutung. Die größten Klassen sind die Mono-, Di- und Triazoverbindungen.
Die Produktion von Farbstoffen und Pigmenten hat sich in asiatische Länder wie China und Indien verlagert. Dennoch nutzen einige weltweit tätige Farbstoff- und Pigmentfabriken in Europa und NAFTA (USA, Kanada, Mexiko) immer noch Anilin, z. B. für die Produktion von Indigo.
Seit der industriellen Umsetzung der chemischen Indigosynthesen durch die BASF im späten 19. Jahrhundert hat sich Indigo zum wichtigsten Farbstoff auf Anilinbasis entwickelt.
Es wird erwartet, dass das weltweite Wachstum dieser Anwendung mit einer Rate von 1–2 % pro Jahr gering bleiben wird.
4.4 Agrarchemikalien
Mehr als 40 Wirkstoffe für Pestizide (Herbizide, Fungizide und Insektizide) nutzen Anilin als Rohstoff. Am wichtigsten sind Amid- und Harnstoffherbizide. Auf Unternehmen mit Sitz in der NAFTA-Region entfallen über 50 % des weltweiten Anilinverbrauchs für Agrarchemikalien.
Anilinbasierte Wirkstoffe befinden sich überwiegend in den späteren Stadien ihres Lebenszyklus und stehen kurz vor der Ablösung. Der weltweite Verbrauch wird voraussichtlich um 1–2 % pro Jahr zurückgehen.
4.5 Arzneimittel
Anilin ist eine stabile, wenn auch unbedeutende Quelle für die Herstellung von Analgetika, Antipyretika, Antiallergika und Vitaminen. Obwohl die Produktion von Anilin für Arzneimittel in den nächsten fünf Jahren voraussichtlich zunehmen wird, wird es aufgrund der wachsenden Beliebtheit der Fermentationstechnologie zu einem entsprechenden Rückgang bei der Verwendung für die Vitaminproduktion kommen.
4.6 Cyclohexylamin/Dicyclohexylamin
In den 1990er Jahren wurde Anilin zum bevorzugten Rohstoff für die Herstellung von Cyclohexylamin und Dicyclohexylamin. Diese Amine werden hauptsächlich als Zwischenprodukte für Sulfenamid-Vulkanisationsbeschleuniger verwendet. Cyclohexylamin wird auch in großen Mengen als Korrosionsinhibitor und Ausgangsstoff für Cyclamate verwendet.
Der Einsatz dieser Amine in Beschleunigern und der Wasseraufbereitung wird voraussichtlich jährlich um etwa 3–4 % zunehmen, während die Nachfrage nach Cyclohexylamin für die Herstellung von Cyclamaten erheblichen Schwankungen unterliegt und schwer vorherzusagen ist. Sollte die FDA das Verbot von Cyclamaten als künstliche Süßstoffe in den USA aufheben, ist mit einem Anstieg der Nachfrage zu rechnen.
4.7 Sonstiges
Neben einer Vielzahl weiterer Verwendungsmöglichkeiten (z. B. Alkylanilin-Herstellung, optische Aufheller, Sulfonsäuren etc.) ist der Verbrauch von Anilin für die Synthese von Aramidfasern zu erwähnen.
Aramide sind vielseitig einsetzbar und können als Ersatz für Stahl verwendet werden, mit gleichwertigen Verstärkungseigenschaften bei deutlich geringerem Gewicht. Aramide verzeichnen aufgrund ihrer Anwendung in verschiedenen Branchen, beispielsweise beim Ersatz von Asbest in Bremsbelägen, gute Wachstumsraten.
Referenz
- Aniline; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_303.pub2
