1,3-propanediol: production, réactions et utilisations

Le 1,3-propanediol est un liquide clair, incolore et inodore qui est miscible avec l’eau, les alcools, les éthers et le formamide. Il est peu soluble dans le benzène et le chloroforme.
Le 1,3-propanediol est un monomère important pour produire des polyesters, des polyuréthanes et des polyéthers.
La demande de 1,3-propanediol a considérablement augmenté depuis le début du 21e siècle et de nouvelles voies de production ont fait baisser son prix.
Table des matières
1. Production de 1,3-propanediol
1.1. Hydrogénation du 3-hydroxypropanal
Le 1,3-propanediol est préparé par un procédé en deux étapes impliquant l’hydrolyse de l’acroléine en 3-hydroxypropanal suivie d’une hydrogénation.
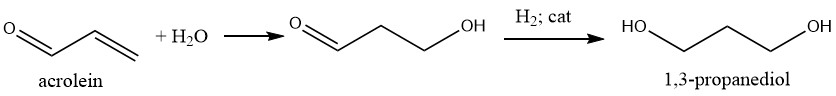
L’hydrolyse est effectuée dans des conditions faiblement acides dans de l’eau contenant initialement env. 20% d’acroléine.
Des concentrations plus élevées d’acroléine ont tendance à conduire à de plus grandes quantités de sous-produits indésirables à la suite de la réaction entre l’acroléine et l’hydroxypropanal.
Le 3-hydroxypropanal peut être directement hydrogéné en phase aqueuse ; cependant, la technique préférée consiste à extraire l’aldéhyde dans un solvant organique, en particulier le 2-méthylpropanol, puis à hydrogéner l’aldéhyde pour donner le diol.
L’hydrogénation est conduite avec du nickel de Raney sous pression dans la phase aqueuse et avec des catalyseurs supportés au nickel à 2-4 MPa et 110-150°C dans la phase organique. Le diol est ensuite séparé du solvant et de l’eau par distillation.
Le rendement en produit désiré par cette voie est d’environ 45 % relativement faible.
La manipulation de l’acroléine dans le processus de production doit être soigneusement contrôlée.
Ce procédé a été utilisé pour la production de 1,3-propanediol par Degussa-DuPont jusqu’au début des années 2000 et a été remplacé par la production biotechnologique.
1.2. Hydroformylation de l’oxyde d’éthylène
Une technique alternative pour synthétiser le 1,3-propanediol est l’hydroformylation de l’oxyde d’éthylène qui a été largement étudiée par Shell.

Dans une première étape, l’oxyde d’éthylène réagit avec le monoxyde de carbone en présence d’un catalyseur organométallique pour produire un 3-hydroxypropanal, qui est ensuite réduit en diol par hydrogénation pour donner du 1,3-propanediol avec un bon rendement (92%).
Comme l’oxyde d’éthylène est moins cher que le 3-hydroxy-propanal, cette méthode est légèrement plus avantageuse.
Néanmoins, la production ou l’utilisation de composés toxiques dans les deux procédés est un inconvénient ainsi que la nécessité d’appliquer des pressions et des températures.
1.3. Désoxygénation sélective du glycérol
Le glycérol peut être converti par catalyse hétérogène ou homogène en propanediols.

La désoxygénation sélective du glycérol par catalyse hétérogène donne un mélange de 1,3-propanediol (rendement 24%), de 1,2-propanediol (rendement 12%) et de 1-propanol (rendement 28%) lors de l’utilisation d’un catalyseur organométallique sur un dioxyde de zirconium support à 170°C et pression élevée d’hydrogène.
Le 1,3-propanediol peut également être synthétisé avec un rendement global de 72% lorsque l’acide p-toluènesulfonique est utilisé comme catalyseur et que des groupes protecteurs sont employés.
Le processus comprend les étapes suivantes : acétalisation pour protéger les premier et troisième groupes hydroxyle du glycérol, tosylation du groupe hydroxy central, ce qui en fait un meilleur groupe partant, suivie d’une détosylation et d’une hydrogénolyse.
2. Réactions chimiques du 1,3-propanediol
Les propriétés chimiques du 1,3-propanediol sont typiques des alcools. Comme le 1,2-propanediol, le 1,3-propanediol se condense avec les acides carboxyliques à température élevée pour donner des esters.
Il réagit également avec les isocyanates et les chlorures d’acide pour donner respectivement des uréthanes et des esters.
Contrairement au 1,2-propanediol, le 1,3-propanediol possède deux groupes hydroxyle primaires avec une réactivité équivalente.
Le 1,3-propanediol forme facilement des éthers. L’éther 3,3′-dihydroxydipropylique se forme lors du reflux continu du diol.
Le 1,3-propanediol réagit avec les aldéhydes et les cétones, souvent en présence de catalyseurs acides, pour former des 1,3-dioxanes.
Sur l’oxyde d’aluminium à des températures supérieures à 250°C, le 1,3-propanediol se décompose en alcool allylique, propanol et autres produits.
Le 1,3-propanediol réagit avec les diacides pour former des polyesters. Le polyester avec l’acide téréphtalique est signalé comme ayant un point de fusion cristalline de 220°C. Les polyuréthanes peuvent également être synthétisés à partir du 1,3-propanediol.
L’impact environnemental du 1,3-propanediol devrait être faible en raison de sa faible toxicité et de sa biodégradabilité facile.
3. Utilisations du 1,3-propanediol
En tant que diol, le 1,3-propanediol est soumis à bon nombre des mêmes applications polymères que d’autres diols de faible masse moléculaire (par exemple, l’éthylène glycol, le 1,2-propanediol et le 1,4-butanediol).
Son prix relativement élevé a longtemps limité son utilisation à des applications nécessitant des performances très spécifiques. Cependant, le développement de voies de production moins chères a élargi son utilisation.
L’une des applications les plus importantes est son utilisation comme matière première pour produire du polytriméthylène téréphtalate (PTT).
De plus, le 1,3-propanediol trouve une application comme agent antigel et liquide de refroidissement.
De plus, c’est une source de matière première pour les 1,3-dioxanes. Le 1,3-propanediol-bis(4-aminobenzoate) peut être utilisé comme allongeur de chaîne dans les élastomères de polyuréthane.
Ce bisbenzoate, qui peut également être synthétisé à partir du 1,3-dichloropropane, trouve d’autres applications comme agent de réticulation dans les formulations époxy et comme additif de caoutchouc.
Les références
- Propanediols, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a22_163.pub2
