1,3-Propanodiol: producción, reacciones y usos

El 1,3-propanodiol es un líquido transparente, incoloro e inodoro que es miscible con agua, alcoholes, éteres y formamida. Tiene solubilidad limitada en benceno y cloroformo.
Este compuesto sirve como un monómero importante en la fabricación de poliésteres, poliuretanos y poliéteres.
En los últimos años, la demanda de 1,3-propanodiol ha experimentado un crecimiento significativo y el descubrimiento de nuevos métodos de producción ha dado lugar a una disminución de su coste.
Tabla de contenido
1. Producción de 1,3-propanodiol
1.1. Hidrogenación de 3-hidroxipropanal
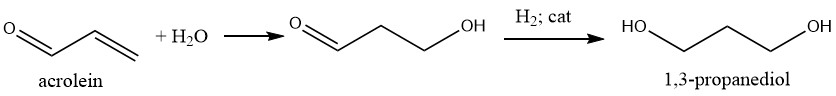
El 1,3-propanodiol se puede sintetizar mediante un proceso de dos pasos que implica la hidrólisis de acroleína a 3-hidroxipropanal seguida de hidrogenación.
Durante la hidrólisis, se emplea agua en condiciones débilmente ácidas, con una concentración inicial de acroleína en agua de alrededor del 20%. Las concentraciones elevadas de acroleína tienden a generar más subproductos indeseables debido a la reacción entre la acroleína y el hidroxipropanal.
Es posible la hidrogenación directa de 3-hidroxipropanal en la fase acuosa, aunque el método preferido implica extraer el aldehído en un disolvente orgánico, principalmente 2-metilpropanol, y posteriormente hidrogenarlo para producir el diol.
La hidrogenación se puede llevar a cabo usando níquel Raney bajo presión en la fase acuosa o catalizadores soportados en níquel a 2-4 MPa y 110-150°C en la fase orgánica.
El diol se puede separar del disolvente y del agua mediante destilación. Sin embargo, el rendimiento del producto deseado es relativamente bajo, aproximadamente 45%, usando esta ruta.
Es necesario un control cuidadoso del manejo de la acroleína en el proceso de producción.
Degussa-DuPont utilizó este proceso para la producción de 1,3-propanodiol hasta principios de la década de 2000. Sin embargo, ha sido reemplazada por la producción biotecnológica debido a los peligros de manipulación y las preocupaciones sobre la sostenibilidad.
1.2. Hidroformilación de óxido de etileno
Un método que Shell ha investigado exhaustivamente para sintetizar 1,3-propanodiol es la hidroformilación del óxido de etileno.
En el paso inicial, el monóxido de carbono y el óxido de etileno reaccionan en presencia de un catalizador organometálico para generar 3-hidroxipropanal, que posteriormente se reduce mediante hidrogenación para obtener 1,3-propanodiol con alto rendimiento (92%).
Este método proporciona una ligera ventaja ya que el óxido de etileno es menos costoso que el 3-hidroxipropanal. Sin embargo, una desventaja de ambos procedimientos es la producción o el uso de sustancias peligrosas, así como la necesidad de presiones y temperaturas elevadas.

1.3. Desoxigenación selectiva de glicerol
El glicerol se puede transformar en propanodioles mediante catálisis heterogénea u homogénea.
Cuando se emplea un catalizador organometálico sobre un soporte de dióxido de circonio a una presión elevada de hidrógeno y 170°C, la desoxigenación selectiva de glicerol da como resultado una mezcla de 1,3-propanodiol (rendimiento del 24%), 1,2-propanodiol (rendimiento del 12%). ), y 1-propanol (rendimiento del 28%).
Utilizando ácido p-toluenosulfónico como catalizador y grupos protectores también se puede conseguir un rendimiento global del 72% para el 1,3-propanodiol. Este proceso implica acetalización para proteger el primer y tercer grupo hidroxilo del glicerol, tosilación del grupo hidroxi central para convertirlo en un mejor grupo saliente, seguido de detosilación e hidrogenólisis.

2. Reacciones químicas del 1,3-propanodiol
El 1,3-propanodiol muestra las propiedades típicas de los alcoholes. A temperaturas elevadas, puede condensarse con ácidos carboxílicos para formar ésteres, similares al 1,2-propanodiol.
Además, puede reaccionar con cloruros de ácido e isocianatos para formar ésteres y uretanos, respectivamente. A diferencia del 1,2-propanodiol, el 1,3-propanodiol posee dos grupos hidroxilo primarios que exhiben una reactividad equivalente.
El 1,3-propanodiol tiende a formar éteres fácilmente. Específicamente, tras un reflujo prolongado, se puede producir éter 3,3´-dihidroxidipropílico. El 1,3-propanodiol también puede formar 1,3-dioxanos al reaccionar con aldehídos y cetonas, a menudo en presencia de catalizadores ácidos.
Cuando se expone al óxido de aluminio a temperaturas superiores a 250 °C, el 1,3-propanodiol se descompone en alcohol alílico, propanol y otros subproductos.
También se puede utilizar para formar poliésteres con diácidos, y se sabe que el poliéster resultante con ácido tereftálico presenta un punto de fusión cristalino de 220°C.
Los poliuretanos también se pueden sintetizar a partir de 1,3-propanodiol.
Debido a su baja toxicidad y su naturaleza fácilmente biodegradable, se espera que el 1,3-propanodiol tenga un bajo impacto ambiental.
3. Usos del 1,3-propanodiol
El 1,3-propanodiol, al ser un diol, comparte numerosas aplicaciones poliméricas con otros dioles de baja masa molecular como el etilenglicol, el 1,2-propanodiol y el 1,4-butanodiol.
Sin embargo, su uso se limitó a aplicaciones que exigían características de rendimiento muy específicas durante un período significativo debido a su costo relativamente elevado. No obstante, el desarrollo de rutas de producción rentables ha ampliado su utilidad.
Una de las aplicaciones más importantes es su uso como material de partida para producir tereftalato de politrimetileno (PTT).
Además, el 1,3-propanodiol se emplea como agente anticongelante y refrigerante.
Sirve como fuente de materia prima para los 1,3-dioxanos.
El bis(4-aminobenzoato) de 1,3-propanodiol puede funcionar como extensor de cadena en elastómeros de poliuretano. Este bisbenzoato, que también puede sintetizarse a partir de 1,3-dicloropropano, encuentra aplicaciones adicionales como agente reticulante en formulaciones epoxi y como aditivo para caucho.
Referencia
- Propanediols, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a22_163.pub2
