Butanona: reacciones, producción y usos
La butanona, también conocida como metiletilcetona, es una cetona alifática y, junto con la acetona, la cetona producida comercialmente más importante. Es un líquido inflamable, incoloro y de baja viscosidad con un olor característico a cetona similar al de la acetona.
La butanona se sintetiza principalmente mediante el proceso de deshidrogenación del 2-butanol, similar a la producción de acetona mediante la deshidrogenación de alcohol isopropílico gaseoso utilizando catalizadores de cobre, zinc o bronce a temperaturas que oscilan entre 400 y 550 °C.
La conversión de 2-butanol alcanza del 80 al 95% y la selectividad de la butanona supera el 95%. Los subproductos incluyen butenos formados por deshidratación y cetonas superiores resultantes de la autocondensación. La producción mundial de metiletilcetona alcanzó aproximadamente 1 millón de toneladas en 2005.
Tabla de contenido
Desde la década de 1980, ha habido un interés creciente en la utilización de 2-butanona como disolvente en pinturas y adhesivos. La metiletilcetona, en particular, se considera un competidor del acetato de etilo, especialmente cuando se utiliza como disolvente de bajo punto de ebullición.
Su versatilidad como disolvente se extiende a diversas aplicaciones como nitrocelulosa, acetato-butirato de celulosa, etilcelulosa, resinas acrílicas, acetatos de vinilo y copolímeros de cloruro de vinilo-acetato de vinilo, principalmente en la preparación de revestimientos de superficies sintéticos.
Su idoneidad como disolvente de lacas se atribuye a su baja viscosidad, alta concentración de sólidos y amplia gama de diluyentes compatibles.
La eliminación de la metiletilcetona de la lista de contaminantes atmosféricos peligrosos (HAP) en 2005 jugó un papel importante en el mantenimiento de la posición de mercado de la butanona en los Estados Unidos. Además, la butanona encuentra utilidad como activador en reacciones oxidativas, agente extractivo selectivo, disolvente especializado para desparafinar fracciones de aceite mineral y producto químico intermedio.
1. Propiedades físicas de la butanona
La butanona es un disolvente de evaporación rápida y de bajo punto de ebullición con un punto de ebullición de 79,6 °C. Es sólo parcialmente miscible con agua, mientras que es completamente miscible con la mayoría de los disolventes orgánicos.
La metiletilcetona forma mezclas azeotrópicas binarias y ternarias en combinación con agua y varios compuestos orgánicos.
Las propiedades físicas de la butanona incluyen:
- Masa molar = 72,1 g/mol
- punto de fusión = -86,7 °C
- Densidad del líquido a 25 °C = 0,7995
- Índice de refracción a 25 °C = 1,736
- Viscosidad del líquido a 25 °C = 0,395 mPa.s
- Solubilidad a 20 °C en agua = 27,5 %
2. Reacciones químicas de la butanona
En condiciones normales y en ausencia de oxígeno atmosférico, la butanona es estable. Se debe tener cuidado después de un almacenamiento prolongado porque se forma peróxido de metiletilcetona en presencia de oxígeno. Pueden producirse explosiones debido a la descomposición instantánea de los peróxidos.
La 2-butanona es insaponificable y resistente al calor y a la luz. Sin embargo, se descompone después de una exposición prolongada a los rayos UV para producir etano, metano, monóxido de carbono, etileno y diacetilo.
El diacetilo se forma por oxidación de metiletilcetona con aire en presencia de catalizadores especiales.
El peróxido de metiletilcetona, un catalizador de polimerización, se forma mediante la oxidación de butanona con una solución de peróxido de hidrógeno.
El ácido nítrico y otros oxidantes fuertes oxidan la butanona a una mezcla de ácido fórmico y ácido propiónico.
El 2-butanol se obtiene por reducción catalítica de butanona con hidrógeno, por reducción electrolítica en solución de acetato de sodio o por reducción con amalgama de amonio o hidruro de litio y aluminio.
Otro producto de reducción es el 3,4-dimetil-3,4-hexanodiol que se obtiene por reducción electrolítica de metiletilcetona en medio ácido o por reducción con amalgama de magnesio.
La metiletilcetona exhibe reactividad hacia el cianuro de hidrógeno y los hidrogenosulfitos de sodio y potasio, lo que resulta en la formación de productos de adición.
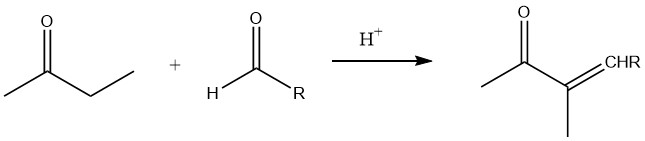
En condiciones alcalinas, la 2-butanona sufre reacciones de condensación con aldehídos, lo que lleva a la producción de cetonas más insaturadas. En particular, cuando se utiliza formaldehído, se produce metil isopropil cetona como intermediario para síntesis posteriores, lo que presenta un área de interés específica.
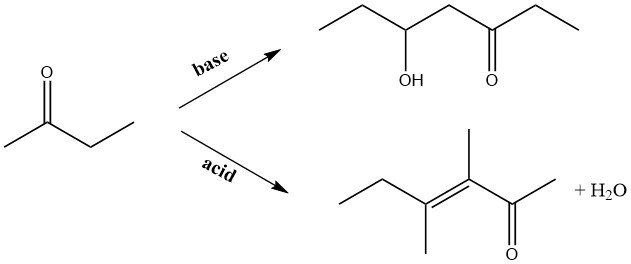
Durante la autocondensación catalizada por bases en fase líquida o la condensación en fase gaseosa sobre catalizadores de cobre alcalinizados, el grupo carbonilo de la molécula reacciona con el grupo metilo. Por el contrario, en la condensación catalizada por ácido, el grupo metileno adyacente al grupo carbonilo se convierte en el sitio de ataque.
La condensación de butanona y citral da como resultado la formación de metilpseudoionona, que posteriormente puede someterse a ciclación para producir metilionona. Este compuesto se emplea en la producción de perfumes sintéticos de violeta.
En presencia de aldehídos de bajo peso molecular, específicamente durante la aldolización catalizada por bases y por ácidos, la posición α del grupo carbonilo está involucrada principalmente en la reacción.
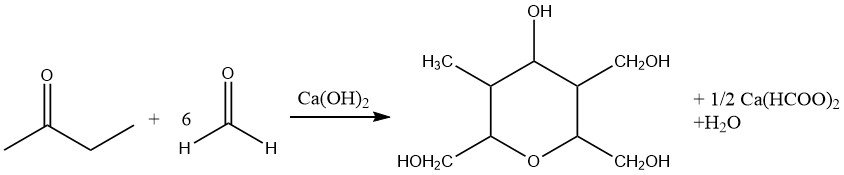
Por lo tanto, emplear cantidades inferiores a las estequiométricas de formaldehído en la aldolización catalizada por bases conduce a la formación de 2-metilbutano-1-ol-3-ona. Además, la hidroximetilación exhaustiva acompañada de la reducción del grupo carbonilo (reacción de Cannizzaro cruzada) produce desoxianhidroeneaheptita.
Cuando la metiletilcetona reacciona con alcoholes primarios y secundarios, produce cetonas superiores. La reacción con alcohol sec-butílico da como resultado específicamente la formación de etil amil cetona.
La metiletilcetona exhibe reactividad hacia compuestos polioxi o epóxidos, lo que lleva a la formación de productos cíclicos.
El nitrito de amilo ataca selectivamente al grupo CH2 en posición α del grupo carbonilo, dando la monooxima de diacetilo.
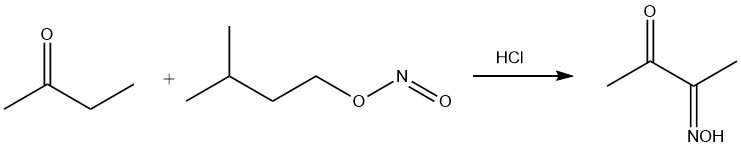
El grupo ceto reacciona con los grupos amino, lo que resulta en la eliminación de agua. En combinación con hidroxilamina, esta reacción produce metil etil cetoxima, un agente antipiel.
La condensación de butanona con ésteres y anhídridos alifáticos produce β-dicetonas.
Los fenoles sufren reacciones con metiletilcetona, formando compuestos de oxifenileno. Cuando se hace reaccionar con fenol, se obtiene 2,2-hidroxifenilbutano, un homólogo del hidroxifenilpropano (bisfenol A). El bisfenol A es un material importante utilizado en la producción de resinas sintéticas.
La metiletilcetona se puede someter a halogenación en la posición α. Además, reacciona con compuestos de Grignard, dando como resultado la formación de alcoholes terciarios.
En presencia de acetileno y amida de sodio, se sintetiza 3-metil-1-pentin-3-ol. Combinando 2-butanona con N-metilformamida, se puede obtener N-metil-formil-aminobutano. Además, la reacción de Reformatzky permite la producción de β-oxiésteres utilizando ésteres sustituidos con monobromo.
3. Producción de butanona
El método principal para la producción de butanona implica la deshidrogenación de 2-butanol (alcohol sec-butílico, SBA). Esta técnica de proceso se emplea en aproximadamente el 92% de las capacidades de producción global, como se informó en 2006.
El 2-butanol se puede obtener fácilmente mediante un proceso de dos pasos de hidratación de n-butenos derivados de refinados C4 petroquímicos. En este proceso se utiliza ácido sulfúrico líquido como catalizador. Alternativamente, un procedimiento de un solo paso implica la adición directa de agua a una resina de intercambio iónico ácida estabilizada, que sirve como catalizador.
El 8% restante de metiletilcetona se produce mediante un método de producción fatal mediante la síntesis de Fischer-Tropsch o mediante oxidación catalítica de n-butano líquido, lo que da como resultado la producción de ácido acético y metiletilcetona como subproducto.
3.1. Deshidrogenación catalítica de alcohol sec-butílico en fase gaseosa
La deshidrogenación del alcohol sec-butílico (SBA) utilizando catalizadores de cobre, zinc o bronce es una reacción endotérmica con un cambio de calor (ΔH) de -51 kJ/mol. El aumento de la temperatura conduce a una elevación de la concentración de butanona en la mezcla de reacción, que se estabiliza en aproximadamente 350 °C, suponiendo que no se produzcan reacciones posteriores.
En la deshidrogenación en fase gaseosa, el cobre es el catalizador preferido, mientras que los catalizadores de zinc o bronce normalmente requieren temperaturas de deshidrogenación más altas (400 °C).
Los catalizadores de óxido de zinc a menudo exhiben una selectividad más baja debido a una reacción secundaria que involucra la deshidratación de SBA a n-butenos. Para la deshidrogenación del SBA se recomiendan catalizadores como platino sobre alúmina, cobre o cromo, y cobre y zinc sobre alúmina, especialmente cuando el SBA contiene cantidades importantes de agua.
Los catalizadores comerciales se reactivan mediante oxidación con aire después de 3-6 meses de uso. La reactivación se vuelve necesaria cuando la tasa de conversión de alcohol disminuye con el tiempo debido a la contaminación de los sitios catalíticos activos por agua, depósitos de oligómeros de buteno y éter di-sec-butílico. Se emplean temperaturas más altas y oxidación para eliminar estos contaminantes.
Normalmente, los catalizadores comerciales presentan una vida útil de varios años o más. Deutsche Texaco ha desarrollado una tecnología de proceso para la producción de metiletilcetona basada en la deshidrogenación de alcohol sec-butílico anhidro utilizando un catalizador de precipitación a base de cobre a temperaturas de 240-260 °C bajo presión normal.
En esta tecnología, el alcohol sec-butílico se produce mediante la hidratación directa de n-butenos catalizada por una resina de intercambio iónico ácida con temperatura estabilizada. A pesar de este procedimiento heterogéneo mejorado, el ácido sulfúrico concentrado sigue siendo el principal catalizador en todo el mundo para la producción de SBA por vía indirecta.
En la ruta indirecta, el sulfato mono o di-sec-butilo intermedio resultante de la primera etapa de reacción se hidroliza en una etapa de reacción posterior.
El alcohol sec-butílico líquido se vaporiza en un evaporador y la corriente de alcohol gaseoso resultante se dirige a un reactor multitubular, donde tiene lugar la deshidrogenación sobre un catalizador de cobre. La corriente de producto gaseoso sale del reactor y, después de enfriar a temperatura ambiente, se separa en una fase líquida de metiletilcetona cruda y una fase de hidrógeno gaseoso.
La corriente líquida todavía contiene algo de SBA sin convertir, junto con 5-metil-3-heptanona, cetonas superiores y agua, además de la metiletilcetona deseada. La formación de 5-metil-3-heptanona, cetonas superiores y agua se produce mediante la autocondensación de dos o más moléculas de metiletilcetona.
La 2-butanona se purifica mediante tres pasos de destilación consecutivos bajo presión atmosférica. En el primer paso, se recoge una corriente azeotrópica de butanona y agua como producto de cabeza, que se purifica adicionalmente en una columna de destilación discontinua separada.
La segunda columna produce la metiletilcetona pura deseada (típicamente con una pureza superior al 99%) junto con SBA mezclado con cetonas superiores como producto de fondo. En el paso de destilación final, el SBA no convertido se destila como producto de cabeza y se devuelve al tanque de alimentación del proceso. Los productos finales de este paso consisten en las cetonas superiores formadas como subproductos durante el proceso de síntesis.
3.2. Metiletilcetona como subproducto del proceso de conversión de carbón a líquido de Fischer-Tropsch
En el proceso Fischer-Tropsch se produce una conversión catalítica de monóxido de carbono e hidrógeno, conocido como gas de síntesis, para producir hidrocarburos líquidos. Este proceso produce una amplia gama de longitudes de cadenas de hidrocarburos y una cantidad significativa de diversos subproductos.
Desarrollado originalmente en la década de 1920 por los investigadores alemanes Franz Fischer y Hans Tropsch, el proceso Fischer-Tropsch ha sido utilizado comercialmente y mejorado por SASOL Ltd., una empresa sudafricana, desde 1955 para la producción de combustibles sintéticos a partir de carbón.
El proceso implica una técnica de dos pasos. Inicialmente, el carbón mineral se gasifica para generar gas de síntesis, que luego se somete a una purificación exhaustiva mediante absorción en sistemas depuradores, utilizando tecnología Rectisol. A continuación, el gas de síntesis purificado se convierte catalíticamente en hidrocarburos.
Además de los productos primarios como olefinas, combustible sintético y ceras, se produce como subproductos una amplia gama de oxigenados solubles en agua, que representan aproximadamente del 3 al 6 % de selectividad en la corriente de agua durante la reacción.
Se emplean tecnologías de separación tradicionales para purificar estos oxigenados, que incluyen alcoholes, ácidos orgánicos, aldehídos, butanona y otras cetonas, en productos solventes de alto valor.
3.3. Oxidación en fase líquida de n-butano
En la oxidación en fase líquida de n-butano a ácido acético, la 2-butanona es un subproducto de la reacción. Este proceso implica la autooxidación u oxidación directa del n-butano en fase líquida a través de una vía de reacción radicalaria.
La oxidación inicial produce metiletilcetona como producto intermedio, que, tras una oxidación adicional, forma hidroperóxido de metiletilcetona. El hidroperóxido de metiletilcetona se escinde posteriormente en dos moléculas, dando como resultado el ácido acético deseado como producto final.
Union Carbide Corp. ha desarrollado un proceso de flujo pistón continuo que permite la recolección parcial de la butanona intermedia. Este proceso implica oxidación en fase líquida no catalizada a 180 °C y 5,3 MPa, con algo de retromezcla. Mediante este proceso se obtienen tanto metiletilcetona como ácido acético.
En condiciones de oxidación continua con flujo tipo pistón a 150 °C, 6,5 MPa y un tiempo de residencia de 2,7 minutos, se forman metiletilcetona y ácido acético en proporciones de masa de hasta 3/1.
Celanese Corp. utiliza ácido acético como disolvente, empleando un sistema catalizador de oxidación disuelto homogéneamente que consta de acetato de cobalto y acetato de sodio. Este proceso discontinuo se lleva a cabo a temperaturas entre 160 y 165 °C y a una presión de 5,7 MPa. Los productos resultantes son butanona y ácido acético, con una relación de masa de 0,4/1,0.
3.4. Oxidación del sec-butilbenceno
La tecnología SPAM de Hock Phenol Synthesis Shell, que combina fenol, acetona y butanona, se basa en la oxidación de una mezcla de sec-butilbenceno y cumeno a sus respectivos compuestos de hidroperóxido. A continuación, estos hidroperóxidos se escinden convencionalmente usando un ácido inorgánico, preferiblemente ácido sulfúrico, dando como resultado una mezcla de fenol, metiletilcetona y acetona como productos deseados.
En este caso, la corriente de cetona bruta se separa del fenol mediante destilación y posteriormente se purifica para obtener los componentes cetónicos puros deseados. La escisión catalítica del hidroperóxido de sec-butilbenceno (sBHP) con un ácido inorgánico para producir fenol y butanona es un proceso bien conocido desde hace muchos años.
Sin embargo, a pesar de la importancia industrial de la 2-butanona en comparación con la acetona, esta ruta alternativa no se ha comercializado debido a un desafío importante encontrado durante el paso de oxidación. La velocidad de oxidación autocatalítica del sec-butilbenceno es varias veces más lenta que la del cumeno, lo que lleva a reacciones secundarias no deseadas que afectan negativamente el rendimiento general de los productos deseados.
Según la investigación de Shell, la disminución de la velocidad de reacción durante la oxidación del sec-butilbenceno se atribuye a la formación de productos escindidos que actúan como eliminadores de radicales en la mezcla de reacción, presentes en concentraciones de partes por millón (ppm). Estos ácidos eliminadores incluyen ácido fórmico, ácido acético y fenol.
Para superar el impacto negativo en la velocidad de reacción, se han sugerido las siguientes opciones:
- Usar una mezcla de sec-butilbenceno y cumeno para establecer cantidades iniciales de hidroperóxido de cumeno (CHP) en el primer paso de reacción, que actúa como iniciador.
- Reducir la formación de metanol o etanol como productos escindidos en corrientes de reciclaje, minimizando así la producción de los ácidos eliminadores antes mencionados.
- Introducir una solución acuosa de amoníaco hasta cierto punto, permitiendo que los ácidos formen sus sales de amonio, evitando al mismo tiempo la división de fases.
3.5. Oxidación directa de n-butenos (proceso Hoechst-Wacker)
El proceso Hoechst-Wacker implica la oxidación directa de n-butenos, donde el oxígeno se transfiere en una fase homogénea utilizando un par de sales redox, PdCl2/2CuCl. Posteriormente, el par de sales sufre una reoxidación.
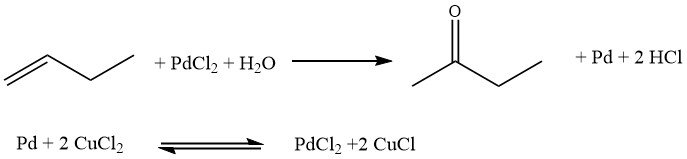
Sin embargo, este proceso tiene ciertos inconvenientes. Esto conduce a la formación de butanonas cloradas y n-butanal, que son subproductos indeseables. Además, pueden surgir problemas de corrosión debido a la presencia de ácidos libres.
En este proceso, el oxígeno se transfiere utilizando una solución acuosa de sulfato de paladio y sulfato férrico. Se han empleado principios de transferencia de oxígeno similares en otros procesos desarrollados por el Consorcio de Electroquímica y Eastman Kodak.
4. Usos de la butanona
La butanona, también conocida como metiletilcetona, es un valioso disolvente con propiedades similares a la acetona. Ofrece varias ventajas en comparación con otros disolventes con tasas de evaporación similares:
- Alto poder de disolución: la butanona exhibe una gran capacidad para disolver diversas sustancias.
- Alta proporción de materia disuelta a viscosidad: puede disolver una gran cantidad de material manteniendo una viscosidad favorable.
- Miscibilidad con hidrocarburos: la butanona se puede mezclar con numerosos hidrocarburos sin afectar el contenido de sólidos o la viscosidad.
- Relación volumen-masa favorable: Debido a su baja densidad, proporciona un equilibrio ventajoso entre volumen y masa.
La 2-butanona tiene la capacidad de disolver una amplia gama de sustancias naturales, plásticos y resinas, incluidas colofonia, resinas éster, nitrocelulosa, derivados de celulosa (como acetato de celulosa y acetobutirato de celulosa), resinas epoxi, resinas alquídicas, resinas fenólicas y resinas vinílicas. polímeros de acetato y muchos otros.
Sin embargo, no puede disolver sólo parcialmente el triacetato de celulosa, el acetato de celulosa de alto peso molecular, el poli(cloruro de vinilo), el poli(vinilbutiral), el caucho de polisulfuro y la goma laca.
El disolvente encuentra aplicaciones en diversas industrias, como la producción de pinturas, lacas y barnices, así como en diluyentes de pintura, adhesivos, cementos, selladores, cintas magnéticas, cuero artificial, papel transparente, tintas de impresión, limpiadores de equipos electrónicos, cosméticos, productos farmacéuticos, desengrasado de superficies metálicas y procesos de extracción.
La butanona también se utiliza como agente aromatizante sintético en alimentos y productos farmacéuticos, como esterilizador de instrumentos quirúrgicos y equipos dentales, y en la fabricación de polvos sin humo.
Aunque su uso principal es como disolvente, la butanona tiene una importancia limitada como materia prima química. Sin embargo, puede sufrir diversas reacciones, como condensación con formaldehído para producir metil isopropenil cetona, autocondensación para formar etil amil cetona y condensación mixta con acetona para obtener metil amil cetona.
MEK se utiliza en la producción de perfumes, antioxidantes, catalizadores, peróxidos y diacetales. La metil etil cetoxima en una aplicación menor se emplea como agente antipiel en lacas.
Además, el peróxido de butanona sirve como iniciador de polimerización para poliésteres insaturados.
En la industria del perfume, la 2-butanona reacciona con el citral para producir componentes de fragancia como la metilpseudoionona. Además, está aprobado como desnaturalizante del alcohol en la República Federal de Alemania desde 1962 (según lo decretado por el Bundesmonopolverwaltung en Offenbach).
Referencia
- 2-Butanone, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a04_475.pub2
