Methacrylsäure: Eigenschaften, Herstellung und Verwendung
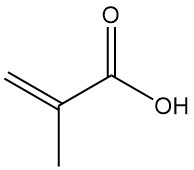
Methacrylsäure, auch bekannt als α-Methylacrylsäure oder 2-Methylpropensäure, ist eine organische Säure mit der Formel CH2=C(CH3)COOH. Es ist eine farblose, mäßig flüchtige, ätzende Flüssigkeit mit stark beißendem Geruch.
Methacrylsäure wurde erstmals 1865 aus Ethylmethacrylat hergestellt, das durch Dehydratisierung von Ethyl-α-hydroxyisobutyrat hergestellt wurde.
Inhaltsverzeichnis
1. Geschichte von Methacrylsäure und Methacrylaten
Die wissenschaftliche Erforschung von Acrylaten und Methacrylaten für kommerzielle Anwendungen begann mit der Doktorarbeit von OTTO ROEHΜ im Jahr 1901. Er untersuchte die Polymerisationsprodukte von Acrylsäure-Derivate und stellte sich deren mögliche industrielle Verwendung vor.
Roehml berichtete über die Synthese transparenter, gummiartiger Materialien, doch es fehlten seinerzeit effiziente Produktionsmethoden. 1907 gründete er gemeinsam mit OTTO HAAS ein Unternehmen, das sich auf Lederbehandlungsenzyme konzentrierte.
In den 1920er Jahren kam es zu bedeutenden Fortschritten bei der kommerziellen Herstellung von Acrylaten und Methacrylaten. Nach dem Ersten Weltkrieg entwickelte Roehml ein Verfahren zur großtechnischen Acrylatproduktion unter Verwendung von Ethylencyanhydrin, einem aus Ethylenchlorhydrin abgeleiteten Zwischenprodukt.
Später entwickelte er zusammen mit Walter Bauer ein ähnliches Verfahren für Methylmethacrylat unter Verwendung von Acetoncyanhydrin. Bis 1931 gelang es Bauer, ein klares und transparentes Methylmethacrylat-Polymer herzustellen, das über 100 °C erweicht.
In den 1930er Jahren wurde von Rohm and Haas und Du Pont (USA), Rohm and Haas AG (Deutschland) und ICI (England) intensiv an der Herstellung von Gussplatten aus Methylmethacrylat geforscht.
Die erste kommerzielle Produktion von Methylmethacrylat-Monomer begann 1933 in Darmstadt über die Acetoncyanhydrin-Route, bei der das Cyanhydrin in Ethyl-α-hydroxyisobutyrat umgewandelt und anschließend mit P2O5.
ICI sicherte sich 1934 ein Patent für ein alternatives Verfahren, bei dem Acetoncyanhydrin mithilfe konzentrierter Schwefelsäure in Methacrylamidsulfat umgewandelt wurde. Methacrylsäure, die durch Hydrolyse von Methacrylamidsulfat gewonnen wird, könnte dann zu Methylmethacrylat verestert werden.
Die Rohm und Haas AG erkannte die Effizienz des ICI-Verfahrens und schloss eine gegenseitige Lizenzvereinbarung für die Produktion von gegossenen Acrylglasplatten ab. Anschließend begannen sowohl ICI als auch Rohm und Haas AG 1937 mit der kommerziellen Methylmethacrylat-Produktion über die Methacrylamidsulfat-Route.
Rohm and Haas in den Vereinigten Staaten, damals seit 1917 ein unabhängiges Unternehmen, nutzte das ursprüngliche Verfahren aufgrund von Lizenzbeschränkungen mehrere Jahre lang weiter.
Die Methacrylamidsulfat-Route blieb bis zur Einführung von Isobuten-Oxidationsprozessen im Jahr 1983 das wichtigste kommerzielle Verfahren zur Herstellung von Methylmethacrylat und Methacrylsäure. Diese Prozesse wurden in Japan unabhängig voneinander von Japan Catalytic Chemical und Mitsubishi Rayon entwickelt.
Während in Japan zusätzliche Kapazitäten für Methacrylsäure auf Isobutenbasis geplant sind und eine neue Anlage auf Ethylenbasis von BASF im Bau ist, wird die Acetoncyanhydrin-Route immer noch für einen erheblichen Teil des weltweiten Bedarfs an Methylmethacrylat genutzt.
Aceton-Cyanhydrin-basierte Verfahren liefern hauptsächlich Methylmethacrylat, das wichtigste Methacrylat-Derivat. Auf anderen Wegen hergestellte Methacrylsäure wird auch als Zwischenprodukt für die Methylmethacrylat-Synthese verwendet.
Kleinere Mengen anderer Methacrylate, darunter Ethylmethacrylat, n-Butylmethacrylat, Isobutylmethacrylat und höhere Homologe wie Laurylmethacrylat und Stearylmethacrylat, werden durch direkte Veresterung von Methacrylsäure oder Umesterung von Methylmethacrylat hergestellt.
Darüber hinaus sind Spezialmonomere wie 2-Hydroxyethylmethacrylat, 2-Hydroxypropylmethacrylat, Aminoalkylmethacrylate (z. B. 2-Dimethylaminoethylmethacrylat) und Methacrylamid im Handel erhältlich. Das Zwischenprodukt Methacrylamidsulfat ist die Vorstufe für die Methacrylamidproduktion.
2. Physikalische Eigenschaften von Methacrylsäure
Methacrylsäure ist eine schwache organische Säure mit einem pKa-Wert von 4,65. Es ist eine klare, farblose Flüssigkeit oder farblose Kristalle mit einem beißenden, abstoßenden Geruch. Es ist in Chloroform löslich und mit Wasser mischbar, Ethanol und Ether.
Die wichtigsten physikalischen Eigenschaften von Methacrylsäure sind in Tabelle 1 aufgeführt.
| Eigenschaft | Wert |
|---|---|
| Molekulargewicht | 86,09 g/mol |
| Schmelzpunkt, °C | 15,8 |
| Siedepunkt (101,3 kPa), °C | 162 |
| Dichte, g/cm3 | 1,015 |
| Brechungsindex | 1,4288 |
| Dampfdruck, kPa |
bei 20 °C: 0,09 bei 60 °C: 1,33 |
| Viskosität (24 °C), mPa·s | 1,38 |
| Löslichkeit in Wasser | Mischbar |
| Kritische Temperatur, °C | 370 |
| Kritischer Druck, Pa | 4,70 |
| Kritisches Volumen, cm3/mol | 270 |
| Verdampfungswärme (101,3 kPa), kJ/mol | 0,418 |
| Spezifische Wärmekapazität, J g-1 K-1 | 2.1 |
| Flammpunkt, °C |
Offener Becher: 77 Geschlossener Becher: 67 |
| Selbstentzündungstemperatur, °C | 400 |
3. Chemische Reaktionen von Methacrylsäure
Methacrylsäure ist sehr reaktiv und zeigt typische Reaktionen sowohl des Alkens als auch der Carbonsäure.
Die elektronenziehende Wirkung der Carbonsäure polarisiert die Doppelbindung und erhöht deren Reaktivität, allerdings ist diese Reaktivität aufgrund der elektronenspendenden Methylgruppe weniger ausgeprägt als bei Acrylsäure.
Daher finden nukleophile Michael- und Michael-ähnliche Additionen an die Doppelbindung nur mit elektronenreichen Reagenzien statt.
3.1. Addition zur Kohlenstoff-Kohlenstoff-Doppelbindung
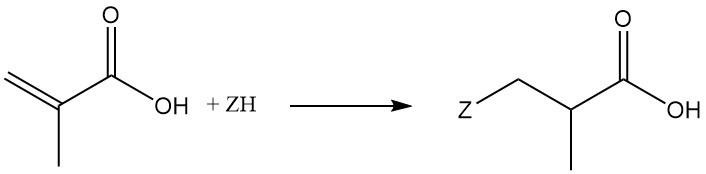
Methacrylsäure reagiert mit Cyanwasserstoff, Halogenwasserstoffen, Schwefelwasserstoff, Mercaptanen, Alkylaminen, Alkoholen, Phenolen oder Phosphinen unter Bildung von β-substituierten α-Methylpropionaten.
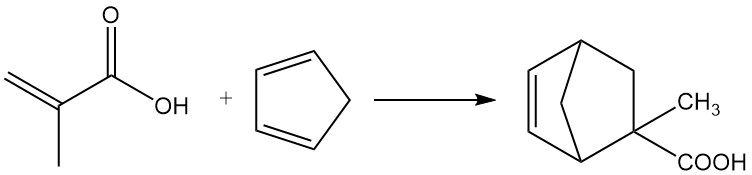
3.2. Diels-Alder-Reaktionen
Methacrylsäure geht Diels-Alder-Reaktionen mit Dienen wie Butadien und Cyclopentadien ein.
3.3. Reaktionen der Carbonsäurefunktion
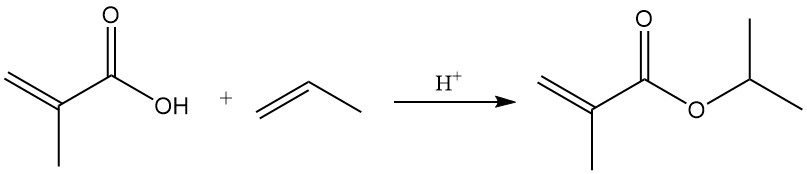
Ester der Methacrylsäure entstehen durch Reaktionen mit Alkoholen in Gegenwart katalytischer Mengen Schwefel- oder Sulfonsäuren. Auch durch säurekatalysierte Addition von Olefinen entstehen Ester.
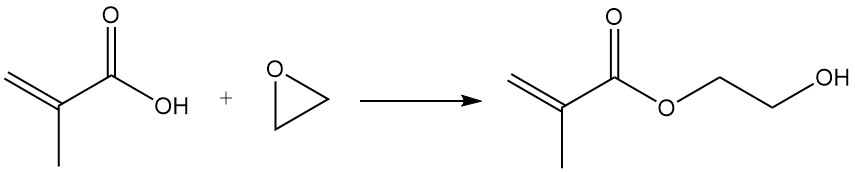
Die Reaktion der Methacrylsäuregruppe mit Epoxiden in Gegenwart von Katalysatoren wie Anionenaustauscherharzen, Eisenchlorid oder Lithiumsalzen ergibt Hydroxyethyl- und Hydroxypropylmethacrylate.
Methacryloylchlorid wird durch die Reaktion der Methacrylsäure mit Thionylchlorid oder Phosphortrichlorid synthetisiert.
Methacrylsäure reagiert mit Essigsäureanhydrid zu Methacrylsäureanhydrid.
3.4. Polymerisation
Polymere aus Methacrylsäure und ihren Derivaten bilden sich leicht beim Erhitzen in Gegenwart von Radikalinitiatoren wie Peroxiden, UV-Licht oder ionisierender Strahlung.
Gängige phenolische Inhibitoren richten sich gegen Peroxyradikale und hemmen den eingeleiteten Polymerisationsprozess nicht. Allerdings ist der Sauerstoffausschluss während der Polymerisation von entscheidender Bedeutung, um die Umwandlung von Alkylradikalen in Hydroperoxyradikale zu verhindern.
4. Industrielle Produktion von Methacrylsäure
Dieser Abschnitt konzentriert sich auf kommerziell realisierbare Methoden zur Herstellung von Methacrylsäure. Für diese Prozesse werden unterschiedliche Rohstoffe verwendet, die nach ihrer Kohlenstoffkettenlänge kategorisiert werden: Ethylen (C2-Route), Propen oder Aceton (C3-Route) und Isobuten (C4-Route).
Die Wirtschaftlichkeit jedes Prozesses hängt von der regionalen Verfügbarkeit und Preisgestaltung der Rohstoffe ab. Derzeit gibt es keine einzige Alternative, die die etablierte Acetoncyanhydrin-Route in wirtschaftlicher Hinsicht übertrifft, was den Weiterbetrieb bestehender Cyanhydrin-basierter Anlagen rechtfertigt.
4.1. Herstellung von Methacrylsäure auf dem Acetoncyanhydrin-Weg
Die gebräuchlichste Methode zur Methacrylsäuresynthese beinhaltet die Hydrolyse von Methacrylamidsulfat, das aus Acetoncyanhydrin gewonnen wird.
Acetoncyanhydrin entsteht durch die Reaktion von trockenem Aceton mit Cyanwasserstoff in Gegenwart eines basischen Katalysators. Dieses Zwischenprodukt reagiert dann mit überschüssiger konzentrierter Schwefelsäure zu Methacrylamidsulfat.
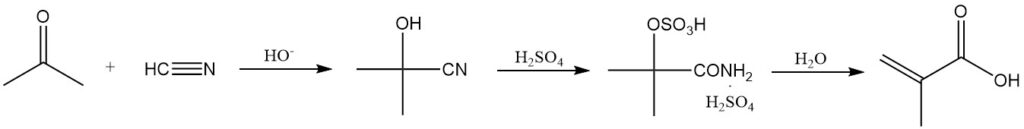
Die Schwefelsäure dient einem doppelten Zweck: als Reaktant und als Reaktionslösungsmittel. Zu wenig Schwefelsäure führt zu einer schwer handhabbaren Reaktionsmischung. Sowohl die Säure als auch das Acetoncyanhydrin müssen wasserfrei sein, um die Bildung von Nebenprodukten zu minimieren.
Die anfängliche Reaktion, die in einer Reihe von Rührkesselreaktoren durchgeführt wird, erfordert eine gute Wärmeübertragung, um den exothermen Prozess zu bewältigen. Gründliches Mischen ist entscheidend, um die Zersetzung des Cyanhydrins in seine Ausgangsstoffe zu verhindern, wodurch unerwünschte Nebenprodukte entstehen können.
Nach der ersten Reaktion (80–110 °C) wird die Mischung einer kurzen thermischen Spaltung (125–160 °C) unterzogen, um den größten Teil des a-Hydroxyisobutyramid-Nebenprodukts zusammen mit etwas Aceton, Kohlenmonoxid und Wasser in das gewünschte Methacrylamidsulfat umzuwandeln .
In der zweiten Stufe wird entweder der Methacrylamidsulfatstrom mit überschüssigem Wasser hydrolysiert, um Methacrylsäure und Ammoniumbisulfat herzustellen, oder er wird in einem kombinierten Hydrolyse-Veresterungsschritt mit wässrigem Methanol behandelt, um eine Mischung aus Methylmethacrylat und Methacrylsäure zu erhalten.
Die Gesamtausbeute bezogen auf Acetoncyanhydrin liegt typischerweise im Bereich von 80–90 %.
Bei der Methacrylsäureproduktion führt die Hydrolyse zu einem Zweiphasengemisch, das eine getrennte Reinigung von Methacrylsäure aus der oberen organischen Schicht und verdünnter wässriger Methacrylsäure aus der unteren Schicht durch Destillation bzw. Dampfstrippung ermöglicht.
Der Wunsch, die Regenerierung von Schwefelsäure und die damit verbundenen Gefahren des Cyanwasserstofftransports zu eliminieren, sind die Hauptgründe für die Erforschung alternativer Produktionsmethoden.
Allerdings profitiert die etablierte Acetoncyanhydrin-Route von dem wirtschaftlichen Vorteil, Aceton (ein Nebenprodukt der Phenolproduktion) und Cyanwasserstoff (ein Nebenprodukt der Acrylnitrilproduktion) als Ausgangsstoffe zu verwenden.
4.2. Herstellung von Methacrylsäure aus Isobuten
In den letzten Jahren haben Unternehmen wie Nihon Methacryl Monomer (ein Joint Venture von Sumitomo und Nippon Shokubai) und Mitsubishi Rayon ein zweistufiges katalytisches Oxidationsverfahren zur Herstellung von Methacrylsäure aus Isobuten oder tert-Butanol entwickelt.
Der Prozess beinhaltet die Oxidation von Isobuten zu Methacrolein, das dann weiter zu Methacrylsäure oxidiert wird.
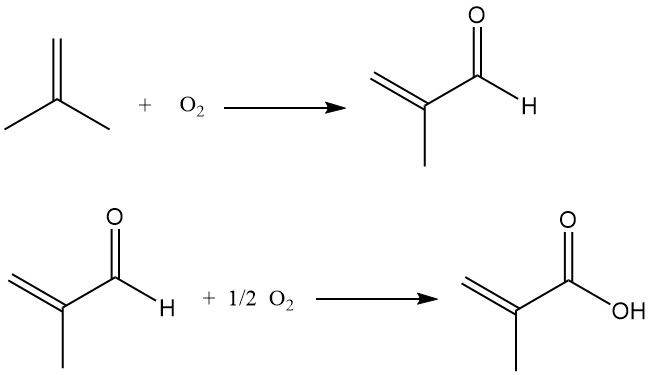
In veröffentlichten Berichten wird dieses Verfahren zur Herstellung von Methacrylsäure aus Isobuten mit einem ähnlichen Verfahren zur Herstellung von Acrylsäure aus Propen verglichen. Die größte Herausforderung besteht in der Aufrechterhaltung einer hohen Katalysatorselektivität während der zweiten Oxidationsstufe, die typischerweise bei moderaten Umwandlungsraten (65–85 %) die beste Leistung erbringt.
Das Sumitomo-Nippon Shokubai-Verfahren (Abbildung 1) überwindet diese Herausforderung, indem es den Reaktor der ersten Stufe mit hoher Umwandlung betreibt und seinen Abstrom direkt dem zweiten Oxidationsreaktor zuführt. Die zweite Stufe arbeitet mit einer niedrigeren Umwandlungsrate, um die Selektivität und Lebensdauer des Katalysators zu optimieren.
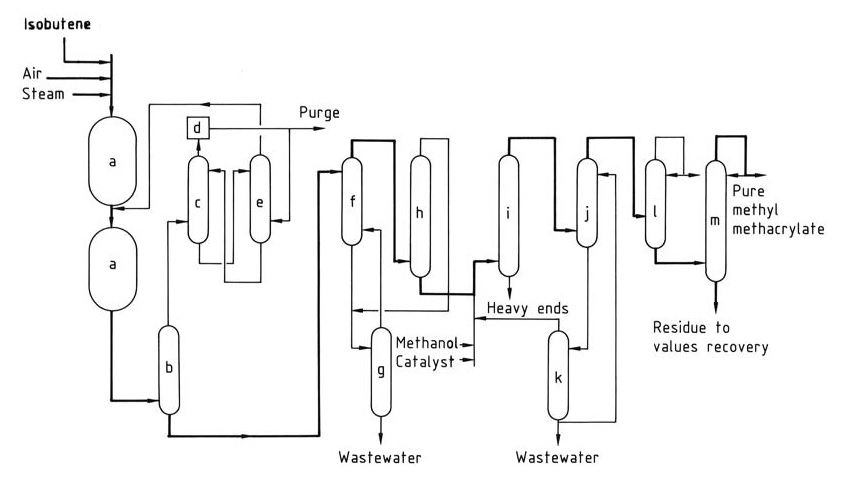
a) Oxidationsreaktoren; b) Quencher; c) Absorber; d) Verbrennungseinheit; e) Methacrolein-Rückgewinnungsturm; f) Lösungsmittelextraktionseinheit; g) Lösungsmittel-Stripping-Turm; h) Lösungsmittelrückgewinnungs-/Dehydratisierungsturm; i) Veresterungsreaktor; j) Extraktor; k) Destillationseinheit; l) Abisolierer für leichte Enden; m) Produktdestillationskolonne.
Anschließend wird nicht umgesetztes Methacrolein aus der zweiten Stufe abgetrennt und recycelt, wodurch eine Gesamtausbeute an Methacrylsäure aus Isobuten von etwa 65–70 % erreicht wird.
Katalysatoren bei der ersten Oxidation sind typischerweise Mehrkomponenten-Metalloxide, die Wismut, Molybdän und andere Metalle enthalten, um die Aktivität zu steigern und die Selektivität zu steuern. Für die zweite Oxidation werden Katalysatoren auf Basis von Phosphomolybdänsäure verwendet. Zusätzliche Elemente wie Kupfer und Vanadium können ebenfalls vorhanden sein.
Der Ausfluss des Oxidationsreaktors der zweiten Stufe wird gequencht (b), um rohe wässrige Methacrylsäure zu erhalten. Der verbleibende Gasstrom wird durch einen Absorber (c) geleitet, wo nicht umgesetztes Methacrolein absorbiert wird (üblicherweise unter Verwendung wässriger Carbonsäure).
Absorberabgase werden vor der Freisetzung verbrannt (d). Ein Teil der verbrannten Gase kann als inertes Verdünnungsmittel in die erste Stufe zurückgeführt werden. Das mit Methacrolein beladene Absorptionsmittel wird zur Rückführung in den Reaktor der zweiten Stufe in einen Rückgewinnungsturm (e) überführt. Die gewonnene Absorptionslösung wird zum Absorber zurückgeführt.
Rohe Methacrylsäure wird einer Lösungsmittelextraktion (f) unterzogen, gefolgt von einer Dehydratisierung in einem Lösungsmittelrückgewinnungs-/Dehydratisierungsturm (h), um rohe Methacrylsäure als Sumpfprodukt zu erhalten.
Das recycelte organische Lösungsmittel wird in den Extraktionsschritt zurückgeführt, während das wässrige Kopfprodukt mit dem Extraktionsraffinat kombiniert und vor der Abwasserbehandlung zum Lösungsmittelstrippen (g) geschickt wird.
Die trockene, rohe Methacrylsäure kann entweder weiter gereinigt oder direkt einem Veresterungsreaktor (i) mit Methanol und Katalysator zur Umwandlung in Methylmethacrylat zugeführt werden.
Mehrere Unternehmen, darunter Nippon Shokubai, Mitsubishi Rayon, Mitsui Toatsu, Kyowa Gas, Nippon Kayaku, Rohm and Haas und Oxirane, haben in die Forschung, Entwicklung und Kommerzialisierung dieses Prozesses investiert.
4.3. Herstellung von Methacrylsäure aus Isobuttersäure
Eine alternative Methode zur Herstellung von Methacrylsäure ist die säurekatalysierte Carbonylierung von Propen zu Isobuttersäure mit anschließender oxidativer Dehydrierung. Im Gegensatz zum Acetoncyanhydrin-Verfahren wird bei diesem Verfahren Propen als Ausgangsstoff verwendet.
Obwohl es noch nicht kommerziell einsatzfähig ist, erforschen mehrere große Methylmethacrylat-Hersteller aktiv sein Kommerzialisierungspotenzial.
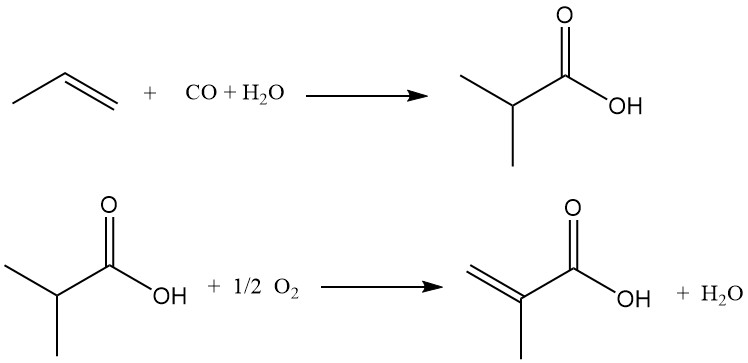
Im ersten Schritt werden Propen, Kohlenmonoxid und Wasser in Gegenwart eines stark sauren Katalysators (Schwefelsäure, Fluorwasserstoff oder Borfluorid) zur Reaktion gebracht, um Isobuttersäure zu erzeugen. Die kontrollierte Wasserzugabe während der Carbonylierung ermöglicht die direkte Synthese von Isobuttersäure.
Fluorwasserstoff kann in diesem Prozess sowohl als Lösungsmittel als auch als Katalysator fungieren. Die Reaktion verlief von 30 °C bei 20 MPa bis 120 °C bei 14 MPa, mit einem leichten Wassermangel im Vergleich zu Propen. Im Anschluss an die Reaktion wird der Produktstrom einer stufenweisen Flash-Trennung unterzogen:
- Stufe 1: Gewinnt überschüssiges Kohlenmonoxid zum Recycling zurück.
- Stufe 2: Entfernt Inertgase und jeglichen Fluorwasserstoff oder Isopropylfluorid durch Waschen mit einer Natronlauge.
Der größte Teil des Fluorwasserstoffs wird dann abgetrennt und recycelt, wobei alle verbleibenden fluorhaltigen Materialien im Bodenstrom hydrolysiert und der freigesetzte Fluorwasserstoff recycelt werden.
Ein abschließender Destillationsschritt reinigt die Isobuttersäure für die nächste Stufe. Im Destillationssumpf sind Nebenprodukte aus mehreren Propenkondensationen vor der Carbonylierung vorhanden, die gesamte Propenselektivität soll jedoch 95–97 % betragen.
In der zweiten Stufe werden Isobuttersäure, Wasserdampf und Luft in einem Rohrbündelreaktor über einen Festbettkatalysator geleitet und dort oxidativ zu Methacrylsäure dehydriert.
Der Reaktorausfluss wird gequencht, um einen wässrigen Methacrylsäurestrom zu erhalten. Dieses Rohprodukt enthält Nebenprodukte wie Aceton und Essigsäure sowie Kohlenmonoxid, Kohlendioxid und nicht kondensierbare Gase, die verbrannt werden.
Methacrylsäure wird durch Lösungsmittelextraktion und Dehydratisierung sowie anschließende Destillation isoliert. Isobutter- und Essigsäure werden dann vor der abschließenden Methacrylsäuredestillation als Vorlauf abgetrennt. Die Trennung von Isobuttersäure und Methacrylsäure ist aufgrund der nahe beieinander liegenden Siedepunkte der beiden Säuren eine Herausforderung.
Für die Dehydrierung von Isobuttersäure zu Methacrylsäure werden hauptsächlich zwei Arten von Katalysatoren verwendet:
- Mo-P-V-Mischoxidkatalysatoren, entwickelt von Mitsubishi Chemical Industries, R€ohm und anderen. Diese Phosphomolybdänsäurederivate erzielen häufig Umsätze von 99,8 % mit Selektivitäten von über 74 %.
- Eisenphosphatkatalysatoren von Ashland Oil. Diese Katalysatoren bieten Selektivitäten von 84–85 % bei Umsätzen von 85–95 %, erfordern jedoch im Vergleich zu Phosphomolybdatkatalysatoren einen Betrieb bei höheren Temperaturen (400 °C).
4.4. Herstellung von Methacrylsäure aus Ethylen
Über die zuvor beschriebenen vorherrschenden Prozesse hinaus gibt es andere alternative Methoden zur Methacrylsäureproduktion. Methacrylsäure kann durch Kondensation von Formaldehyd mit Propionsäure oder durch Kondensation von Formaldehyd mit Propanal zu Methacrolein hergestellt werden, das dann zu Methacrylsäure oxidiert wird.
BASF hat ein Verfahren kommerzialisiert, das auf der Kondensation von Formaldehyd mit Propanal basiert und dabei Ethylen, Synthesegas und Formaldehyd als Ausgangsstoffe verwendet. Ihr seit 1990 in Betrieb befindliches Werk verfügt über eine Produktionskapazität von 40.000 Tonnen pro Jahr.
Im BASF-Verfahren wird Ethylen zu Propanal hydroformyliert, das mit Formaldehyd zu Methacrolein kondensiert. Methacrolein wird an der Luft katalytisch zu Methacrylsäure oxidiert.
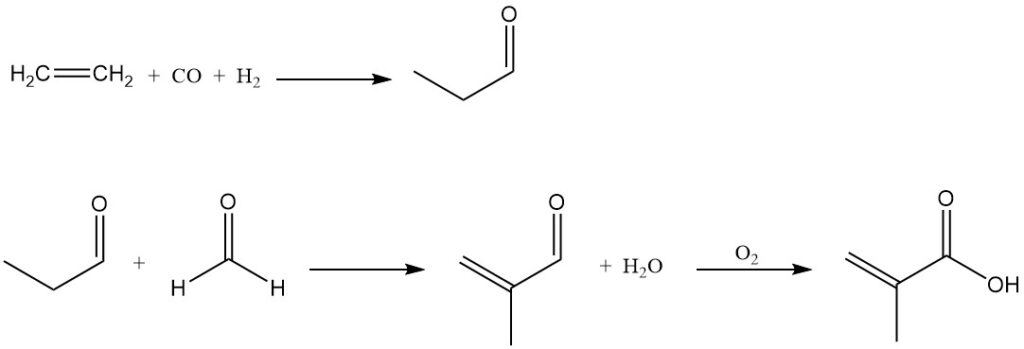
Es wird ein alternatives Verfahren vorgeschlagen, bei dem Propanal zu Propionsäure oxidiert und anschließend mit Formaldehyd kondensiert wird, um direkt Methacrylsäure herzustellen.
5. Verwendung von Methacrylsäure
Methacrylsäure wird zur Herstellung einer Vielzahl von Polymeren, einschließlich Methacrylaten, und zur Herstellung ihrer Ester verwendet. Diese Polymere liefern wasserklare, robuste Kunststoffe, die in Plattenform für Verglasungen, Schilder, Displays und Beleuchtungsplatten verwendet werden.
Durch Formen von Polymerpellets können Automobilbeleuchtungslinsen und ähnliche Produkte hergestellt werden.
Höhere Methacrylatpolymere werden bei der Herstellung von Öladditiven, lösungsmittelfreien Tinten und Beschichtungen sowie Bindemitteln für die Xerografie verwendet.
Methacrylsäure wird in Farben, Klebstoffen, Lederbehandlungsmitteln und als Rohstoff bei der Herstellung von Ionenaustauscherharzen verwendet.
Salze der Poly(methacrylsäure) werden als Zusatzstoffe in Waschmitteln und als wasserlösliche Verdickungsmittel verwendet.
6. Toxikologie von Methacrylsäure
Basierend auf oralen und dermalen Expositionsstudien an Ratten und Kaninchen wird Methacrylsäure als leicht bis mäßig gefährlich eingestuft.
Schleimhäute reagieren sehr empfindlich auf Methacrylsäure. Die Exposition kann zu leichten bis ätzenden Reizungen führen und möglicherweise zu dauerhaften Augenschäden oder Blindheit führen. Bei der Handhabung ist ein vollständiger Augenschutz erforderlich.
Direkter Kontakt kann leichte bis schwere Hautrötungen und Reizungen verursachen, einschließlich möglicher Korrosion. Methacrylsäure ist ätzender als ihre Ester. Handschuhe und Schutzkleidung sind erforderlich.
Übermäßiger Kontakt mit Methacrylsäuredämpfen kann die Nase und den Rachen reizen und zu Schwindel, Schläfrigkeit oder einer Depression des Zentralnervensystems führen.
Das Verschlucken von Methacrylsäure kann Mund, Rachen, Speiseröhre und Magen stark reizen und zu Unwohlsein, Erbrechen, Durchfall, Schwindel und möglicherweise zum Kollaps führen.
Wiederholter Hautkontakt kann zu allergischer Dermatitis (Hautausschlag, Juckreiz und Schwellung) führen. Einzelpersonen können nach der Exposition eine Empfindlichkeit entwickeln, die zu Reaktionen bei späterer Exposition gegenüber demselben oder anderen Acrylmonomeren führen kann.
Studien an Tieren, die extrem hohen Dampfkonzentrationen von Methacrylsäure ausgesetzt waren, zeigten Entzündungen der Atemwege und degenerative Veränderungen in Organen (Leber, Nieren und Herz), die weit über den Reizschwellenwerten lagen. Beim Menschen wurden keine derartigen Wirkungen berichtet.
Verweise
- Methacrylic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_441.pub2
- https://www.m-chemical.co.jp/en/products/departments/mcc/mma_pmma/product/1201254_9386.html
- https://www.basf.com/global/documents/en/products-and-industries/acrylic-monomers/technical-information/TI_CP_1574_e_Methacrylic_acid_technical_190419_SCREEN_02.pdf
