Ácido Metacrílico: Propiedades, Producción y Usos
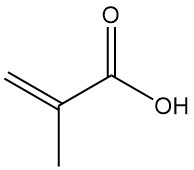
El ácido metacrílico, también conocido como ácido α-metilacrílico o ácido 2-metilpropenoico, es un ácido orgánico con la fórmula CH2=C(CH3)COOH. Es un líquido corrosivo, incoloro, moderadamente volátil y de olor fuertemente acre.
El ácido metacrílico se produjo por primera vez en 1865 a partir de metacrilato de etilo, que se preparaba mediante deshidratación de α-hidroxiisobutirato de etilo.
Tabla de contenido
1. Historia del Ácido Metacrílico y los metacrilatos
La exploración científica de los acrilatos y metacrilatos para aplicaciones comerciales comenzó con la tesis doctoral de OTTO ROEHΜ en 1901. Investigó los productos de polimerización de derivados del ácido acrílico y previó su potencial uso industrial.
Roehml informó sobre la síntesis de materiales gomosos transparentes, pero en ese momento carecía de métodos de producción eficientes. En 1907, se asoció con OTTO HAAS para establecer una empresa centrada en enzimas para el tratamiento del cuero.
En la década de 1920 se produjeron avances significativos en la producción comercial de acrilatos y metacrilatos. Después de la Primera Guerra Mundial, Roehml desarrolló un proceso para la producción de acrilato a gran escala utilizando cianhidrina de etileno, un intermedio derivado de la clorhidrina de etileno.
Posteriormente, colaboró con Walter Bauer para establecer un proceso similar para metacrilato de metilo utilizando acetonacianhidrina. En 1931, Bauer había producido con éxito un polímero de metacrilato de metilo transparente que se ablandaba por encima de los 100 °C.
La década de 1930 fue testigo de una intensa investigación sobre la fabricación de láminas fundidas a partir de metacrilato de metilo por parte de Rohm and Haas y Du Pont (EE. UU.), Rohm and Haas AG (Alemania) e ICI (Inglaterra).
La primera producción comercial de monómero de metacrilato de metilo comenzó en Darmstadt, Alemania (1933), mediante la ruta de la cianhidrina de acetona, que implicaba convertir la cianhidrina en α-hidroxiisobutirato de etilo, seguido de una deshidratación usando P2O5.
ICI obtuvo una patente en 1934 para un método alternativo que transformaba la acetonacianhidrina en sulfato de metacrilamida utilizando ácido sulfúrico concentrado. El ácido metacrílico, obtenido hidrolizando sulfato de metacrilamida, podría luego esterificarse para formar metacrilato de metilo.
Al reconocer la eficiencia del proceso ICI, Rohm y Haas AG firmaron un acuerdo de licencia cruzada para la producción de láminas acrílicas fundidas. Posteriormente, tanto ICI como Rohm and Haas AG iniciaron la producción comercial de metacrilato de metilo utilizando la ruta del sulfato de metacrilamida en 1937.
Rohm and Haas en Estados Unidos, entonces una empresa independiente desde 1917, continuó utilizando el proceso original durante varios años debido a limitaciones de la licencia.
La ruta del sulfato de metacrilamida siguió siendo el principal proceso comercial para la producción de metacrilato de metilo y ácido metacrílico hasta la introducción de los procesos de oxidación de isobuteno en 1983. Estos procesos fueron desarrollados de forma independiente en Japón por Japan Catalytic Chemical y Mitsubishi Rayon.
Si bien en Japón se planea aumentar la capacidad de ácido metacrílico a base de isobuteno y BASF está construyendo una nueva instalación a base de etileno, la ruta de la cianhidrina de acetona todavía se utiliza para una parte importante de la demanda mundial de metacrilato de metilo.
Las operaciones basadas en acetona-cianhidrina producen principalmente metacrilato de metilo, el derivado de metacrilato más importante. El ácido metacrílico producido por otras rutas también se utiliza como intermediario para la síntesis de metacrilato de metilo.
Cantidades más pequeñas de otros metacrilatos, incluido el metacrilato de etilo, el metacrilato de n-butilo, el metacrilato de isobutilo y homólogos superiores como el metacrilato de laurilo y el metacrilato de estearilo, se fabrican mediante esterificación directa del ácido metacrílico o transesterificación del metacrilato de metilo.
Además, están disponibles comercialmente monómeros especiales como metacrilato de 2-hidroxietilo, metacrilato de 2-hidroxipropilo, metacrilatos de aminoalquilo (por ejemplo, metacrilato de 2-dimetilaminoetilo) y metacrilamida. El sulfato de metacrilamida intermedio es el precursor para la producción de metacrilamida.
2. Propiedades físicas del ácido metacrílico
El ácido metacrílico es un ácido orgánico débil con un pKa de 4,65. Es un líquido transparente, incoloro o cristales incoloros con un olor acre y repulsivo. Es soluble en cloroformo y miscible con agua, etanol y éter.
Las propiedades físicas más importantes del ácido metacrílico se enumeran en la Tabla 1.
| Propiedad | Valor |
|---|---|
| Peso molecular | 86,09 g/mol |
| Punto de fusión, °C | 15.8 |
| Punto de ebullición (101,3 kPa), °C | 162 |
| Densidad, g/cm3 | 1.015 |
| Índice de refracción | 1,4288 |
| Presión de vapor, kPa |
a 20 °C: 0,09 a 60 °C: 1,33 |
| Viscosidad (24 °C), mPa·s | 1,38 |
| Solubilidad en agua | Miscible |
| Temperatura crítica, °C | 370 |
| Presión crítica, Pa | 4,70 |
| Volumen crítico, cm3/mol | 270 |
| Calor de vaporización (101,3 kPa), kJ/mol | 0,418 |
| Capacidad calorífica específica, J g-1 K-1 | 2.1 |
| Punto de inflamación, °C |
Copa abierta: 77 Copa cerrada: 67 |
| Temperatura de autoignición, °C | 400 |
3. Reacciones químicas del ácido metacrílico
El ácido metacrílico es muy reactivo y muestra reacciones típicas tanto del alqueno como del ácido carboxílico.
El efecto aceptor de electrones del ácido carboxílico polariza el doble enlace y aumenta su reactividad, pero esta reactividad es menos pronunciada que en el ácido acrílico debido al grupo metilo donador de electrones.
Como resultado, las adiciones nucleofílicas de Michael y tipo Michael al doble enlace sólo tienen lugar con reactivos ricos en electrones.
3.1. Adición al doble enlace carbono-carbono
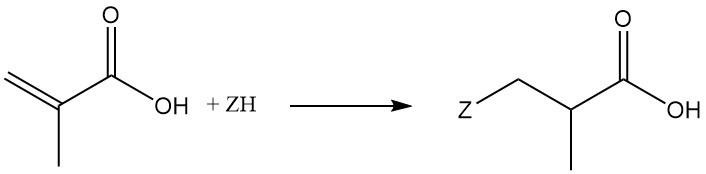
El ácido metacrílico reacciona con cianuro de hidrógeno, haluros de hidrógeno, sulfuro de hidrógeno, mercaptanos, alquilaminas, alcoholes, fenoles o fosfinas para producir propionatos de α-metilo β-sustituidos.
3.2. Reacciones de Diels-Alder
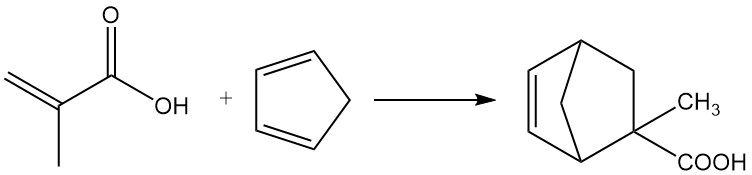
El ácido metacrílico sufre reacciones de Diels-Alder con dienos como el butadieno y el ciclopentadieno.
3.3. Reacciones de la función del ácido carboxílico
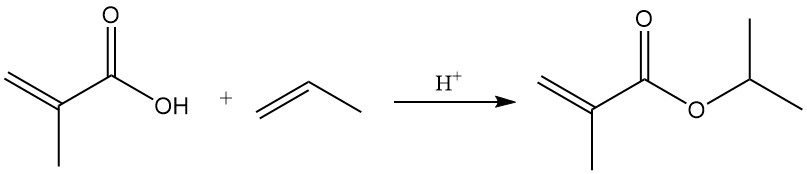
Los ésteres del ácido metacrílico se forman mediante reacciones con alcoholes en presencia de cantidades catalíticas de ácidos sulfúricos o sulfónicos. La adición de olefinas catalizada por ácido también produce ésteres.
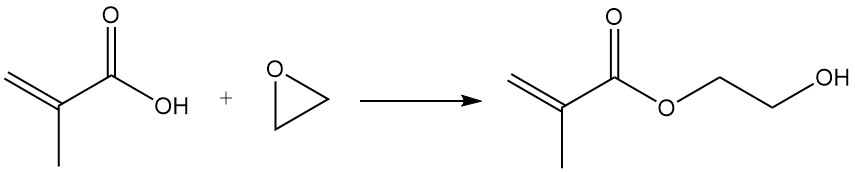
La reacción del grupo ácido metacrílico con epóxidos en presencia de catalizadores como resinas de intercambio aniónico, cloruro férrico o sales de litio produce metacrilatos de hidroxietilo e hidroxipropilo.
El cloruro de metacriloilo se sintetiza mediante la reacción del ácido metacrílico con cloruro de tionilo o tricloruro de fósforo.
El ácido metacrílico reacciona con el anhídrido acético para producir anhídrido metacrílico.
3.4. Polimerización
Los polímeros de ácido metacrílico y sus derivados se forman fácilmente al calentarlos en presencia de iniciadores de radicales libres como peróxidos, luz ultravioleta o radiación ionizante.
Los inhibidores fenólicos comunes se dirigen a los radicales peroxi y no inhiben el proceso de polimerización iniciado. Sin embargo, la exclusión de oxígeno es crítica durante la polimerización para evitar la conversión de radicales alquilo en radicales hidroperoxi.
4. Producción industrial de ácido metacrílico
Esta sección se centra en métodos comercialmente viables para producir ácido metacrílico. Para estos procesos se utilizan diferentes materias primas, categorizadas por la longitud de su cadena de carbono: etileno (ruta C2), propeno o acetona (ruta C3) e isobuteno (ruta C4).
La viabilidad económica de cada proceso depende de la disponibilidad regional y el precio de las materias primas. Actualmente, ninguna alternativa supera la ruta establecida de la cianhidrina de acetona en términos económicos, lo que justifica la operación continua de las plantas existentes basadas en cianhidrina.
4.1. Producción de ácido metacrílico por ruta de cianohidrina de acetona
El método más común para la síntesis de ácido metacrílico implica la hidrólisis del sulfato de metacrilamida, derivado de la acetonacianhidrina.
La cianhidrina de acetona se forma haciendo reaccionar acetona seca con cianuro de hidrógeno en presencia de un catalizador básico. Este intermedio luego reacciona con un exceso de ácido sulfúrico concentrado para producir sulfato de metacrilamida.
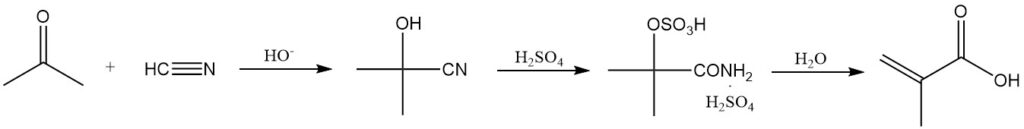
El ácido sulfúrico tiene un doble propósito: como reactivo y como disolvente de reacción. Una cantidad insuficiente de ácido sulfúrico da como resultado una mezcla de reacción difícil de manejar. Tanto el ácido como la acetona cianhidrina deben ser anhidros para minimizar la formación de subproductos.
La reacción inicial, llevada a cabo en una serie de reactores de tanque agitado, requiere una buena transferencia de calor para gestionar el proceso exotérmico. Una mezcla completa es crucial para evitar la descomposición de la cianhidrina en sus materiales de partida, que pueden formar subproductos no deseados.
Después de la reacción inicial (80–110 °C), la mezcla se somete a un breve craqueo térmico (125–160 °C) para convertir la mayor parte del subproducto de a-hidroxiisobutiramida en el sulfato de metacrilamida deseado, junto con algo de acetona, monóxido de carbono y agua. .
La segunda etapa implica hidrolizar la corriente de sulfato de metacrilamida con exceso de agua para producir ácido metacrílico y bisulfato de amonio, o tratarla con metanol acuoso en una etapa combinada de hidrólisis-esterificación para producir una mezcla de metacrilato de metilo y ácido metacrílico.
El rendimiento general basado en acetonacianhidrina suele estar dentro del rango del 80 al 90%.
Para la producción de ácido metacrílico, la hidrólisis da como resultado una mezcla de dos fases que permite la purificación separada del ácido metacrílico de la capa orgánica superior y el ácido metacrílico acuoso diluido de la capa inferior mediante destilación y extracción con vapor, respectivamente.
El deseo de eliminar la regeneración de ácido sulfúrico y los peligros asociados al transporte de cianuro de hidrógeno son factores clave para explorar métodos de producción alternativos.
Sin embargo, la ruta establecida de la acetonacianhidrina se beneficia de la ventaja económica de utilizar acetona (un subproducto de la producción de fenol) y cianuro de hidrógeno (un subproducto de la producción de acrilonitrilo) como materias primas.
4.2. Producción de ácido metacrílico a partir de isobuteno.
En los últimos años, empresas como Nihon Methacryl Monomer (una empresa conjunta de Sumitomo y Nippon Shokubai) y Mitsubishi Rayon han desarrollado un proceso de oxidación catalítica de dos etapas para producir ácido metacrílico a partir de isobuteno o terc-butanol.
El proceso implica la oxidación del isobuteno a metacroleína, que luego se oxida aún más a ácido metacrílico.
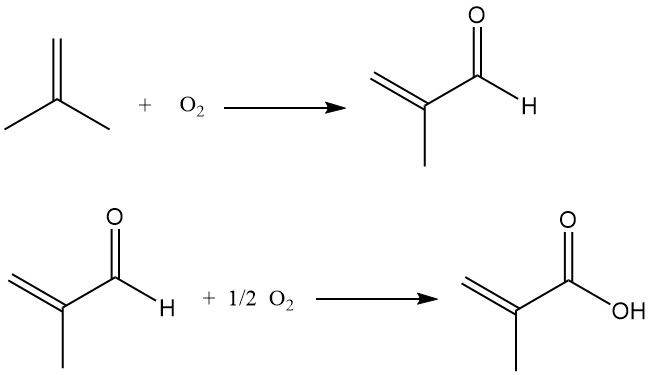
Los informes publicados comparan este proceso para la producción de ácido metacrílico a partir de isobuteno con un proceso similar para la producción de ácido acrílico a partir de propeno. El desafío clave radica en mantener una alta selectividad del catalizador durante la segunda etapa de oxidación, que normalmente funciona mejor con tasas de conversión moderadas (65-85%).
El proceso Sumitomo-Nippon Shokubai (Figura 1) supera este desafío operando el reactor de primera etapa con alta conversión y alimentando directamente su efluente al segundo reactor de oxidación. La segunda etapa opera a una tasa de conversión más baja para optimizar la selectividad y la vida útil del catalizador.
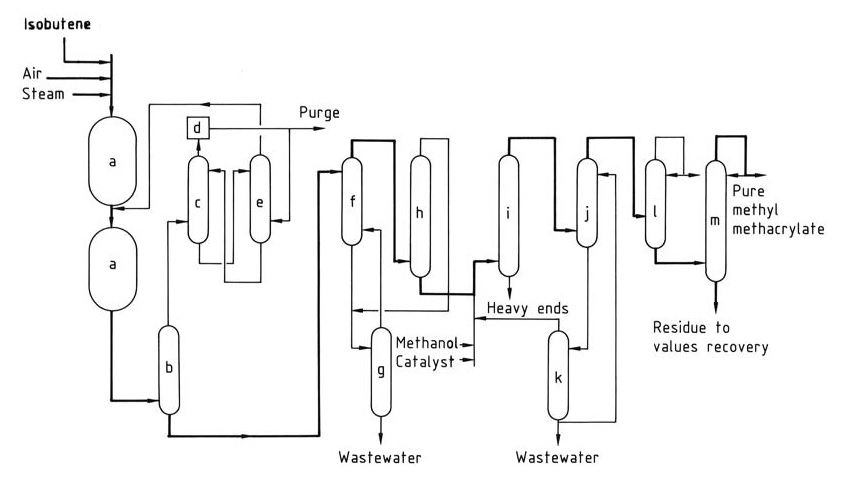
a) Reactores de oxidación; b) extintor; c) Absorbedor; d) Unidad de combustión; e) Torre de recuperación de metacroleína; f) Unidad de extracción por solvente; g) Torre de extracción de solventes; h) Torre de recuperación/deshidratación de disolventes; i) reactor de esterificación; j) extractor; k) Unidad de destilación; l) Decapante de puntas ligeras; m) Columna de destilación del producto.
A continuación, la metacroleína que no ha reaccionado de la segunda etapa se separa y se recicla, consiguiendo un rendimiento global de ácido metacrílico a partir de isobuteno de alrededor del 65-70 %.
Los catalizadores en la primera oxidación suelen ser óxidos metálicos multicomponente que contienen bismuto, molibdeno y otros metales para mejorar la actividad y controlar la selectividad. Para la segunda oxidación se utilizan catalizadores a base de ácido fosfomolíbdico. También pueden estar presentes elementos adicionales como cobre y vanadio.
El efluente del reactor de oxidación de la segunda etapa se enfría (b) para obtener ácido metacrílico acuoso bruto. La corriente gaseosa restante se hace pasar a través de un absorbente (c), donde se absorbe la metacroleína que no ha reaccionado (usualmente usando ácido carboxílico acuoso).
Los gases de escape del absorbente se incineran (d) antes de su liberación. Una parte de los gases incinerados se puede reciclar a la primera etapa como diluyente inerte. El absorbente cargado de metacroleína se transfiere a una torre de recuperación (e) para su reciclado de regreso al reactor de segunda etapa. La solución absorbente recuperada se devuelve al absorbente.
El ácido metacrílico en bruto se somete a extracción con disolvente (f) seguida de deshidratación en una torre de recuperación/deshidratación de disolvente (h) para producir ácido metacrílico en bruto como producto de cola.
El disolvente orgánico reciclado se devuelve a la etapa de extracción, mientras que la parte superior acuosa se combina con el refinado del extractor y se envía para extracción de disolvente (g) antes del tratamiento de aguas residuales.
El ácido metacrílico crudo seco puede purificarse adicionalmente o enviarse directamente a un reactor de esterificación (i) con metanol y catalizador para su conversión en metacrilato de metilo.
Varias empresas, incluidas Nippon Shokubai, Mitsubishi Rayon, Mitsui Toatsu, Kyowa Gas, Nippon Kayaku, Rohm and Haas y Oxirane, han invertido en la investigación, el desarrollo y la comercialización de este proceso.
4.3. Producción de ácido metacrílico a partir de ácido isobutírico
Un método alternativo para la producción de ácido metacrílico es la carbonilación catalizada por ácido de propeno a ácido isobutírico, seguida de deshidrogenación oxidativa. A diferencia del proceso de cianhidrina de acetona, este proceso utiliza propeno como material de partida.
Si bien aún no está comercialmente operativo, varios productores importantes de metacrilato de metilo están investigando activamente su potencial de comercialización.
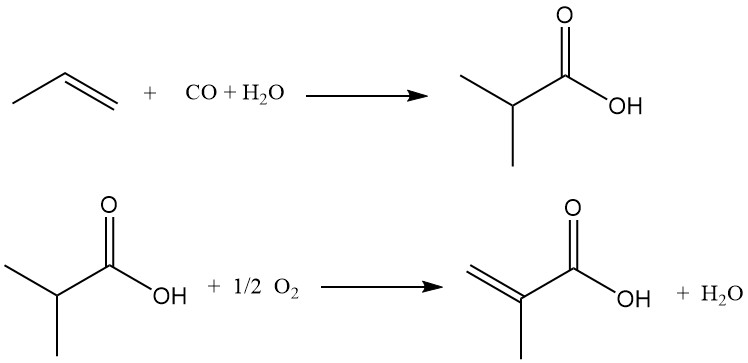
La primera etapa consiste en hacer reaccionar propeno, monóxido de carbono y agua en presencia de un catalizador ácido fuerte (ácido sulfúrico, fluoruro de hidrógeno o fluoruro de boro) para producir ácido isobutírico. La adición controlada de agua durante la carbonilación permite la síntesis directa de ácido isobutírico.
El fluoruro de hidrógeno puede actuar como disolvente y catalizador en este proceso. La reacción transcurrió desde 30 °C a 20 MPa hasta 120 °C a 14 MPa, con una ligera deficiencia de agua con respecto al propeno. Después de la reacción, la corriente de producto se somete a una separación instantánea por etapas:
- Etapa 1: Recupera el exceso de monóxido de carbono para reciclarlo.
- Etapa 2: elimina los gases inertes y cualquier fluoruro de hidrógeno o fluoruro de isopropilo mediante el lavado con una solución cáustica.
Luego, la mayor parte del fluoruro de hidrógeno se separa y se recicla, hidrolizándose cualquier material que contenga flúor restante en la corriente inferior y se recicla el fluoruro de hidrógeno liberado.
Un paso final de destilación purifica el ácido isobutírico para la siguiente etapa. Los subproductos de múltiples condensaciones de propeno antes de la carbonilación están presentes en los fondos de destilación, pero se informa que la selectividad general del propeno es del 95 al 97%.
En la segunda etapa, el ácido isobutírico, el vapor y el aire pasan sobre un catalizador de lecho fijo en un reactor multitubular, sometiéndose a una deshidrogenación oxidativa a ácido metacrílico.
El efluente del reactor se enfría rápidamente para obtener una corriente acuosa de ácido metacrílico. Este producto crudo contiene subproductos como acetona y ácido acético, junto con monóxido de carbono, dióxido de carbono y gases no condensables que se incineran.
El ácido metacrílico se aísla mediante extracción con disolventes y deshidratación, seguida de destilación. Luego se separan los ácidos isobutírico y acético como extremos ligeros antes de la destilación final del ácido metacrílico. Separar el ácido isobutírico del ácido metacrílico es un desafío debido a los puntos de ebullición cercanos de los dos ácidos.
Se utilizan dos tipos principales de catalizadores para la deshidrogenación del ácido isobutírico a ácido metacrílico:
- Catalizadores de óxido mixto Mo-P-V desarrollados por Mitsubishi Chemical Industries, R€ohm y otros. Estos derivados del ácido fosfomolíbdico a menudo alcanzan conversiones del 99,8 % con selectividades superiores al 74 %.
- Catalizadores de fosfato de hierro de Ashland Oil. Estos catalizadores ofrecen selectividades del 84 al 85 % con conversiones del 85 al 95 %, pero requieren operación a temperaturas más altas (400 °C) en comparación con los catalizadores de fosfomolibdato.
4.4. Producción de ácido metacrílico a partir de etileno
Más allá de los procesos dominantes descritos anteriormente, existen otros métodos alternativos para la producción de ácido metacrílico. El ácido metacrílico se puede preparar mediante la condensación de formaldehído con ácido propiónico o mediante la condensación de formaldehído con propanal para formar metacroleína, que luego se oxida a ácido metacrílico.
BASF ha comercializado un proceso basado en la condensación de formaldehído con propanal, utilizando etileno, gas de síntesis y formaldehído como materias primas. Su planta, operativa desde 1990, tiene una capacidad de producción de 40.000 toneladas métricas al año.
En el proceso BASF, el etileno se hidroformila a propanal, que se condensa con formaldehído para formar metacroleína. La metacroleína se oxida catalíticamente con el aire a ácido metacrílico.
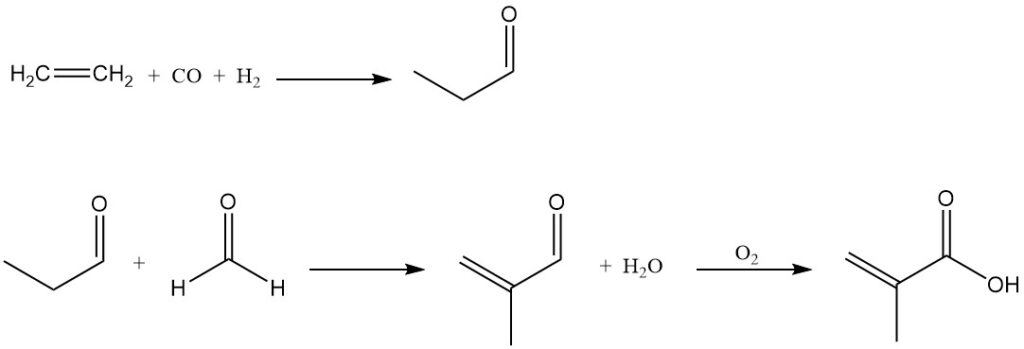
Se propone un proceso alternativo que implica la oxidación del propanal a ácido propiónico, seguida de su condensación con formaldehído para producir directamente ácido metacrílico.
5. Usos del ácido metacrílico
El ácido metacrílico se utiliza para preparar una amplia gama de polímeros, incluidos los metacrilatos, y para producir sus ésteres. Estos polímeros proporcionan plásticos resistentes, transparentes como el agua, que se utilizan en forma de láminas en acristalamientos, letreros, exhibidores y paneles de iluminación.
Moldeando gránulos de polímero se pueden preparar lentes de iluminación para automóviles y productos similares.
Los polímeros de metacrilato superior se utilizan en la fabricación de aditivos para aceites, tintas y recubrimientos sin disolventes y aglutinantes para xerografía.
El ácido metacrílico se utiliza en pinturas, adhesivos, agentes para el tratamiento del cuero y como materia prima en la fabricación de resinas de intercambio iónico.
Las sales de poli(ácido metacrílico) se utilizan como aditivos en detergentes y como espesantes solubles en agua.
6. Toxicología del ácido metacrílico
El ácido metacrílico se considera de leve a moderadamente peligroso según estudios de exposición oral y dérmica en ratas y conejos.
Las membranas mucosas son muy sensibles al ácido metacrílico. La exposición puede causar irritación que va desde leve hasta corrosiva, lo que podría provocar daños oculares permanentes o ceguera. Es obligatoria la protección ocular completa durante la manipulación.
El contacto directo puede causar enrojecimiento e irritación de la piel, desde leves hasta graves, incluida la posible corrosión. El ácido metacrílico es más corrosivo que sus ésteres. Se requieren guantes y ropa protectora.
La sobreexposición a los vapores de ácido metacrílico puede irritar la nariz y la garganta y causar mareos, somnolencia o depresión del sistema nervioso central.
La ingestión de ácido metacrílico puede irritar gravemente la boca, la garganta, el esófago y el estómago, provocando malestar, vómitos, diarrea, mareos y posible colapso.
La exposición repetida de la piel puede provocar dermatitis alérgica (sarpullido, picazón e hinchazón). Las personas pueden desarrollar sensibilidad después de la exposición, lo que lleva a reacciones por exposiciones posteriores al mismo u otros monómeros acrílicos.
Los estudios en animales expuestos a concentraciones extremadamente altas de vapor de ácido metacrílico han demostrado inflamación del tracto respiratorio y cambios degenerativos en órganos (hígado, riñones y corazón) a niveles que superan con creces los umbrales de irritación. No se han informado tales efectos en humanos.
Referencias
- Methacrylic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_441.pub2
- https://www.m-chemical.co.jp/en/products/departments/mcc/mma_pmma/product/1201254_9386.html
- https://www.basf.com/global/documents/en/products-and-industries/acrylic-monomers/technical-information/TI_CP_1574_e_Methacrylic_acid_technical_190419_SCREEN_02.pdf
