Butadieno: Propiedades, Producción y Usos
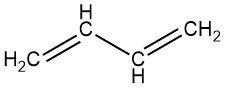
El 1,3-butadieno es un gas incoloro con olor a gasolina. Es el miembro más simple de la serie de dienos conjugados, que contienen la estructura C=C-C=C, siendo el C carbono.
Butadieno normalmente se refiere al 1,3-butadieno (106-99-0), un hidrocarburo C4 insaturado muy significativo. Su homólogo termodinámicamente menos estable, el 1,2-butadieno (590-19-2), tiene una relevancia industrial insignificante.
1,3-Butadieno: CH2=CH–CH=CH2
1,2-Butadieno: CH2=C=CH–CH3
El butadieno se destaca como un petroquímico crucial, con una producción global que supera los 10 millones de toneladas al año.
Tabla de contenido
1. Propiedades físicas del butadieno
El butadieno es un gas incoloro en condiciones normales. Algunas propiedades físicas se resumen en la siguiente tabla:
| Propiedad | Valor |
|---|---|
| Punto de ebullición a 101,3 kPa | -4,4 °C |
| Punto de fusión a 101,3 kPa | -108,9 °C |
| Temperatura crítica | 425 000 |
| Presión crítica | 4,32 MPa |
| Volumen molar crítico | 221 cm³/mol |
| Densidad (líquido, 0 °C) | 0,646 g/cm³ |
| Densidad (líquido, 25 °C) | 0,616 g/cm³ |
| Densidad (líquido, 50 °C) | 0,582 g/cm³ |
| Densidad del gas (relativa al aire) | 1,87 |
| Presión de vapor (-4,4°C) | 101,3 kPa |
| Presión de vapor (0 °C) | 120,0 kPa |
| Presión de vapor (25 °C) | 273,6 kPa |
| Presión de vapor (50 °C) | 537,9kPa |
| Presión de vapor (75 °C) | 986,7 kPa |
| Presión de vapor (100 °C) | 1733kPa |
| Viscosidad (líquido, 0 °C) | 0,25 mPa·s |
| Viscosidad (líquido, 50 °C) | 0,20 mPa·s |
| Entalpía de vaporización (25 °C) | 20,86 kJ/mol |
| Entalpía de vaporización (-4,4 °C) | 22,47 kJ/mol |
| Entalpía de formación (gaseosa, 298 K, 101,3 kPa) | 110,0 kJ/mol |
| Entalpía libre de formación (gaseosa, 298 K, 101,3 kPa) | 151,5 kJ/mol |
| Entalpía de combustión (gaseosa, 298 K, 101,3 kPa) | 2541,5 kJ/mol |
| Entalpía de hidrogenación a butano (gaseoso, 298 K, 101,3 kPa) | 235,7 kJ/mol |
| Entropía de formación (líquido, 298 K, 101,3 kPa) | 199,0 J·mol⁻¹·K⁻¹ |
| Entalpía de fusión (164,2 K, 101,3 kPa) | 7,988 kJ/mol |
El butadieno tiene una solubilidad limitada en agua. Es soluble en metanol y etanol y muy soluble en disolventes polares de alto punto de ebullición como la metilpirrolidona.
Varias propiedades técnicas son cruciales para el manejo seguro del butadieno. Éstas incluyen:
- Punto de inflamación: -85 °C
- Temperatura de ignición: 415 °C
El butadieno no estabilizado o insuficientemente estabilizado puede reaccionar con el oxígeno del aire formando peróxidos explosivos.
2. Propiedades químicas del butadieno
El butadieno, que posee dos dobles enlaces conjugados, participa en diversas reacciones, incluidas las adiciones 1,2 y 1,4 consigo mismo (polimerización) y otros reactivos, la dimerización lineal, la trimerización y la formación de anillos.
Polimerización:
La reacción más importante del butadieno implica la polimerización mediante adición 1,2 y 1,4, lo que da lugar a una variedad de polímeros. La naturaleza de estos polímeros depende de los métodos de preparación y del sistema catalítico empleado, lo que da como resultado cauchos sintéticos y resinas poliméricas de importancia industrial.
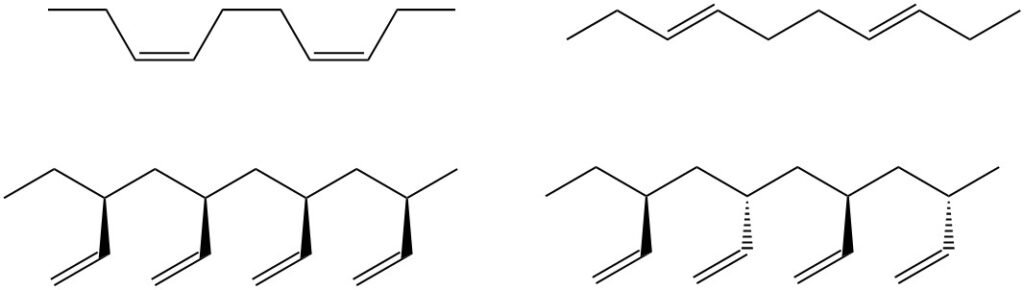
Otras reacciones de adición:
El butadieno se somete a una adición 1,2 o 1,4 con varios reactivos, dependiendo las proporciones de los productos de adición de las condiciones de reacción. Estos productos de adición sirven como intermediarios cruciales en la producción de sustancias como el cloropreno y la hexametilendiamina.
Reacciones específicas:
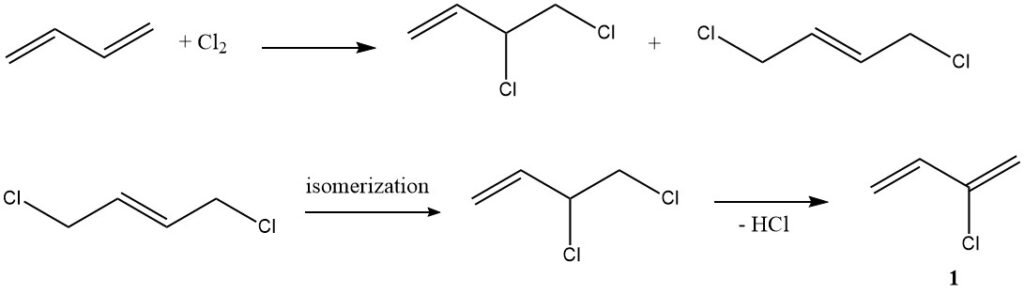
1. Cloración (producción de cloropreno): en un ejemplo típico de adición electrófila, el butadieno reacciona con el cloro para producir cloropreno (1), un compuesto con múltiples aplicaciones industriales.
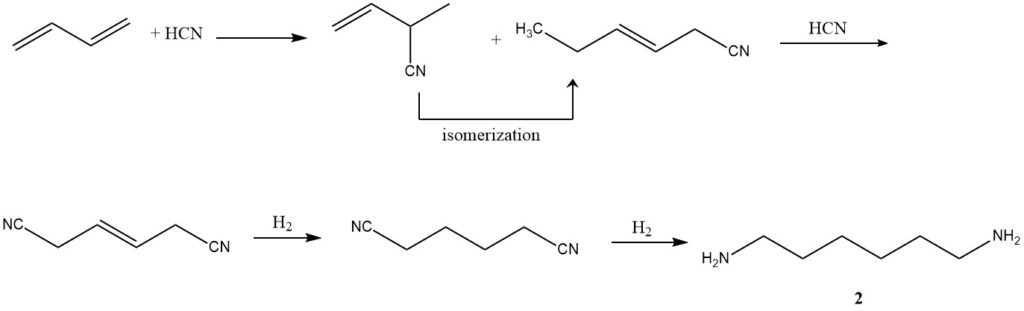
2. Hidrocianación (producción de adiponitrilo): empleando un proceso de tres pasos desarrollado por Du Pont, el butadieno se somete a hidrocianación para formar una mezcla de pentenonitrilos isoméricos lineales y ramificados. La isomerización posterior y la hidrocianación adicional dan como resultado el adiponitrilo (2).
3. Carboalcoxilación (producción de ε-caprolactama): DSM y Du Pont han explorado un proceso alternativo para la producción de ε-caprolactama a partir de butadieno. Este proceso de varios pasos implica carboalcoxilación, hidroformilación y aminación reductora. Aunque todavía no se ha implementado a escala industrial, presenta una vía prometedora para el desarrollo futuro.
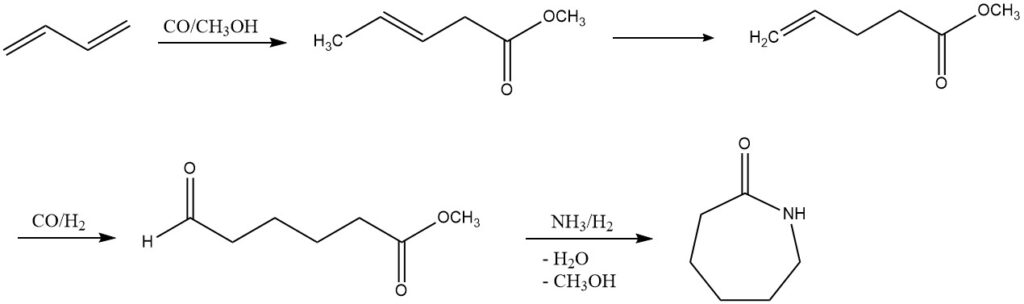
4. Acetoxilación (producción de 1,4-butanodiol o tetrahidrofurano): mediante la acetoxilación, el butadieno conduce a la síntesis de 1,4-diacetoxi-2-buteno, que, en un proceso Mitsubishi de varios pasos, se convierte en 1,4- butanodiol o tetrahidrofurano. Estos procesos, bajo la influencia de catalizadores específicos, muestran el potencial de diversas transformaciones químicas.
5. Otras reacciones de oxidación: Los procesos innovadores, como el proceso Toyo Soda y la oxidación directa con aire u oxígeno, representan métodos económicos para la producción de diversos derivados C4. La introducción de 3,4-epoxi-1-buteno mediante oxidación abre vías para la creación de valiosos intermediarios químicos.
6. Reacción de Diels-Alder: Una de las reacciones más conocidas del butadieno, la reacción de Diels-Alder, juega un papel crucial en los procesos industriales para la producción de estireno. La dimerización del butadieno y su posterior conversión en estireno resalta la versatilidad de esta reacción en la síntesis de valiosos compuestos químicos.
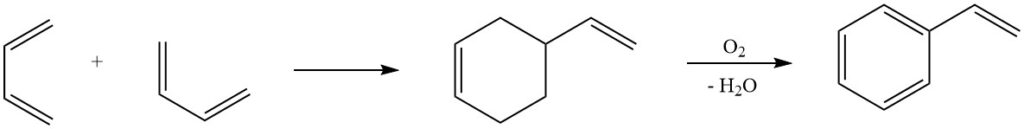
7. Ciclodimerización, ciclotrimerización: dos moléculas de butadieno pueden someterse a ciclodimerización para producir 1,5-ciclooctadieno, mientras que tres moléculas dan como resultado 1,5,9-ciclododecatrieno. Estos compuestos cíclicos, facilitados por catalizadores específicos, sirven como intermediarios en la producción de poliamidas superiores.
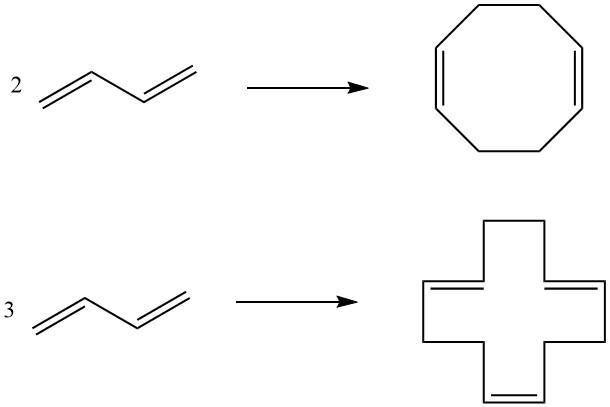
8. 1,4-Cicloadición: La 1,4-adición reversible de butadieno con dióxido de azufre conduce a la formación de la sulfona cíclica 2,5-dihidrotiofeno-1,1-dióxido, que luego se convierte en sulfolano. Este proceso muestra la adaptabilidad del butadieno en la síntesis de disolventes altamente polares.
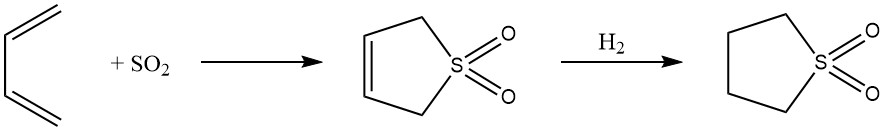
9. Dimerización y Trimerización Lineal; Telomerización: bajo la influencia de catalizadores de Ni, Co, Pd o Fe, el butadieno sufre una dimerización o trimerización lineal. Los oligómeros lineales resultantes, separados por la longitud de la cadena, ofrecen diversos compuestos, como el 1,3,7-octatrieno.
La reacción de telomerización es la di y oligomerización de un 1,3-dieno mediante la adición de un compuesto nucleofílico. Está catalizado por Pd, Ni o Pt y produce un amplio espectro de productos según el nucleófilo utilizado.
10. Hidrogenación: la hidrogenación selectiva de butadieno genera 1-buteno o 2-buteno, y el ajuste cuidadoso de las condiciones de reacción garantiza una conversión suficiente sin sobrehidrogenación a n-butano. Los procesos comerciales de empresas como Axens, UOP y Lummus proporcionan enfoques personalizados para maximizar el rendimiento de isómeros de buteno específicos.
11. Formación de complejos: el butadieno forma complejos con diversos compuestos metálicos, como las sales de Cu(I). Si bien históricamente se han utilizado en la extracción de butadieno, las técnicas modernas de destilación extractiva han reemplazado en gran medida a este método.
Los complejos con otros metales de transición como Fe, Ni, Co, Pd y Pt están bien establecidos, lo que contribuye a los estudios mecanicistas en la catálisis de polimerización de alfa-olefinas.
3. Producción de butadieno
Históricamente, existieron diversos métodos para la producción de butadieno. Hoy en día, quedan cuatro caminos principales:
- Craqueo de nafta: esta ruta dominante captura el butadieno como subproducto de la producción de etileno.
- Deshidrogenación de butano/buteno: este proceso desempeña un papel menor, basado en campañas, dependiendo de los precios de la materia prima y del butadieno.
- Producción de etanol: Este método ha perdido importancia.
- Producción de acetileno: Esta ruta ya no es comercialmente viable.
Se están explorando nuevos enfoques de base biológica.
La economía de la producción de butadieno está fuertemente influenciada por la producción conjunta de etileno y propileno. Cuando estas olefinas C2 y C3 son económicas, la producción específica de butadieno a partir de butenos y butano se vuelve más atractiva.
3.1. Producción a partir de acetileno
Históricamente, se emplearon dos vías para producir butadieno a partir de acetileno. Ambos están ahora obsoletos debido a la naturaleza costosa y que requiere mucha energía de la producción de acetileno. Sólo los pasos iniciales del proceso Reppe, que conducen a 1,4-butanodiol y tetrahidrofurano, siguen siendo comercialmente relevantes.
3.2. Producción a partir de etanol
El proceso IPATJEW y OSTROMISLENSKY, modificado posteriormente por LEBEDEW, alguna vez sirvió como fuente clave de butadieno, especialmente en Alemania y Europa del Este durante la Segunda Guerra Mundial. Este proceso se ilustra con la reacción:
2 CH3CH2OH → CH2=CHCH=CH 2 + 2 H2O + H2
y operado a temperaturas que oscilan entre 370 y 450 °C usando MgO – SiO2 o SiO2 – Al2O3 catalizadores, alcanza selectividades de hasta el 70 %.
Aunque ya no es competitivo para la producción a gran escala, aún puede ser viable en regiones con etanol barato o excedentes de alcohol agrícola.
3.3. Deshidrogenación de Butano y Butenos
La deshidrogenación de butano y butenos para producir butadieno presenta desafíos únicos debido a su naturaleza endotérmica. Para maximizar el rendimiento y la selectividad, se deben abordar varias consideraciones clave:
Principio de Le Chatelier: Reducir la presión parcial de los productos deseados, butadieno e hidrógeno, impulsa la reacción. Esto se puede lograr mediante el funcionamiento al vacío o agregando vapor a la mezcla de reacción.
Beneficios de Steam:
- El vapor ayuda a mitigar la desactivación del catalizador al prevenir la formación de coque en la superficie del catalizador.
- La naturaleza endotérmica de la reacción de deshidrogenación requiere un aporte de calor externo. El vapor se condensa fácilmente, liberando una cantidad significativa de calor para impulsar la reacción.
- El vapor condensado se puede separar fácilmente del flujo del producto, lo que garantiza una contaminación mínima.
Si bien las temperaturas más altas favorecen la formación de butadieno, también aumentan el riesgo de reacciones secundarias indeseables como craqueo, isomerización y polimerización. Encontrar el equilibrio de temperatura óptimo entre rendimiento y selectividad es crucial.
Los compuestos susceptibles a las reacciones secundarias antes mencionadas se eliminan antes del proceso de deshidrogenación para minimizar su influencia.
Como la reacción de deshidrogenación no se completa, la corriente del producto requiere separación para aislar el butadieno. Los materiales de partida que no reaccionaron se reciclan nuevamente en el proceso para maximizar la eficiencia.
Controlando cuidadosamente estos aspectos, se puede optimizar la deshidrogenación de butano y butenos para una producción eficiente y selectiva de butadieno.
3.3.1. Deshidrogenación del n-butano
Existen dos métodos destacados para deshidrogenar n-butano en butadieno:
1. Proceso Houdry-Catadieno:
Este proceso establecido de un solo paso opera comercialmente desde 1943. Múltiples reactores de lecho compacto, dispuestos en paralelo, realizan ciclos entre las fases de reacción y regeneración. Un catalizador de óxido de aluminio que contiene un 20 % de óxido de cromo facilita la deshidrogenación del n-butano puro o su mezcla con n-butenos a 550-650 °C y 10-25 kPa.
Las altas temperaturas favorecen la producción de butadieno, pero también generan subproductos indeseables como hidrocarburos C1-C3, hidrógeno y coque que contamina el catalizador.
Después de cada ciclo de reacción (5-15 minutos), el reactor se regenera: al quemar el depósito de coque se libera calor, almacenado en el catalizador y el material inerte, para la siguiente fase de reacción.
Este proceso produce una concentración de butadieno del 15 al 18% a la salida del reactor. Los pasos de recuperación posteriores, que incluyen enfriamiento rápido, compresión, extracción y separación, aumentan la concentración de butadieno al 30-50%. De 1.000 toneladas de n-butano se obtienen aproximadamente 550 toneladas de butadieno. El butadieno puro se puede aislar mediante destilación extractiva.
2. Proceso de petróleo Phillips:
Este proceso de dos pasos ofrece ventajas como una vida útil más larga del catalizador y mayores rendimientos de butadieno.
- Deshidrogenación a buteno: el n-butano se somete a una deshidrogenación catalítica a buteno a 600 °C y 1 bar en un Cr2O3– Catalizador Na2O-Al2O3.
- Separación de buteno: los n-butenos se extraen utilizando auxiliares como acetona, acetonitrilo o furfural.
- Formación de butadieno: los n-butenos separados se deshidrogenan a butadieno en un reactor tubular isotérmico. El reactor se calienta mediante gases de combustión a 600 °C y funciona a 1 bar de presión con adición de vapor sobrecalentado sobre Catalizador Fe2O3-K2O-Al2O3.
- Recuperación y purificación de butadieno: la destilación extractiva con los auxiliares antes mencionados recupera y purifica el butadieno.
El proceso Phillips cuenta con tiempos de funcionamiento más prolongados (sin regeneración del catalizador) y un rendimiento de butadieno del 65 % basado en n-butano, lo que demuestra su eficiencia y selectividad mejorada en comparación con el proceso Houdry-Catadieno.
3.3.2. Deshidrogenación de n-butenos
Los n-butenos, que se encuentran comúnmente en la gasolina craqueada, la producción de olefinas y la deshidrogenación de GLP, a menudo están presentes como parte de una mezcla de hidrocarburos C4.
Si bien las parafinas C4 se pueden separar de las olefinas C4 mediante destilación extractiva (como en la recuperación de butadieno), la separación de isobuteno y n-buteno plantea un desafío único debido a sus puntos de ebullición cercanos.
Varios métodos abordan este obstáculo de la separación:
1. Proceso BASF: utiliza entre un 40 y un 45 % de H2SO4 para convertir selectivamente el isobuteno en terc-butanol, lo que permite una separación más fácil.
2. El isobuteno se puede convertir en metil terc-butil éter u oligómeros de isobuteno para su posterior procesamiento y separación.
3. Destilación con hidroisomerización: procesos como Isopure de Axens y CD DeIB de CD-Tech combinan la destilación con la hidroisomerización de 1-buteno a 2-buteno. Dado que el 2-buteno presenta un punto de ebullición distinto al del isobuteno, la destilación se vuelve factible.
4. Proceso Dow: Emplea la deshidrogenación de n-butenos con vapor sobre un catalizador de fosfato Ca/Ni estabilizado con Cr2O3. El vapor sobrecalentado proporciona el calor necesario para la reacción, logrando una conversión de buteno del 50 % y una selectividad de butadieno de hasta un 90 %.
5. Enfoque de reactor paralelo: Como el proceso Dow requiere la regeneración del catalizador después de 15 minutos, se emplean reactores paralelos, lo que permite una operación continua.
Shell y Phillips Petroleum también han desarrollado procesos similares, que muestran los diversos enfoques disponibles para la deshidrogenación de n-buteno y la producción de butadieno.
3.3.3. Deshidrogenación oxidativa de n-butenos
La deshidrogenación oxidativa (ODH) ofrece varias ventajas sobre los procesos de deshidrogenación convencionales para la producción de butadieno. Al eliminar el hidrógeno del equilibrio mediante oxidación, el ODH mejora significativamente la conversión y la selectividad:
2 C4H8 + O2 → 2 C4H6 + 2 H2O
Esta reacción exotérmica proporciona calor para la deshidrogenación endotérmica, lo que reduce aún más los requisitos energéticos. Además, la presencia de oxígeno y vapor ayuda a minimizar la coquización del catalizador.
Procesos ODH Históricos:
- Proceso Oxo-D (Petro-Tex): este proceso, empleado desde 1965, utiliza un catalizador de ferrita y opera bajo presión suave. Las ventajas incluyen un bajo consumo de vapor y energía de calefacción, alta conversión/selectividad, larga vida útil del catalizador y ausencia de necesidad de regeneración.
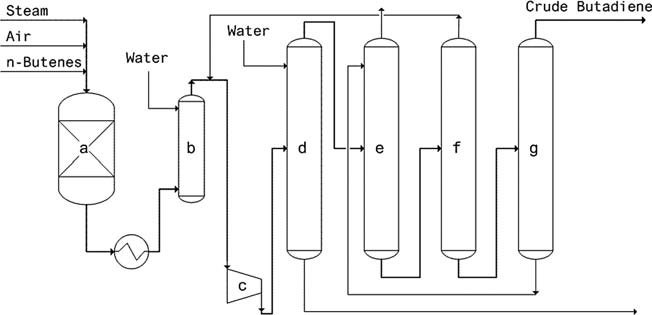
- Proceso O-X-D (Phillips): en funcionamiento desde 1976, este proceso emplea un catalizador Li-Sn-P-O y logra una conversión de buteno del 75-80 % con una selectividad de butadieno del 88-92 %.
Novedades más recientes en ODH:
- Proceso Nippon-Zeon: este proceso utiliza una mezcla de n-buteno/butano y aire/gas de escape como alimentación, lo que ofrece flexibilidad en la composición de la alimentación. Un catalizador de óxido metálico mixto alcanza un rendimiento de butadieno del 85 % basado en los butenos.
- Proceso químico Mitsubishi: este proceso utiliza un catalizador de Mo/Bi/Co y convierte una mezcla de C4 que contiene 70% de n-buteno con aire, vapor y nitrógeno. La adición de nitrógeno permite una alta relación oxígeno/butano, minimizando la coquización. La conversión de butadieno supera el 80% con una selectividad superior al 90%.
- Otros desarrollos: Asahi Kasai y Mitsui Chemicals también han desarrollado procesos ODH con resultados prometedores, incluidos reactores de lecho fluidizado y estrategias de conversión de etileno a butadieno.
Beneficios generales de ODH:
- Mayor conversión y selectividad en comparación con los procesos de deshidrogenación convencionales.
- Requisitos energéticos reducidos debido a la reacción de oxidación exotérmica.
- Coquización del catalizador inferior.
- Potencial para utilizar corrientes mixtas de C4 como materia prima.
Limitaciones:
- Los procesos ODH son generalmente más complejos que la deshidrogenación convencional.
- Las altas temperaturas requeridas pueden provocar la formación de subproductos no deseados si se utiliza oxígeno con butano
3.4. Aislamiento de butadieno a partir de fracciones de craqueador de vapor C4
El butadieno se aísla principalmente de fracciones C4 generadas durante el craqueo con vapor de hidrocarburos. La elección de la materia prima, como la nafta en Europa occidental y el GLP en Estados Unidos, desempeña un papel importante en el proceso, mientras que la gravedad del craqueo influye principalmente en la composición de la fracción C4.
Separar el butadieno de esta mezcla presenta un desafío debido a su comportamiento azeotrópico con el butano. En consecuencia, son necesarias técnicas especializadas.
El proceso de acetato cuproso de amonio, utilizando su capacidad para formar un complejo con butadieno, aborda este problema para fracciones con bajo contenido de butadieno y acetileno C4. Sin embargo, los niveles más altos de acetilenos requieren un tratamiento previo mediante hidrogenación selectiva.
La destilación extractiva surge como el método preferido para el aislamiento de butadieno. Esta técnica explota las diferentes afinidades de los diferentes componentes hacia disolventes orgánicos específicos en función de su grado de insaturación.
Los disolventes populares incluyen acetonitrilo (de Shell/KBR y LyondellBasell), N-metilpirrolidona (de BASF), dimetilformamida (de Nippon Zeon Chemicals) y furfural (de ConocoPhillips). ).
Estos procesos, que implican uno o dos pasos de destilación extractiva junto con la destilación convencional, separan el butadieno y otros componentes de alta afinidad de los butanos y butenos menos solubles. Otros pasos de purificación eliminan las impurezas restantes para lograr la pureza del butadieno.
El proceso BASF, que emplea NMP como solvente, cuenta con no corrosividad y altos rendimientos de butadieno, mientras que el proceso Nippon Zeon DMF exhibe ventajas similares.
Los avances recientes en este campo incluyen la tecnología de pared divisoria, que combina dos pasos de destilación en una unidad para mejorar la eficiencia, y mejores componentes internos de destilación y control de procesos para aumentar la capacidad y el rendimiento de las unidades existentes.
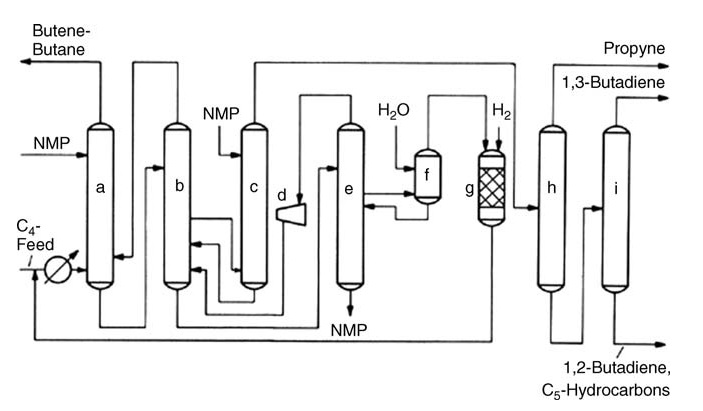
a) Lavadora principal; b) Rectificador; c) Después del lavado; d) Compresor centrífugo; e) Torre de desgasificación; f) Lavadora de agua; g) reactor de hidrogenación; h) Primera destilación; i) Segunda destilación
Enfoques alternativos como la hidrogenación selectiva de acetilenos C4 ofrecen varios beneficios. El proceso KLP de UOP elimina los acetilenos antes de la extracción, simplificando el proceso y aumentando el rendimiento de butadieno. El proceso CDHYDRO de CDTECH proporciona flexibilidad al permitir diferentes niveles de conversión de acetileno, minimizando la pérdida de butadieno.
3.5. Butadieno de recursos biológicos
La creciente tendencia a utilizar recursos renovables para la producción petroquímica se extiende al butadieno. Si bien existen varias vías, las que utilizan bioalcoholes son las más prometedoras.
Producción de bioetanol, establecida mediante la fermentación de caña de azúcar, maíz o material lignocelulósico, alcanzó 68 millones de toneladas a nivel mundial en 2011. Las tecnologías existentes pueden convertir el bioetanol en butadieno.
Aunque actualmente no existe una producción de biobutadieno a gran escala, el creciente interés del biobutanol como aditivo para combustible impulsa el desarrollo continuo de procesos. Deshidratación y deshidrogenación de biobutanol a n-buteno.
Otra ruta potencial implica la fermentación gaseosa del monóxido de carbono, obtenido de la gasificación de material orgánico o gases residuales industriales. Este proceso bacteriano produce 2,3-butanodiol, un precursor del butadieno. Sin embargo, esta tecnología aún se encuentra en sus primeras etapas.
Actualmente, la producción de butadieno de base biológica carece de competitividad económica en comparación con la ruta petroquímica. Sin embargo, el aumento de los precios del petróleo y el gas natural, junto con nuevos avances tecnológicos, podrían favorecer rutas de biotransformación en el futuro.
4. Usos e importancia económica del butadieno
El butadieno se utiliza principalmente como monómero o comonómero en la producción de caucho sintético. Contribuye al caucho de estireno-butadieno (SBR), al caucho de polibutadieno (BR), al caucho de acrilonitrilo-butadieno (NBR) y al caucho de cloropreno (CR).
Más allá de la producción de caucho, el butadieno desempeña un papel crucial en varios plásticos. Forma la columna vertebral del poliestireno resistente a los impactos, un sistema de dos fases que combina poliestireno y polibutadieno. Además, el butadieno contribuye a los polímeros ABS, una mezcla de acrilonitrilo, butadieno y estireno, y copolímeros MBS. , utilizados como modificadores del cloruro de polivinilo.
Además, el butadieno sirve como intermediario en diversas síntesis químicas.
En Estados Unidos, Japón y Europa occidental, la industria del automóvil constituye el principal consumidor de caucho de butadieno.
Los precios del butadieno experimentaron una caída significativa a principios de la década de 1990 debido al exceso de oferta debido al aumento de la capacidad de craqueo. Esto condujo a la hidrogenación del butadieno y a su uso como materia prima para el craqueo.
Desde finales de la década de 1990, la creciente demanda de productos de caucho y polímeros, particularmente en Asia, impulsó un aumento exponencial de la demanda de butadieno y un aumento constante de los precios.
La recesión económica mundial de 2008 provocó una caída dramática en la demanda de butadieno, seguida de una recuperación. Los precios del butadieno superaron a los del etileno, algo poco común, hasta que la volatilidad llevó a picos superiores a los 2.000 euros por tonelada.
Estas fluctuaciones de precios pueden atribuirse a la llegada de crackers a base de etano a Oriente Medio y al cambio de los crackers estadounidenses hacia una materia prima de gas más ligera. Estos cambios dan como resultado un rendimiento reducido de butadieno a pesar de la creciente demanda global.
5. Toxicología del butadieno
Exposición y toxicidad:
- La exposición ocupacional al butadieno es mayor en las industrias petroquímica, de purificación y procesamiento de butadieno, y en la fabricación de productos de caucho y plástico.
- El butadieno ingresa al cuerpo principalmente a través de la inhalación, siendo el contacto con la piel menos frecuente.
- La exposición no ocupacional puede ocurrir cerca de fuentes puntuales como incendios, humo de cigarrillos y emisiones de vehículos, aunque en niveles mucho más bajos que en entornos ocupacionales.
Estudios en animales:
- El butadieno presenta una toxicidad aguda baja; dosis altas causan narcosis precedida de excitación e hiperventilación.
- La exposición repetida a corto plazo a altas concentraciones (4000-8000 ppm) provoca salivación en ratas, pero no afecta el crecimiento, el consumo de alimentos ni otros parámetros.
- Los ratones expuestos a niveles similares muestran una disminución del peso corporal y una mayor mortalidad, con mayor sensibilidad al butadieno en comparación con las ratas.
- La exposición prolongada en ratas (hasta 111 semanas) provoca secreción nasal transitoria, ataxia y mortalidad temprana en la concentración más alta (8000 ppm). También aumenta el peso del hígado y sugiere un potencial de metaplasia en el pulmón y una mayor incidencia de algunos tumores.
- Los ratones expuestos a concentraciones más bajas (625-1250 ppm) durante 60-61 semanas presentan lesiones tóxicas y proliferativas en la cavidad nasal, necrosis hepática y atrofia de los órganos reproductivos. En particular, desarrollan diversos tumores, incluidos tumores malignos, antes y en mayor proporción que los controles.
- Un estudio de dos años con concentraciones aún más bajas (6,25-625 ppm) revela el desarrollo temprano de linfomas extensos, tumores cardíacos inusuales y tumores de pulmón en ratones.
Metabolismo y mutagenicidad:
- El butadieno se metaboliza en el hígado para formar intermediarios epóxido, que se sospecha que son los principales contribuyentes a su toxicidad y carcinogenicidad.
- La formación de estos metabolitos es más pronunciada en ratones que en ratas y humanos.
- El butadieno exhibe mutagenicidad en la prueba de Ames solo en presencia de enzimas, lo que sugiere la formación de un intermediario mutagénico.
Datos humanos:
- Hay datos limitados en humanos disponibles sobre los efectos de la exposición al butadieno.
- Los voluntarios expuestos a una concentración muy alta (8000 ppm) experimentaron irritación temporal, visión borrosa y síntomas respiratorios, pero no se observaron efectos acumulativos.
- Los estudios hematológicos de trabajadores expuestos a niveles promedio de 20 ppm de butadieno no mostraron anomalías significativas.
- Los estudios de mortalidad temprana de trabajadores de la industria del caucho de estireno-butadieno no sugirieron un mayor riesgo de cáncer.
- Revisiones recientes de estudios epidemiológicos proporcionan evidencia de un mayor riesgo de neoplasias malignas hematolinfáticas, en particular leucemia, con una exposición elevada al butadieno.
Límites de clasificación y exposición en el lugar de trabajo:
- Según datos de animales y humanos, la Agencia Internacional para la Investigación del Cáncer (IARC) clasifica el butadieno como carcinógeno del Grupo 1.
- Los límites de exposición laboral varían ligeramente entre los distintos organismos reguladores, con límites que oscilan entre 0,5 y 4,4 mg/m3.
- Se están realizando esfuerzos continuos para reducir los niveles de exposición en los lugares de trabajo que manipulan butadieno.
Referencia
- Butadiene; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a04_431.pub2
