Crotonsäure: Eigenschaften, Reaktionen, Herstellung und Verwendung
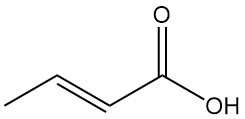
Crotonsäure ist das trans-Isomer der 2-Butensäure. Es handelt sich um eine kurzkettige, ungesättigte Carbonsäure mit der chemischen Formel CH3CH=CHCOOH. Das cis-Isomer der 2-Butensäure ist als Isocrotonsäure bekannt.
Crotonsäure erscheint als weißer bis gelblicher Feststoff mit einem stechenden, erstickenden Geruch, während Isocrotonsäure eine ölige, farblose Flüssigkeit mit einem charakteristischen Geruch ist, der an braunen Zucker erinnert.
Der Begriff „Crotonsäure“ stammt von Crotonöl, einem Öl, das aus den Samen von Croton tiglium gewonnen wird. Ursprünglich wurde Crotonsäure fälschlicherweise als Produkt identifiziert, das bei der Verseifung dieses Öls entsteht.
Crotonsäure kommt im rohen Holzdestillat vor und entsteht als Metabolit beim Fettsäureabbau.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Crotonsäure
Bei der Kristallisation bildet Crotonsäure im monoklinen System weiße Nadeln oder Prismenkristalle. Es ist in Wasser schwer löslich und in Ethanol, Aceton, Ethylacetat und Toluol löslich und bildet bei 99,7 °C ein Azeotrop mit Wasser, das 96,86 % Crotonsäure enthält.
Isocrotonsäure ist mit Wasser und polaren Lösungsmitteln mischbar und bildet mit Crotonsäure (30 % Crotonsäure) ein eutektisches Gemisch, das bei -3°C schmilzt.
Tabelle 1 fasst einige der physikalischen Eigenschaften von Crotonsäure und Isocrotonsäure zusammen.
| Eigenschaft | Crotonsäure | Isocrotonsäure |
|---|---|---|
| Molekulargewicht | 86,09 g/mol | 86,09 g/mol |
| Siedepunkt | 189 °C | 169°C |
| Schmelzpunkt | 72°C | 15°C |
| Dichte (20°C) | 1,018 | 1,0267 |
| Brechungsindex | 1.4228 (80 °C) | 1.4456 (20 °C) |
| Löslichkeit in Wasser, g/kg | 41,5 (0°C), 94 (25°C) | 656 (40°C), 1260 (42°C) |
| Flammpunkt | 88 °C | - |
| Selbstzündungstemperatur | 396 °C | - |
| Dampfdruck | 24 Pa (20°C), 880 Pa (70°C) | - |
| Spezifische Wärme | 3,031 J g-1 K-1 (fest) 2,072 J g-1 K-1 (flüssig) |
- |
| Verbrennungswärme | 2,00 MJ/mol | 2,03 MJ/mol |
| Schmelzwärme | 150,9 J/g | - |
| pKa | 4,817 (25°C) | - |
2. Chemische Reaktionen von Crotonsäure
Crotonsäure ist in wässrigen Lösungen eine schwache Säure und kann daher mit organischen und anorganischen Basen reagieren.
Crotonsäure durchläuft beim Erhitzen, bei Einwirkung von Säuren, Basen, UV-Strahlung oder anderen Reagenzien verschiedene Umwandlungen. Zu diesen Reaktionen gehören Isomerisierung, Oligomerisierung und Polymerisation.
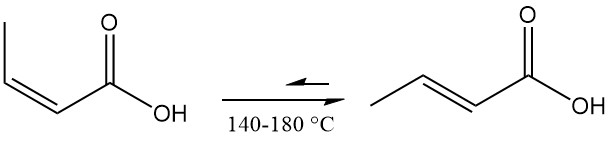
Isocrotonsäure isomerisiert zu Crotonsäure und erreicht bei 140–180 °C ein Gleichgewicht. Als Nebenprodukt entsteht 3-Butensäure, wobei die Endmischung ein Isocrotonsäure-zu-Crotonsäure-Verhältnis von etwa 0,17:1 enthält.
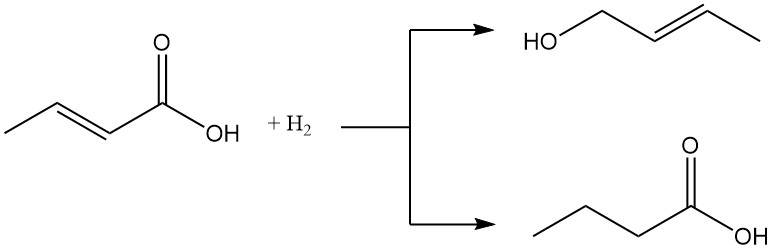
Sowohl Crotonsäure als auch Isocrotonsäure können entweder zu Crotylalkohol oder Buttersäure reduziert werden. Umgekehrt können sie zur entsprechenden Persäure oxidiert werden.
Crotonsäure polymerisiert leicht über einen Radikalmechanismus mit verschiedenen Monomeren. Copolymere mit Vinylacetat sind industriell wichtig.
Additionsreaktionen an die Doppelbindung der Crotonsäure ergeben 2-substituierte oder 2,3-disubstituierte Buttersäuren.
Durch katalytische Hydrierung wird Crotonsäure in Buttersäure umgewandelt.
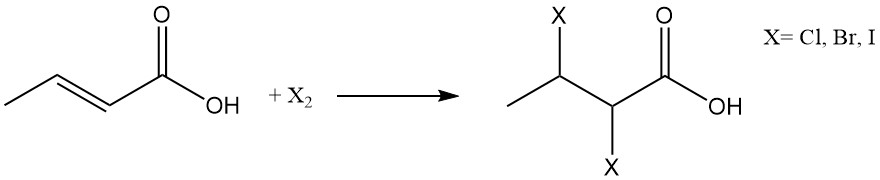
Durch die Halogenierung bzw. Anlagerung von Halogenwasserstoffen entstehen 2,3-Dihalobuttersäuren bzw. 3-Halogenbuttersäuren.
Durch die Reaktion von Crotonsäure mit Osmiumtetroxid (OsO4) oder Peroxybenzoesäure entsteht 2,3-Dihydroxybuttersäure.
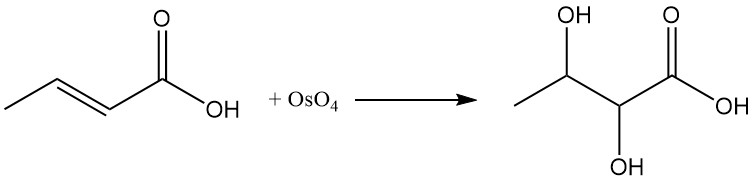
Unter geeigneten Reaktionsbedingungen entsteht durch Ammoniakzugabe β-Aminobuttersäure.
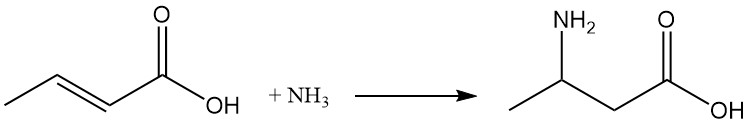
Aufgrund ihres dienophilen Charakters nimmt Crotonsäure an Diels-Alder-Reaktionen teil.
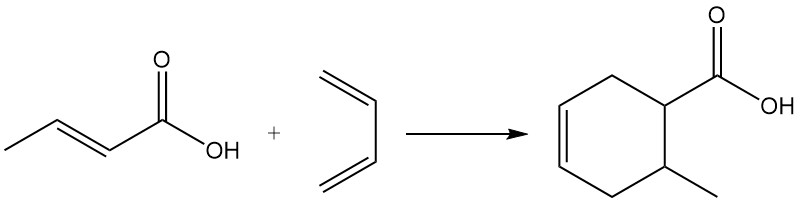
Die Veresterung von Crotonsäure ist mit herkömmlichen Methoden möglich. Allerdings führt das Vorhandensein der konjugierten Doppelbindung im Vergleich zu Buttersäure häufig zu langsameren Reaktionsgeschwindigkeiten.
Crotonylhalogenide können durch Reaktion von Crotonsäure mit dem entsprechenden Acylhalogenid synthetisiert werden.
Crotonsäureanhydrid wird entweder durch Reaktion von Crotonylchlorid mit Natriumcrotonat oder durch Behandlung von Crotonsäure mit Essigsäureanhydrid gewonnen.
3. Herstellung von Crotonsäure
Crotonsäure wird industriell durch Oxidation von Crotonaldehyd hergestellt. Dieses Verfahren wird von Unternehmen wie Weylchem Frankfurt verwendet und verwendet eine zweistufige Reaktionssequenz:
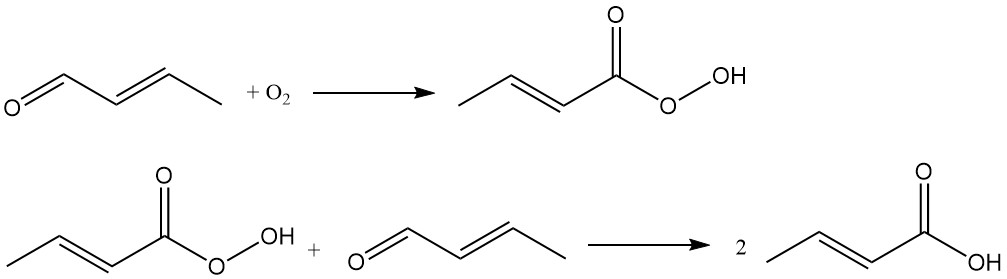
Crotonaldehyd wird oxidiert, um als Zwischenprodukt Peroxocrotonsäure zu bilden, die mit einem anderen Crotonaldehydmolekül zu Crotonsäure reagiert.
Die Reaktion findet typischerweise bei moderaten Temperaturen (20–45 °C) und Drücken (100–500 kPa) statt. Als Katalysatoren werden Metallsalze, insbesondere von Mangan, Kobalt, Kupfer oder Thallium, zugesetzt, um die unerwünschte Anreicherung von Peroxiden zu verhindern. Zu den Nebenprodukten gehören Ameisensäure, Essigsäure, Wasser und Kohlendioxid aus der vollständigen Oxidation.
Ein historisches Verfahren von Hoechst verwendete einen Mangansalzkatalysator für die Crotonaldehyd-Oxidation bei 20–30 °C. Die resultierende Reaktionsmischung enthielt ungefähr:
- 20–30 % Crotonsäure
- 1–3 % Ameisen- und Essigsäure
- 3-5 % Wasser
- Spuren von 3-Butensäure, unbekannten Verbindungen und 0,5–1 % Isocrotonsäure
Überschüssiger Crotonaldehyd wird durch Vakuumdestillation zurückgewonnen und in die Reaktion zurückgeführt. Der an Crotonsäure (60–70 %) reiche Destillationsrückstand wird durch eine zweite Vakuumdestillation weiter gereinigt.
Die niedrigsiedende Fraktion und der Rückstand werden als Abfall verworfen. Die Hauptproduktfraktion enthält Crotonsäure mit etwas Isocrotonsäure (3-5 %). Anschließend wird durch fraktionierte Kristallisation die Isocrotonsäure entfernt, wodurch hochreine Crotonsäure (bis zu 99,9 %) entsteht.
Während die industrielle Produktion auf der Oxidation von Crotonaldehyd beruht, gibt es mehrere alternative Methoden für die Synthese von Crotonsäure im Labormaßstab. Diese beinhalten:
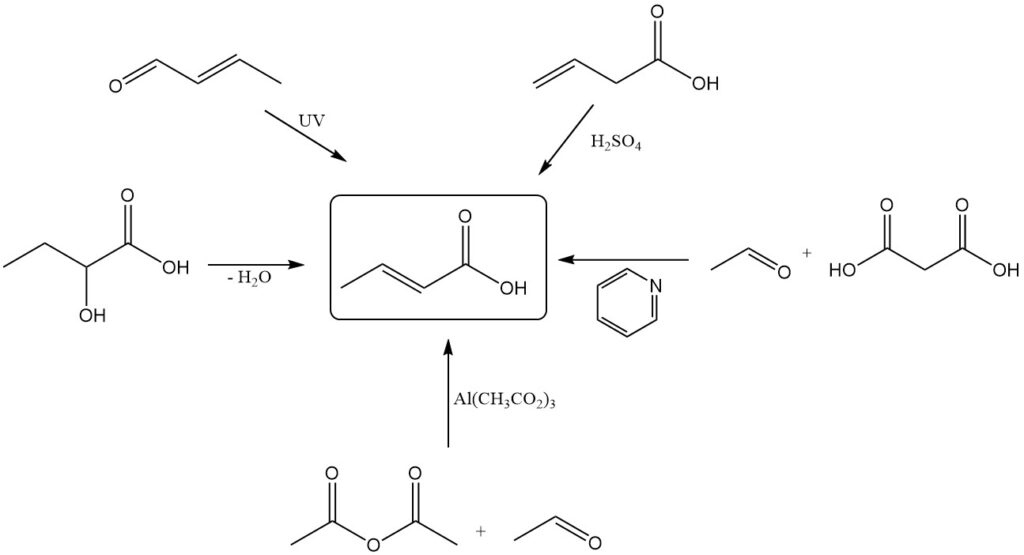
- Dehydratisierung von 2-Hydroxybuttersäure
- Photochemische Oxidation oder oxidative Bestrahlung (mit Ultraschall) von Crotonaldehyd
- Isomerisierung von Vinylessigsäure mit Schwefelsäure
- Kondensation von Acetaldehyd und Malonsäure unter Verwendung von Pyridin als Katalysator
- Oxidation von Buten mit einem Heteropolymolybdänsäure-Katalysatorsystem
- Oxycarbonylierung von Propen mit Übergangsmetallkomplexkatalysatoren
- Carbonylierung von Propylenoxid
- Reaktion von Essigsäureanhydrid mit Acetaldehyd unter Verwendung eines basischen Aluminiumacetatkatalysators
- Carbonylierung von Allylalkohol mit Katalysatoren auf Nickel- oder Palladiumbasis
Isocrotonsäure kann aus Gemischen, die Crotonsäure enthalten, mithilfe von Techniken wie fraktionierter Kristallisation, Rektifikation (Destillation) oder Gelfiltrationschromatographie abgetrennt werden.
Eine stereospezifische Methode zur Laborvorbereitung von Isocrotonsäure beinhaltet die Bromierung von 2-Butanon (Methylethylketon), gefolgt von einer Favorskii-Umlagerung.
4. Verwendungsmöglichkeiten von Crotonsäure
Die Hauptanwendung von Crotonsäure ist die Herstellung von Copolymeren mit verschiedenen Comonomeren. Crotonsäure-Vinylacetat-Copolymere sind von industrieller Bedeutung. Diese Copolymere werden häufig unter Handelsnamen wie Mowilith, Vinnapas und Vinac vermarktet.
Crotonsäure-Copolymere werden in Farben, Beschichtungen, Schmelzfarben, Klebstoffen und Schmelzklebstoffen verwendet. Sie werden auch für Beschichtungen auf Papier und Textilien, als Flockungsmittel, Bindemittel für Sprengstoffe, Keramik und Agrochemikalien sowie als Bohrzusätze verwendet.
Andere Anwendungen von Crotonsäure umfassen:
- Als antimikrobieller Wirkstoff in Esterform für Deodorants.
- In UV-Absorbern und Metalleffekt-Interferenzpigmenten.
- Fettalkoholester der Crotonsäure werden in der Lederindustrie eingesetzt.
- Die freie Säure findet Anwendung in Kraftstoffen, beim Ätzen von Metalloberflächen, bei der elektrochemischen Metallabscheidung und bei der PVC-Wärmestabilisierung.
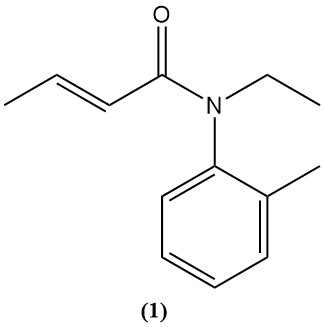
Crotonsäure und ihre Derivate wie Anhydrid und Chlorid dienen als Vorläufer für verschiedene Agrochemikalien und Pharmazeutika. Ein Beispiel ist Crotamiton (1), ein Medikament zur Behandlung von Krätze (skabizid) und zur Linderung von Juckreiz (juckreizstillend).
5. Toxikologie von Crotonsäure
Crotonsäure ist eine ätzende Substanz und kann bei Kontakt mit Augen, Haut oder Atemwegen schwere Reizungen oder Verbrennungen verursachen. Das Einatmen kann zu Brennen, Husten, Kopfschmerzen, Übelkeit, Halsschmerzen und Kurzatmigkeit führen (die Symptome können verzögert auftreten). Das Verschlucken verursacht Schmerzen, Brennen, Halsschmerzen, Durchfall und Erbrechen.
Toxikologische Daten aus Tierstudien sind unten aufgeführt:
- LD50 (Ratte, oral): 1000 mg/kg
- LD50 (Ratte, i.p.): 100 mg/kg
- LD50 (Kaninchen, dermal): 600 mg/kg
Der Körper kann während des Fettstoffwechsels auf natürliche Weise Crotonsäure produzieren und diese durch Enzyme in der Leber und anderen Geweben schnell abbauen. Es ist unwahrscheinlich, dass die Exposition gegenüber nicht reizenden Konzentrationen zu kumulativen Wirkungen führt.
Crotonsäure kann das Pflanzenwachstum und die Samenkeimung beeinträchtigen.
Referenz
- Crotonaldehyde and Crotonic Acid; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a08_083.pub2
