Ácido butírico: propiedades, reacciones, producción y usos
¿Qué es el ácido butírico?
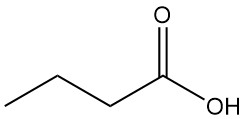
El ácido butírico, también conocido como ácido n-butanoico, es un ácido graso volátil de cadena corta con la fórmula química C4H8O2. Es un líquido oleoso incoloro con un olor rancio desagradable que se mezcla con agua y la mayoría de los solventes orgánicos.
El ácido butírico fue descubierto en 1869 por Lieben y Rossi. En latín, ácido butírico significa el ácido de la mantequilla, ya que se descubrió por primera vez en la mantequilla rancia (el ácido butírico se hidroliza a partir del glicérido y causa un olor muy desagradable).
El ácido butírico es un ácido graso saturado de cadena corta que se encuentra en forma de ésteres en grasas animales y aceites vegetales y es producido naturalmente por bacterias anaeróbicas.
Tabla de contenido
1. Propiedades físicas del ácido butírico
El ácido butírico es un ácido carboxílico que forma un líquido aceitoso e incoloro que es soluble en agua, etanol y éter y ligeramente soluble en tetracloruro de carbono.
La Tabla 1 resume las propiedades físicas del ácido butírico.
| Propiedad | Valor |
|---|---|
| Número CAS | [107-92-6] |
| Fórmula química | C4H8O2 |
| Peso molecular | 88,1 g/mol |
| Punto de fusión | -7,9 °C |
| Punto de ebullición punto | 163,5 °C |
| Densidad | 0,958 g/cm3 |
| pKa | 4,82 a 25 °C |
| Viscosidad a 25 °C | 1,426 mPa.s |
| Índice de refracción | 1,3991 a 20 °C |
| Temperatura crítica | 342,05 °C |
| Presión crítica | 4,06 MPa |
| Presión de vapor | 1,65 mmHg |
| Punto de inflamación | 72 °C |
| Temperatura de autoignición | 443 °C |
2. Reacciones químicas del ácido butírico
El grupo carboxílico del ácido butírico sufre diferentes tipos de reacciones, principalmente desprotonación, reducción y sustitución nucleofílica. Otras reacciones tienen lugar en la posición α del grupo carboxílico debido a la presencia de un hidrógeno ácido.
Las sales de metales alcalinos del ácido butírico se obtienen fácilmente por neutralización utilizando una base (por ejemplo, hidróxido de sodio). Los butiratos de amonio se obtienen por reacción con amoníaco o aminas.
El n-butanol se puede preparar por reducción del grupo carboxilo utilizando agentes reductores como el hidruro de litio y aluminio o por hidrogenación catalítica del ácido butírico o sus ésteres.
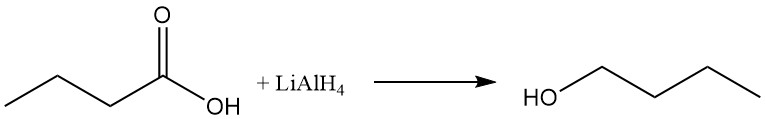
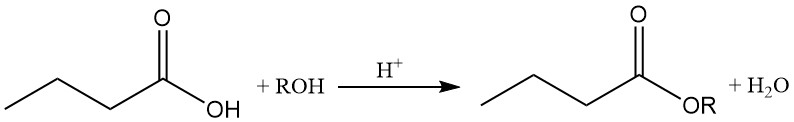
Los ésteres de ácido butírico se producen mediante una reacción catalizada por ácido entre el ácido butírico y alcoholes u olefinas. Los butiratos son intermediarios importantes en diferentes industrias.
Las amidas butíricas se pueden sintetizar directamente haciendo reaccionar el ácido butírico con amoníaco o aminas. Como primero se forma el butirato de amonio, se requiere calentamiento para eliminar el agua y acelerar la reacción.
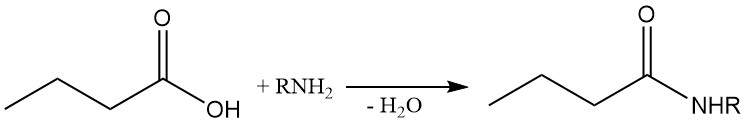
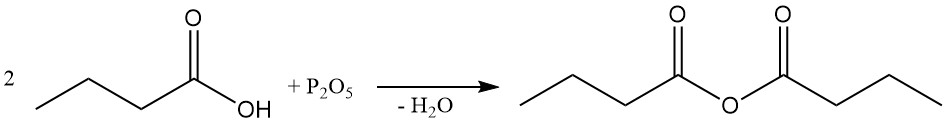
El anhídrido butírico se prepara mediante la deshidratación del ácido butírico utilizando un agente deshidratante (por ejemplo, pentóxido de fósforo) o, preferiblemente, mediante la reacción del cloruro de butirilo con ácido butírico o su sal.
Los haluros de butirilo se pueden obtener a partir del ácido butírico utilizando compuestos halogenados como haluros de tionilo, haluros de fósforo u oxihaluros de fósforo. Los haluros de butirilo, altamente reactivos y sensibles a la hidrólisis, son una clase valiosa de intermediarios sintéticos.
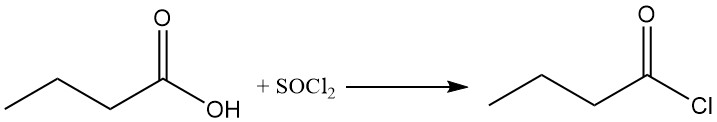
La oxidación del ácido butírico con peróxido de hidrógeno produce acetona, dióxido de carbono y agua.
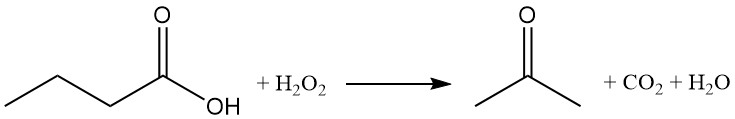
En determinadas condiciones, el ácido butírico puede sufrir descarboxilación.
El ácido butírico que tiene al menos un hidrógeno en el carbono próximo a la función carboxilo también puede desprotonarse en esa posición α, pero esta tendencia no es tan pronunciada como en el caso de los aldehídos y las cetonas. Son necesarios dos equivalentes de una base fuerte no nucleófila.
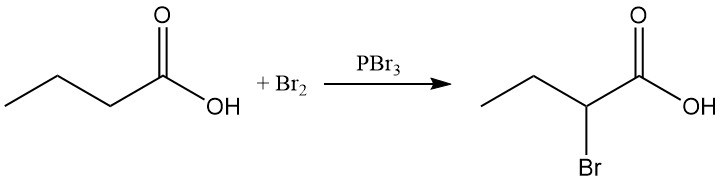
En la halogenación de Hell-Volhard-Zelinsky, utilizando bromo y tribromuro de fósforo, se puede sintetizar ácido 2-bromobutírico.
3. Producción de ácido butírico
3.1. Producción química de ácido butírico
En el mercado, el ácido n-butírico se produce por oxidación en fase líquida del n-butanal con oxígeno. Este proceso continuo produce un líquido incoloro, que se purifica por rectificación.
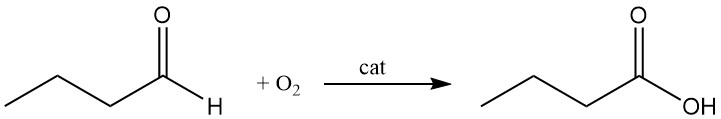
El proceso de hidroformilación (proceso Oxo) del propileno es el principal método de producción de n-butanal. Implica la hidroformilación del propileno utilizando gas de síntesis (principalmente hidrógeno y monóxido de carbono) a altas temperaturas (100–180 °C) y presiones entre 20 y 30 MPa en presencia de un catalizador metálico.
El proceso LP Oxo (reacción de oxo de rodio modificado con trifenilfosfina) produce hasta un 90 % de ácido butírico crudo. Sin embargo, el proceso Oxo genera tanto butiraldehído como isobutiraldehído, lo que reduce la selectividad del ácido butírico. Además, el proceso produce subproductos nocivos para el medio ambiente, como catalizadores metálicos gastados y compuestos tóxicos.
Para superar estos problemas, se ha desarrollado una oxidación de un solo paso del butiraldehído a ácido butírico utilizando oxígeno molecular y catalizadores heterogéneos. Este proceso logra rendimientos de ácido butírico superiores al 99,5 % y una selectividad superior al 95 % en comparación con el proceso Oxo.
Las sales de metales alcalinos y de cobalto son catalizadores heterogéneos altamente activos utilizados en este proceso.
En una patente de Huntsman Petrochemical Corporation, el ácido butírico se puede producir mediante hidrogenación catalítica de anhídrido maleico con una selectividad del 35 % para el ácido butírico.
Los principales fabricantes de ácido butírico incluyen Oxea, Eastman y Perstorp.
3.2. Biosíntesis del ácido butírico
La biosíntesis del ácido butírico ocurre en condiciones anaeróbicas. El acetil-CoA, derivado de la degradación de ácidos grasos o piruvato a través de la piruvato-ferredoxina oxidorreductasa, sirve como precursor. El acetil-CoA se transforma en butiril-CoA, produciendo posteriormente ácido butírico.
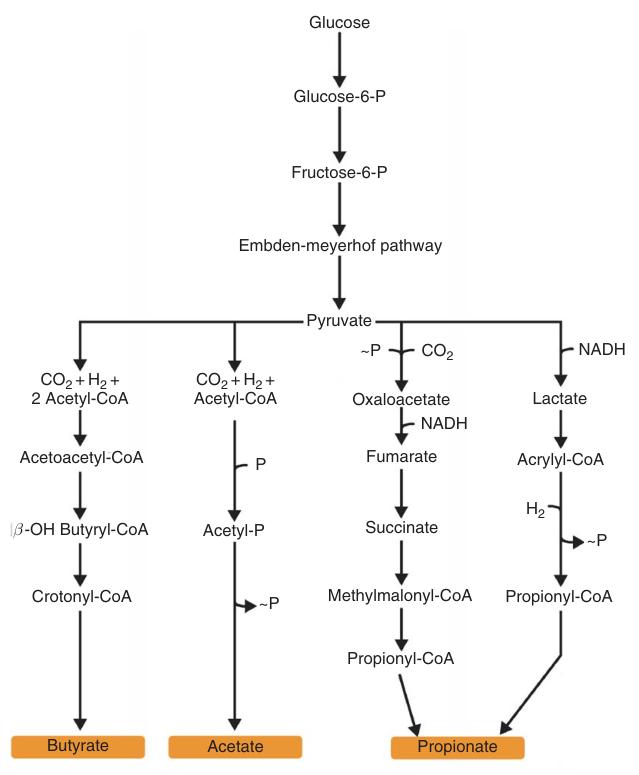
La fermentación anaeróbica de glucosa a ácido butírico genera tres moléculas de ATP, lo que supera el rendimiento de ATP de la fermentación de ácido láctico/etanol (dos ATP) y se acerca al de la fermentación de ácido acético (cuatro ATP).
El ácido butírico es un producto final de la fermentación producido por bacterias anaeróbicas obligadas, siendo Clostridium butyricum el organismo principal. Otras bacterias productoras de ácido butírico incluyen Clostridium, Butyribacterium, Sarcina, Megasphera, Fusobacterium, Peptococcus, Butyrivibrio, Pseudobutyrivibrio y Eubacterium.
Las condiciones óptimas de crecimiento incluyen 35-37 °C, una atmósfera de CO2/N2 y un rango de pH de 4,5 a 7,0. Se pueden utilizar hexosas, pentosas y polisacáridos como materias primas.
La producción de ácido butírico se optimiza controlando la disponibilidad de nutrientes. Limitar la glucosa y elementos esenciales como el fosfato y el nitrógeno mientras se utilizan condiciones de crecimiento lento favorece la formación de butirato sobre otros productos. Para mejorar la eficiencia, se pueden combinar métodos de fermentación por lotes, por lotes alimentados o continua con técnicas de retención celular.
La acumulación de ácido butírico durante el proceso de fermentación puede reducir el proceso de producción. Para evitarlo, se reduce la concentración de ácido butírico en el caldo de fermentación mediante destilación, evaporación, electrodiálisis de permeado, adsorción, extracción o pertracción.
4. Usos del ácido butírico
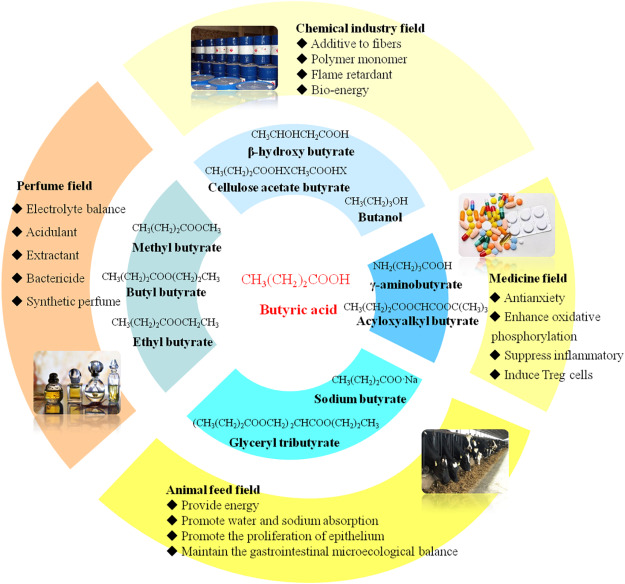
El ácido butírico se utiliza principalmente en la producción de acetato butirato de celulosa, un polímero empleado en la fabricación de plásticos, revestimientos y textiles.
En la industria alimentaria, el ácido butírico y sus derivados se utilizan como agentes aromatizantes, contribuyendo al sabor característico de la mantequilla, el queso y los dulces. Además, se utiliza como conservante de alimentos debido a sus propiedades antimicrobianas.
Los ésteres de ácido butírico se utilizan en perfumes, y algunos sirven como bases de ingredientes aromatizantes artificiales en ciertos licores, jarabes de agua carbonatada y caramelos.
El ácido butírico se utiliza en formulaciones para preparar cebos de pesca y repelentes de vida silvestre debido a su potente olor.
El ácido butírico se utiliza en productos farmacéuticos como antagonista de la histamina. Sus derivados han demostrado potencial como agentes anticancerígenos al inducir la diferenciación celular. Se han sugerido profármacos de ácido butírico para el tratamiento de enfermedades neoplásicas y trastornos de la β-globina.
También se utiliza como intermediario en la producción de butiroperóxidos, herbicidas, emulsionantes, desinfectantes y surfactantes.
En la industria agrícola, el ácido butírico se emplea como aditivo alimentario y suplemento dietético para la cría de cerdos, ganado vacuno y aves de corral. Además, ha demostrado su eficacia para prevenir el crecimiento de hongos en cereales con alto contenido de humedad.
Investigaciones recientes han explorado el potencial del ácido butírico como precursor para la producción de biocombustibles. Su conversión en butanol, un alcohol de mayor energía, es un área activa de investigación.
5. Toxicología del ácido butírico
Si bien el ácido butírico no se utiliza en productos de consumo, la exposición de la población general se produce principalmente al consumir alimentos que lo contienen, como grasas de leche animal, aceites esenciales, aceites vegetales, fluidos animales, productos fermentados y en ciertas frutas.
El ácido butírico se metaboliza rápidamente en el hígado, principalmente a ácido acético y cuerpos cetónicos (acetona, acetoacetato y β-hidroxibutirato). La eliminación del ácido butírico sigue un patrón bifásico en humanos. Una fase inicial rápida con una vida media de 0,5 minutos es seguida por una fase de eliminación más lenta con una vida media de 13,7 minutos.
Toxicidad aguda
El ácido butírico está clasificado como no tóxico según los valores de LD50 en varios modelos animales.
- LD50 oral en ratas: 2940–8790 mg/kg
- LD50 intraperitoneal o subcutánea en ratones: 3180 mg/kg
- LC50 por inhalación en conejos: 440 mg/l
El ácido butírico es un irritante moderado para la piel y los ojos. Se observó irritación ocular grave y quemaduras corneales en conejos. Se observó un aumento del letargo, disnea, dilatación bronquial y capilar y enfisema en conejos expuestos al aerosol de ácido butírico (40 mg/l).
Las dosis intravenosas altas de ácido butírico (sal sódica) causan depresión temporal del sistema nervioso central en conejos y perros. Se observó un aumento de la concentración plasmática de insulina en corderos tras la administración intravenosa de ácido butírico.
La exposición aguda en humanos al ácido butírico produce principalmente irritación o quemaduras en la piel, los ojos y el tracto respiratorio.
En humanos, los síntomas de inhalación incluyen dolor de garganta, tos, sensación de ardor, falta de aire y dificultad para respirar. El contacto dérmico produce dolor, enrojecimiento, ampollas y quemaduras en la piel. El contacto con los ojos produce dolor, enrojecimiento, quemaduras graves y posible pérdida de la visión.
La ingestión produce sensación de ardor, dolor abdominal, shock y posible colapso.
Toxicidad crónica
En estudios con animales, la exposición repetida a dosis moderadas a altas de acetato de n-butilo y n-butanol (metabolitos del ácido butírico) es generalmente bien tolerada por los animales. Sin embargo, dosis altas de ácido butírico en la dieta provocaron pérdida de peso y anomalías en el tejido gástrico en ratas.
En estudios realizados en humanos, el ácido butírico se considera un aditivo alimentario GRAS (generalmente reconocido como seguro). La exposición crónica puede producirse a través de la producción endógena y la ingesta alimentaria. Si bien es un metabolito esencial, la exposición prolongada puede dañar los pulmones, el sistema nervioso y las membranas mucosas.
Inmunotoxicidad
La exposición prolongada de ratones, ratas y conejos a bajas concentraciones atmosféricas de ácido butírico (0,1–0,2 mg/l) provocó un aumento significativo de los linfocitos y neutrófilos circulantes.
Esta respuesta inmunitaria se atribuye principalmente a la naturaleza irritante del ácido butírico en lugar de a un objetivo específico del sistema inmunitario.
Toxicidad reproductiva
Los estudios sobre la toxicidad reproductiva del ácido butírico se basan principalmente en sus metabolitos, n-butanol y acetato de n-butilo.
Los estudios de inhalación de n-butanol y acetato de n-butilo no mostraron efectos adversos sobre los parámetros reproductivos hasta determinadas concentraciones:
- Toxicidad reproductiva en mujeres: 6000 ppm para n-butanol y 1500 ppm para acetato de n-butilo.
- Toxicidad reproductiva en hombres: 3000 ppm para acetato de n-butilo.
Toxicidad para el desarrollo
La administración directa de ácido butírico a ratas preñadas provocó una elevada mortalidad materna y una reducción de la ganancia de peso corporal en dosis altas (100 y 133 mg/kg/día). A pesar de la toxicidad materna, no se observaron efectos adversos en las crías.
El ácido butírico induce malformaciones (microcefalia, defectos oculares, edemas y defectos intestinales) en embriones de rana en una concentración de 400 mg/l.
Genotoxicidad y carcinogenicidad
El ácido butírico no es genotóxico ni carcinógeno.
Referencias
- Carboxylic Acids, Aliphatic; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a05_235.pub2
- https://www.sciencedirect.com/science/article/abs/pii/B9780123864543005911
- https://www.sciencedirect.com/science/article/abs/pii/B9780128096338130833
- Process of Making Butyric Acid. – https://patents.justia.com/patent/20080009652
- https://www.sciencedirect.com/science/article/abs/pii/S0734975018301629
- https://onlinelibrary.wiley.com/doi/10.1100/2012/471417
- Fermentation process for producing butyric acid. – https://patents.google.com/patent/US2181310A/en
