Choline (chimie)
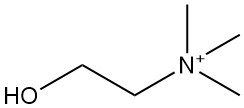
La choline [62-49-7], également connue sous le nom d’hydroxyde de triméthyl(2-hydroxyéthyl)ammonium, est un composé d’ammonium quaternaire de formule moléculaire C5H15O2N. Il a été isolé pour la première fois dans la bile de porc en 1849 par Stecker et est ensuite retrouvé dans le tissu cérébral.
La structure chimique de la choline peut être représentée par (CH3)3N+CH2CH2OH∙OH–. La choline libre existe en petites quantités dans les matières biologiques. Les formes plus fréquentes comprennent la phosphorylcholine, la phosphatidylcholine (lécithine) et l’acétylcholine.
Table des matières
La choline joue un rôle dans le métabolisme et la synthèse de la glycine, de la bétaïne, de la cystéine, de la sérine, de la méthionine et de divers autres composés biologiques contenant du méthyle.
La choline a quatre fonctions principales dans le corps :
- Composant structurel : Comme la phosphatidylcholine (lécithine) et la sphingomyéline, la choline constitue un composant important des membranes cellulaires.
- Agent lipotrope : La choline prévient la stéatose hépatique.
- Neurotransmetteur : L’acétylcholine, un dérivé de la choline, agit comme un neurotransmetteur.
- Donateur de groupes méthyle : La choline sert de source de groupes méthyles labiles.
Bien qu’historiquement considérée comme une vitamine, la choline ne répond pas strictement à la définition en raison de son manque de fonction de cofacteur enzymatique. Cependant, tout comme les vitamines, la choline joue un rôle essentiel dans la nutrition. Les recommandations d’apport quotidien sont significativement plus élevées pour la choline que pour les vitamines (voir tableau 1).
| Population | Catégorie | Apport adéquat (mg/jour) |
|---|---|---|
| Bébés | 0 à 5 mois | 125 |
| Bébés | 6 à 11 mois | 150 |
| Enfants et adolescents | 1 à 3 ans | 200 |
| 4 à 8 ans | 250 | |
| 9 à 13 ans | 375 | |
| Hommes (14 à 18 ans) | 550 | |
| Femmes (14 à 18 ans) | 400 | |
| Adultes | Hommes (19 ans et plus) | 550 |
| Femmes (19 ans et plus) | 425 | |
| Grossesse | Tous les âges | 450 |
| Allaitement | Tous les âges | 550 |
La Pharmacopée des États-Unis élabore actuellement des monographies pour le chlorure de choline et le bitartrate de choline à inclure dans les suppléments USP 24.
La stéatose hépatique et un taux de croissance réduit sont les principaux signes d’une carence en choline chez les animaux en développement. Des études ont montré que diverses espèces, notamment les rats, les souris et la volaille, ont besoin de choline pour une croissance optimale et une fonction hépatique saine.
Les sels de choline (chlorure, citrate de dihydrogène et bitartrate) sont fréquemment ajoutés aux aliments pour animaux comme complément alimentaire.
1. Propriétés de la Choline
La choline est un composé basique avec un pKa de 5,06 qui peut absorber le dioxyde de carbone et la vapeur d’eau de l’atmosphère. La choline disponible dans le commerce se présente généralement sous forme de solutions dans du méthanol ou dans de l’eau, avec des concentrations ne dépassant généralement pas 45 % en volume.
Solubilité :
- Soluble dans l’éthanol
- Légèrement soluble dans l’acétone et le chloroforme
- Insoluble dans l’éther, le benzène, le toluène et le tétrachlorure de carbone
La choline réagit facilement avec les acides pour former des sels stables. Cependant, la cristallisation est difficile pour la plupart des sels de choline, à l’exception des formes chlorure, bitartrate et citrate de dihydrogène. De plus, la choline peut réagir avec les acides pour former des esters.
En tant qu’hydroxyde d’ammonium quaternaire, la choline subit une auto-décomposition lors du chauffage. Cette réaction, connue sous le nom d’élimination d’Hofmann, se déroule comme suit :

L’alcool vinylique intermédiaire instable peut soit se réarrange en acétaldéhyde, soit réagir avec l’eau pour former de l’éthylène glycol. L’acétaldéhyde peut subir une condensation aldolique supplémentaire, conduisant à des produits colorés. La triméthylamine libérée confère à la solution une forte odeur de « poisson ».
2. Sels de choline
La choline forme divers sels aux propriétés physiques et chimiques différentes. Voici une description de quelques sels de choline courants :
2.1. Chlorure de choline [67-48-1]
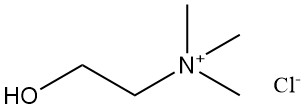
- Formule : C5H14ONCl
- Masse molaire : 139,63 g/mol
- Apparence : Un solide cristallin blanc avec une légère odeur d’amine et un fort goût saumâtre.
- Solubilité :
- Il est très soluble dans l’eau
- Librement soluble dans l’alcool
- Légèrement soluble dans l’acétone et le chloroforme
- Presque insoluble dans l’éther et le benzène
- Propriétés : Hygroscopique ; se décompose vers 180°C.
- pH : neutre à papier de tournesol.
2.2. Tartrate de choline [87-67-2]
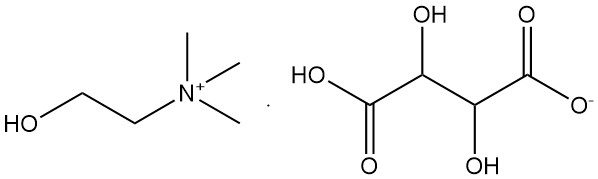
- Formule : C9H19O7N
- Masse molaire : 253,26 g/mol
- Point de fusion : 149 – 153 °C
- Aspect : poudre cristalline blanche au goût acide et à légère odeur d’amine.
- Solubilité :
- Il est très soluble dans l’eau
- Légèrement soluble dans l’alcool
- Presque insoluble dans l’éther, le benzène et le chloroforme
- pH : une solution aqueuse à 25 % a un pH d’environ 3,5.
2.3. Citrate de choline [77-91-8]
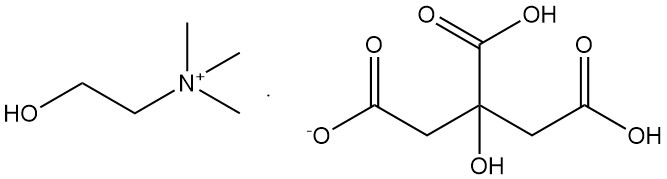
- Formule : C11H21O8N
- Masse molaire : 295,30 g/mol
- Point de fusion : 105 – 107,5 °C
- Apparence : poudre blanche granuleuse à finement cristalline avec une légère odeur d’amine et un goût acide.
- Solubilité :
- Hygroscopique et très soluble dans l’eau
- Soluble dans l’alcool
- Presque insoluble dans l’éther, le benzène et le chloroforme
- pH : une solution aqueuse à 25 % a un pH d’environ 4,3.
2.4. Bicarbonate de Choline [78-73-9]
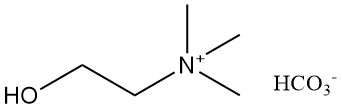
- Formule : C6H15NO4
- Masse molaire : 165,2 g/mol
- Apparence : Liquide clair, incolore à légèrement jaune, avec une odeur caractéristique d’amine.
- Solubilité :
- Il est très soluble dans l’eau
- Librement soluble dans l’alcool
- Légèrement soluble dans le benzène
- pH : la solution aqueuse (bicarbonate de choline à 75 %) a un pH compris entre 9,0 et 11,5.
2.5. Gluconate de Choline [608-59-3]
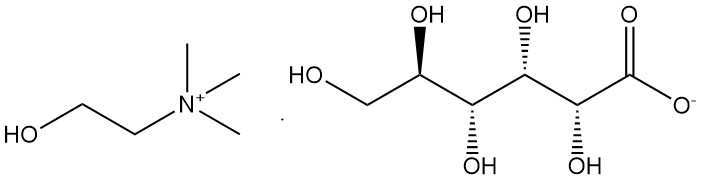
- Formule : C11H25O8N
- Masse molaire : 299,33 g/mol
- Aspect : masse jaune hygroscopique.
- Solubilité :
- Soluble dans l’eau
- Légèrement soluble dans l’éthanol
3. Production de Choline
La choline est principalement produite commercialement par la réaction de la triméthylamine, de l’oxyde d’éthylène et de l’eau. Ce procédé peut être adapté pour produire des sels de choline en incorporant un acide pendant la réaction. La production se produit généralement dans des reacteurs par lots ou en continu.

Des méthodes alternatives de synthèse existent pour la choline, mais cette réaction spécifique reste le procédé industriel dominant en raison de son efficacité et de son évolutivité.
Le chlorure de choline peut être produit par la réaction de la triméthylamine avec la chlorhydrine.
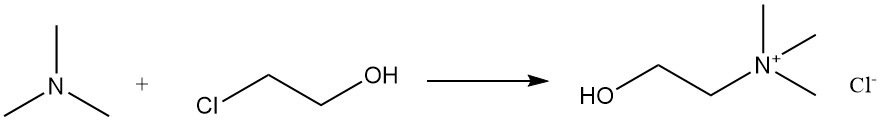
4. Utilisations de la Choline
4.1. Nutrition Animale
La carence en choline chez les animaux domestiques est bien comprise et peut être efficacement évitée grâce à une supplémentation alimentaire en sels de choline.
4.2. Thérapeutique humaine
La recherche en nutrition humaine explore le potentiel de la choline pour soulager diverses maladies. Bien que de nombreuses recherches en soient à leurs débuts, elles sont prometteuses pour une compréhension plus approfondie du rôle de la choline dans la santé humaine.
Les sels de choline comme le chlorure, le tartrate d’hydrogène, le citrate de dihydrogène et le gluconate sont utilisés en thérapeutique chez les patients atteints de cirrhose du foie (stade non fibrotique). L’administration orale de choline semble efficace pour inverser l’infiltration de stéatose hépatique et stopper la progression de la cirrhose.
Le traitement implique généralement un régime faible en gras, riche en protéines et en calories, complété par des vitamines et de la choline. De plus, les sels de choline par voie orale peuvent être utilisés pour répondre à l’apport quotidien recommandé pour les humains.
4.3. Applications pharmacologiques
Plusieurs dérivés de la choline possèdent des propriétés pharmacologiques distinctes :
- L’acétylcholine est utilisée comme vasodilatateur.
- Le chlorure de méthacholine fonctionne comme un stimulant parasympathique et une substance antiépinéphrine.
- Le chlorure de carbamoylcholine améliore la circulation périphérique en cas de vasospasmes causés par des troubles vasculaires périphériques.
4.4. Applications industrielles
La demande croissante d’agents tensioactifs sûrs et efficaces a attiré l’attention sur la choline dans les industries alimentaires et cosmétiques. Des composés d’acylcholine, tels que le chlorure de stéaroylcholine, ont été proposés comme ingrédients dans les revitalisants capillaires.
4.5. Applications agricoles
Le dérivé de choline « chlorure de chlorocholine » est utilisé en agriculture comme régulateur de croissance des plantes, favorisant la compacité des plantes contrairement aux effets accélérateurs de croissance de acide gibbérellique. Il est utilisé pour les plantes ornementales comme les poinsettias et les azalées.
Il est également utilisé pour empêcher la verse et l’aplatissement des cultures de blé liés au vent et dans les serres pour empêcher l’étiolation (allongement dû à une lumière insuffisante) des tomates, conduisant à des rendements de fruits plus précoces et plus importants.
5. Toxicologie de la Choline
La choline présente une faible toxicité inhérente. Des études ont montré que l’administration orale de chlorure de choline chez le rat entraînait une valeur DL50 (dose mortelle, 50 %) comprise entre 3 et 6 grammes par kilogramme de poids corporel.
Cependant, en raison de son fort caractère basique, la choline peut être corrosive pour les tissus par contact direct. Cela nécessite des précautions de manipulation pour éviter les irritations de la peau et des yeux.
Références
- Choline; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a07_039
- Choline; Present Knowledge in Nutrition, Tenth Edition. – https://onlinelibrary.wiley.com/doi/10.1002/9781119946045.ch26
- Choline; Kirk-Othmer Encyclopedia of Chemical Technology. – https://onlinelibrary.wiley.com/doi/10.1002/0471238961.0308151207090404.a01
- Choline: an essential nutrient for public health. – https://onlinelibrary.wiley.com/doi/10.1111/j.1753-4887.2009.00246.x
