Anthracène : production, réactions et utilisations
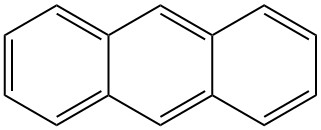
L’anthracène est un hydrocarbure aromatique polycyclique (HAP) solide de formule C14H10, constitué de trois cycles benzéniques condensés. C’est un composant du goudron de houille et a été découvert en 1832 par J. DUMAS et H. A. LAURENT. L’anthracène est incolore mais présente une fluorescence bleue sous rayonnement ultraviolet.
Table des matières
1. Propriétés physiques de l’anthracène
L’anthracène (C14H10 avec un poids moléculaire de 178,24 g/mol) est un solide incolore avec un point de fusion de 218 °C et un point d’ébullition de 340 °C à 101,3 kPa. Il présente une fluorescence bleu-violet et peut se sublimer, ce qui signifie qu’il passe directement d’un solide à une vapeur.
L’anthracène peut former des cristaux mixtes avec le phénanthrène et le carbazole dans des systèmes binaires et ternaires.
L’anthracène a une légère solubilité dans le benzène, le chloroforme et le disulfure de carbone, moins de solubilité dans l’éther diéthylique et l’éthanol et est presque insoluble dans l’eau.
L’anthracène a une capacité thermique spécifique de 1 164 J/kg à 24 °C, une chaleur de fusion de 162 kJ/kg, une chaleur de vaporisation de 294 kJ/kg et une chaleur de combustion de 40 110 kJ/kg à 25 °C. .
2. Réactions chimiques de l’anthracène
L’anthracène peut subir diverses transformations chimiques dans des conditions spécifiques :
1. Irradiation par la lumière UV : Lorsqu’il est exposé à la lumière UV en l’absence d’oxygène, l’anthracène est converti en dianthracène.
2. Oxydation avec l’oxygène : En présence d’oxygène, l’anthracène réagit en ajoutant de l’oxygène aux positions 9,10, entraînant la formation d’un composé peroxyde.

3. Pyrocondensation : Grâce à la pyrocondensation, l’anthracène peut donner deux produits, à savoir le 2,9-bianthryl et le 9,10-dihydroanthracène.
4. Hydrogénation : L’anthracène peut être facilement hydrogéné pour produire du 9,10-dihydroanthracène. En utilisant des catalyseurs homogènes au ruthénium, il peut en outre subir une hydrogénation pour donner du 1,2,3,4-tétrahydroanthracène et une hydrogénation ultérieure peut conduire à la formation de 1,2,3,4,5,6,7,8-octahydroanthracène.

5. Oxydation : Lorsqu’il est soumis à une oxydation, en phase liquide ou gazeuse, l’anthracène se transforme en anthraquinone.
6. Halogénation, nitration et sulfonation : L’anthracène subit principalement une halogénation et une nitration en positions 9 et 10 et une sulfonation en position 1 ou 2, selon les conditions de réaction spécifiques.

7. Addition Diels-Alder : L’anthracène est capable de subir des réactions d’addition Diels-Alder avec des diénophiles tels que l’anhydride maléique. Ces ajouts se produisent généralement aux positions 9 et 10.
8. Réaction avec magnésium : l’anthracène peut réagir avec le magnésium métallique présent dans le tétrahydrofurane (THF) pour former un adduit magnésium-anthracène. Cet adduit peut être traité ultérieurement pour obtenir du magnésium hautement réactif, qui peut ensuite être converti en hydrure de magnésium et en réactifs de Grignard.
Ces réactions chimiques illustrent la polyvalence de l’anthracène dans divers procédés de synthèse et son potentiel de formation de divers composés organiques dans des conditions spécifiques.
3. Production d’anthracène
3.1. Extraction de l’anthracène du goudron de houille
L’anthracène est extrait du goudron de houille à haute température par distillation continue du goudron. La fraction qui bout entre 300 et 360 °C, appelée huile anthracénique I, est concentrée pour contenir environ 7 % d’anthracène.
Cette huile est ensuite refroidie et centrifugée pour produire des résidus d’anthracène, qui contiennent environ 20 à 35 % d’anthracène.
Les résidus anthracènes peuvent être davantage purifiés par cristallisation ou distillation. La distillation produit un produit brut contenant 45 à 55 % d’anthracène, communément appelé « anthracène des années 50 ». L’anthracène des années 50 de qualité améliorée peut être obtenu grâce à un processus de distillation sur colonne continue en deux étapes.
Pour obtenir une pureté plus élevée, l’anthracène brut des années 50 peut être recristallisé à l’aide de solvants sélectifs. Une recristallisation répétée à partir d’un excès de trois à quatre fois de pyridine, par exemple, donne de l’anthracène d’une pureté de 95 % par rapport à sa teneur dans l’anthracène des années 50, avec un rendement de 80 %. Divers autres solvants sélectifs peuvent également être utilisés pour la recristallisation.
3.2. Méthodes d’extraction alternatives
L’anthracène peut également être extrait de l’huile à point d’ébullition élevé issue de la liquéfaction du charbon. Pour l’anthracène brut sans carbazole, la distillation et la cristallisation des résidus de la pyrolyse des fractions d’hydrocarbures en oléfines peuvent être utilisées, bien que ces huiles de pyrolyse contiennent généralement moins de 1 % d’anthracène.
L’hydrodésalkylation sélective de la fraction aromatique contenant des méthylphénanthrènes et des méthylanthracènes peut améliorer les rendements en anthracène.
3.3. Synthèse de l’anthracène
L’anthracène peut également être synthétisé par diverses méthodes, notamment l’hydrogénation du phénanthrène, l’isomérisation du sym-octahydrophénanthrène en sym-octahydroanthracène et la déshydrogénation ultérieure.
Un mélange de sym-octahydroanthracène et de sym-octahydrophénanthrène peut être obtenu par dismutation catalytique de la tétraline.
De plus, de l’anthracène peut être formé à partir du diphénylméthane en présence de HF/BF3 à 80 °C et par réaction thermique de l’o-méthyldiphénylméthane à environ 600 °C.
Cependant, ces méthodes de synthèse ne sont pas significatives sur le plan commercial en raison de la grande disponibilité d’anthracène provenant du goudron de houille.
4. Utilisations de l’anthracène
L’anthracène est un composé organique polyvalent avec une large gamme d’applications. À l’échelle commerciale, il est principalement utilisé pour produire de l’anthraquinone, un produit chimique industriel clé utilisé dans la production de colorants, de pigments et d’autres produits chimiques.
L’anthracène est également à l’étude pour un certain nombre d’applications alternatives. Par exemple, il a été proposé comme plastifiant potentiel pour les résines thermodurcissables et également considéré comme stabilisant à la lumière pour les polymères.
Dans la science des matériaux, les dérivés de l’anthracène sont étudiés comme éléments constitutifs des plastiques techniques. Par exemple, le polyéther du 9,10-dihydroxyanthracène est un plastique haute performance doté d’excellentes propriétés mécaniques et thermiques.
L’anthracène est un photoconducteur organique cristallin, ce qui signifie qu’il peut générer un courant électrique lorsqu’il est exposé à la lumière. Cette propriété rend l’anthracène utile en électrophotographie, une technologie couramment associée à la photocopie et à l’impression laser.
Dans sa forme la plus pure, l’anthracène est utilisé comme scintillant dans les applications scientifiques. Les scintillants sont des matériaux qui émettent de la lumière lorsqu’ils interagissent avec un rayonnement.
Les scintillants anthracènes sont particulièrement utiles pour la détection de rayonnements à haute énergie, tels que les rayons gamma et les rayons X. Cette utilisation est vitale dans des domaines tels que la physique nucléaire, où la mesure précise des rayonnements est de la plus haute importance pour la recherche et la sécurité.
5. Toxicologie de l’anthracène
L’anthracène est un hydrocarbure aromatique polycyclique dont la cancérogénicité potentielle a été étudiée, mais l’anthracène pur dans des conditions contrôlées ne présente pas d’effets cancérigènes significatifs. Ceci est étayé par les résultats négatifs de nombreux tests de génotoxicité in vitro et in vivo.
Par exemple, des injections sous-cutanées de 20 mg d’anthracène dans une solution huileuse 33 fois par semaine ont entraîné l’apparition de fibromes locaux, parfois accompagnés d’excroissances ressemblant à des sarcomes. Toutefois, ce résultat ne reflète pas le potentiel cancérigène de l’anthracène pur.
De plus, un test d’initiation de tumeur épidermique sur des souris utilisant de l’anthracène pur et de l’ester de phorbol comme promoteur n’a abouti à des papillomes que dans quelques cas (4 animaux sur 28). Ces occurrences limitées n’établissent pas de lien cancérogène fort pour l’anthracène pur.
Par conséquent, le Centre international de recherche sur le cancer (CIRC) et l’Agence américaine de protection de l’environnement (EPA) ont classé l’anthracène comme « inclassable quant à sa cancérogénicité pour l’homme » (catégorie 3 du CIRC et groupe D de l’EPA).
En termes de toxicité aiguë, l’administration orale de 1,7 g/kg d’anthracène pur à des souris n’a eu aucun effet mortel.
L’anthracène est également absorbé par la peau. Lorsqu’une solution marquée au 14C dans de l’hexane ou de l’acétone (environ 9 mg/cm3) était appliquée localement sur la peau de rat, environ 50 % étaient absorbés en 6 jours, dont 29 % étaient récupérés dans l’urine, 22 % dans les selles et 1 % dans divers tissus, principalement le foie et les reins. Après seulement 1 jour, 20 % de la dose était déjà présente dans les urines (environ 17 %) et les selles (environ 3 %).
L’anthracène est un sensibilisant cutané et peut provoquer une photosensibilité locale. Par mesure de sécurité, une valeur limite seuil (TLV) recommandée de 0,1 mg/m3 a été proposée pour minimiser les problèmes d’exposition potentiels.
Référence
- Anthracene; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_343.pub2
