Antraceno: Producción, Reacciones y Usos
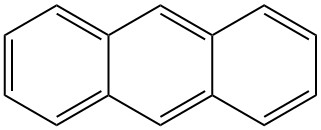
El antraceno es un hidrocarburo aromático policíclico (PAH) sólido de fórmula C14H10, que consta de tres anillos de benceno fusionados. Es un componente del alquitrán de hulla y fue descubierto en 1832 por J. DUMAS y H. A. LAURENT. El antraceno es incoloro pero exhibe una fluorescencia azul bajo la radiación ultravioleta.
Tabla de contenido
1. Propiedades físicas del antraceno
El antraceno (C14H10 con un peso molecular de 178,24 g/mol) es un sólido incoloro con un punto de fusión de 218 °C y un punto de ebullición de 340 °C a 101,3 kPa. Exhibe una fluorescencia azul violeta y puede sublimar, lo que significa que pasa directamente de sólido a vapor.
El antraceno puede formar cristales mixtos con fenantreno y carbazol en sistemas binarios y ternarios.
El antraceno tiene ligera solubilidad en benceno, cloroformo y disulfuro de carbono, menos solubilidad en éter dietílico y etanol y es casi insoluble en agua.
El antraceno tiene una capacidad calorífica específica de 1164 J/kg a 24 °C, un calor de fusión de 162 kJ/kg, un calor de vaporización de 294 kJ/kg y un calor de combustión de 40110 kJ/kg a 25 °C. .
2. Reacciones químicas del antraceno
El antraceno puede sufrir diversas transformaciones químicas en condiciones específicas:
1. Irradiación con luz ultravioleta: cuando se expone a la luz ultravioleta en ausencia de oxígeno, el antraceno se convierte en diantraceno.
2. Oxidación con oxígeno: en presencia de oxígeno, el antraceno reacciona añadiendo oxígeno a las posiciones 9,10, lo que da como resultado la formación de un compuesto de peróxido.

3. Pirocondensación: mediante pirocondensación, el antraceno puede producir dos productos, a saber, 2,9-biantrilo y 9,10-dihidroantraceno.
4. Hidrogenación: El antraceno se puede hidrogenar fácilmente para producir 9,10-dihidroantraceno. Usando catalizadores de rutenio homogéneos, puede sufrir una hidrogenación adicional para producir 1,2,3,4-tetrahidroantraceno y la hidrogenación posterior puede conducir a la formación de 1,2,3,4,5,6,7,8-octahidroantraceno.

5. Oxidación: Cuando se somete a oxidación, ya sea en fase líquida o gaseosa, el antraceno se transforma en antraquinona.
6. Halogenación, nitración y sulfonación: el antraceno sufre principalmente halogenación y nitración en las posiciones 9 y 10 y sulfonación en las posiciones 1 o 2, dependiendo de las condiciones de reacción específicas.

7. Adición de Diels-Alder: El antraceno es capaz de sufrir reacciones de adición de Diels-Alder con dienófilos como el anhídrido maleico. Estas adiciones suelen ocurrir en las posiciones 9 y 10.
8. Reacción del magnesio: El antraceno puede reaccionar con magnesio metálico en tetrahidrofurano (THF) para formar un aducto de magnesio-antraceno. Este aducto se puede procesar adicionalmente para obtener magnesio altamente reactivo, que posteriormente se puede convertir en hidruro de magnesio y reactivos de Grignard.
Estas reacciones químicas ilustran la versatilidad del antraceno en diversos procesos sintéticos y su potencial para formar diversos compuestos orgánicos en condiciones específicas.
3. Producción de antraceno
3.1. Extracción de antraceno del alquitrán de hulla
El antraceno se extrae del alquitrán de hulla a alta temperatura mediante destilación continua de alquitrán. La fracción que hierve entre 300 y 360 °C, conocida como aceite de antraceno I, se concentra para contener aproximadamente un 7% de antraceno.
Luego, este aceite se enfría y se centrifuga para producir residuos de antraceno, que contienen aproximadamente entre un 20 y un 35 % de antraceno.
Los residuos de antraceno se pueden purificar aún más mediante cristalización o destilación. La destilación produce un producto crudo que contiene entre un 45% y un 55% de antraceno, comúnmente conocido como «antraceno de los años 50». El antraceno 50 de calidad mejorada se puede obtener mediante un proceso de destilación en columna continua de dos pasos.
Para lograr una mayor pureza, el antraceno 50 en bruto se puede recristalizar utilizando disolventes selectivos. La recristalización repetida a partir de un exceso de piridina de tres a cuatro veces, por ejemplo, produce antraceno con una pureza del 95% en relación con su contenido en el antraceno 50, con un rendimiento del 80%. También se pueden utilizar otros diversos disolventes selectivos para la recristalización.
3.2. Métodos de extracción alternativos
El antraceno también se puede extraer del aceite de alto punto de ebullición procedente de la licuefacción del carbón. Para el antraceno crudo sin carbazol, se puede utilizar la destilación y cristalización de residuos de la pirólisis de fracciones de hidrocarburos en olefinas, aunque estos aceites de pirólisis normalmente contienen menos del 1% de antraceno.
La hidrodesalquilación selectiva de la fracción aromática que contiene metilfenantrenos y metilantracenos puede mejorar los rendimientos de antraceno.
3.3. Síntesis de antraceno
El antraceno también se puede sintetizar mediante varios métodos, incluida la hidrogenación de fenantreno, la isomerización de sim-octahidrofenantreno a sim-octahidroantraceno y la deshidrogenación posterior.
Se puede obtener una mezcla de sim-octahidroantraceno y sim-octahidrofenantreno mediante desproporción catalítica de tetralina.
Además, el antraceno se puede formar a partir de difenilmetano en presencia de HF/BF3 a 80 °C y mediante la reacción térmica de o-metildifenilmetano a aproximadamente 600 °C.
Sin embargo, estos métodos sintéticos no son comercialmente significativos debido a la amplia disponibilidad de antraceno del alquitrán de hulla.
4. Usos del antraceno
El antraceno es un compuesto orgánico versátil con una amplia gama de aplicaciones. A escala comercial, se utiliza principalmente para producir antraquinona, una sustancia química industrial clave utilizada en la producción de tintes, pigmentos y otras sustancias químicas.
El antraceno también se está explorando para una serie de aplicaciones alternativas. Por ejemplo, se ha propuesto como plastificante potencial para resinas termoestables y también se ha considerado como estabilizador de luz para polímeros.
En la ciencia de los materiales se exploran los derivados del antraceno como componentes básicos para los plásticos técnicos. Por ejemplo, el poliéter de 9,10-dihidroxiantraceno es un plástico de alto rendimiento con excelentes propiedades mecánicas y térmicas.
El antraceno es un fotoconductor orgánico cristalino, lo que significa que puede generar una corriente eléctrica cuando se expone a la luz. Esta propiedad hace que el antraceno sea útil en electrofotografía, una tecnología comúnmente asociada con el fotocopiado y la impresión láser.
En su forma más pura, el antraceno se utiliza como centelleante en aplicaciones científicas. Los centelleantes son materiales que emiten luz cuando interactúan con la radiación.
Los centelleantes de antraceno son particularmente útiles para la detección de radiaciones de alta energía, como los rayos gamma y los rayos X. Este uso es vital en campos como la física nuclear, donde la medición precisa de la radiación es de suma importancia para fines de investigación y seguridad.
5. Toxicología del antraceno
El antraceno es un hidrocarburo aromático policíclico que ha sido investigado por su potencial carcinógeno, pero el antraceno puro en condiciones controladas no presenta efectos cancerígenos significativos. Esto está respaldado por resultados negativos en numerosas pruebas de genotoxicidad in vitro e in vivo.
Por ejemplo, las inyecciones subcutáneas de 20 mg de antraceno en una solución oleosa 33 veces por semana dieron como resultado fibromas locales, a veces acompañados de excrecencias similares a sarcomas. Sin embargo, este resultado no refleja el potencial cancerígeno del antraceno puro.
Además, una prueba de iniciación de tumores epidérmicos en ratones utilizando antraceno puro y éster de forbol como promotor sólo dio como resultado papilomas en unos pocos casos (4 de 28 animales). Estos casos limitados no establecen un fuerte vínculo cancerígeno para el antraceno puro.
Por lo tanto, la Agencia Internacional para la Investigación del Cáncer (IARC) y la Agencia de Protección Ambiental de EE. UU. (EPA) han categorizado el antraceno como «no clasificable en cuanto a su carcinogenicidad para los humanos» (Categoría 3 de la IARC y Grupo D de la EPA).
En términos de toxicidad aguda, la administración oral de 1,7 g/kg de antraceno puro a ratones no tuvo efectos letales.
El antraceno también se absorbe a través de la piel. Cuando se aplicó tópicamente una solución marcada con 14C en hexano o acetona (aproximadamente 9 mg/cm3) sobre la piel de rata, aproximadamente el 50% se absorbió en 6 días, y el 29% se recuperó de la orina, el 22% de las heces y el 1% de diversos tejidos, principalmente el hígado y los riñones. Después de sólo 1 día, el 20% de la dosis ya estaba presente en la orina (alrededor del 17%) y las heces (alrededor del 3%).
El antraceno es un sensibilizador de la piel y puede causar fotosensibilidad local. Como medida de seguridad, se ha propuesto un valor límite umbral (TLV) recomendado de 0,1 mg/m3 para minimizar los posibles problemas de exposición.
Referencia
- Anthracene; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_343.pub2
