Acide acrylique : réactions, production et utilisations
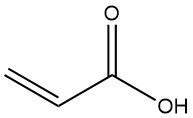
L’acide acrylique, également connu sous le nom d’acide 2-propénoïque, est l’acide carboxylique insaturé le plus simple de formule CH2=CHCOOH. C’est un liquide incolore, inflammable, volatil et légèrement toxique.
Pour empêcher la polymérisation, les préparations commerciales incorporent généralement de l’hydroquinone ou son éther monométhylique.
Dans le passé, la production industrielle d’acide acrylique impliquait diverses méthodes telles que l’hydrolyse de l’acrylonitrile et le procédé Reppe modifié. Cependant, des progrès significatifs dans l’oxydation catalytique, en particulier dans la conversion du propène en acide acrylique via l’acroléine, ont presque entièrement supplanté ces techniques précédentes.
Table des matières
1. Propriétés physiques de l’acide acrylique
L’acide acrylique est un liquide transparent et incolore avec un point d’ébullition de 141,0 °C à 101,3 kPa et un point de fusion de 13,5 °C, formant des aiguilles cristallines lorsqu’il est solidifié.
Il présente une miscibilité élevée avec l’eau, les alcools, les esters et divers autres solvants organiques, ce qui le rend facilement soluble dans ces substances.
D’autres propriétés physiques importantes sont énumérées ci-dessous :
| Propriété | Valeur |
|---|---|
| Masse molaire (Mr) | 72,06 g/mol |
| Indice de réfraction | 1.421 |
| Densité | 1,05 g/cm³ |
| Viscosité | 1,15 mPa.s (à 25°C) |
| Température critique | 380 °C |
| Pression critique | 5,06 Mpa |
| Constante de dissociation | 5,46 x 10-5 (à 25 °C) |
| pKa | 4.25 |
2. Réactions chimiques de l’acide acrylique
L’acide acrylique présente des réactions distinctes caractéristiques à la fois des composés insaturés et des acides carboxyliques aliphatiques. Sa grande réactivité peut être attribuée à la présence de deux centres insaturés en position conjuguée.
L’atome de carbone β, polarisé par le groupe carbonyle, agit comme un électrophile, permettant l’addition de divers nucléophiles et composés à hydrogène actif au groupe vinyle.
De plus, la double liaison carbone-carbone participe aux réactions d’addition initiées par les radicaux, aux réactions de Diels-Alder avec les diènes et aux réactions de polymérisation.
Quant à la fonction carboxyle, elle subit des réactions de déplacement typiques des acides aliphatiques, telles que l’estérification.
Lorsque les fonctions vinyle et carboxyle réagissent conjointement, en particulier avec des réactifs bifonctionnels, elles forment des substances polycycliques et hétérocycliques.
L’acide acrylique subit facilement une polymérisation, qui peut être catalysée par la chaleur, la lumière et les peroxydes, mais inhibée par des stabilisants comme l’éther monométhylique de l’hydroquinone ou l’hydroquinone elle-même.
Notamment, ces inhibiteurs phénoliques ne sont efficaces qu’en présence d’oxygène. Le processus de polymérisation de l’acide acrylique est hautement exothermique et peut être extrêmement vigoureux.
2.1. Réactions d’addition
L’acide acrylique subit facilement des réactions d’addition avec diverses substances, telles que l’hydrogène, les halogénures d’hydrogène et le cyanure d’hydrogène, qui sont couramment ajoutés aux oléfines :
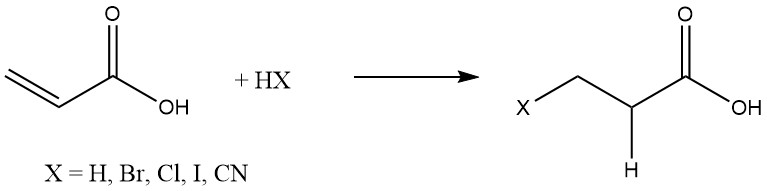
Les additions de Michael de substances organiques se produisent en présence de catalyseurs basiques comme les amines tertiaires, les sels d’ammonium quaternaire et les alcoolates alcalins.
L’ammoniac et les amines, étant suffisamment basiques, peuvent réagir sans avoir besoin d’un catalyseur. L’ajout d’une seule molécule de NH3 peut être réalisé à l’aide d’une solution aqueuse d’ammoniac et de carbonate d’ammonium.
L’addition d’amines ou d’amides aromatiques et d’amines primaires tert-alkyles est favorisée plus efficacement par les acides. Les amines peuvent attaquer à la fois les fonctions vinyle et carboxyle, mais les produits résultant de ces réactions se décomposent pour donner des amides N-substitués.
Dans des conditions basiques, les alcools, les phénols, le sulfure d’hydrogène et les thiols subissent également des réactions d’addition. Le sulfure d’hydrogène, lorsqu’il est combiné avec du soufre et du polysulfure d’ammonium ou des catalyseurs amine, donne des acides polythiodipropioniques. Pendant ce temps, les ajouts d’hydrocarbures aromatiques sont favorisés plus efficacement par les acides de Lewis.
Si des atomes d’hydrogène acides supplémentaires sont disponibles dans le produit d’addition, une deuxième (et troisième) molécule d’acide acrylique peut s’ajouter. Cela se produit lors de la réaction de l’acide acrylique avec H2S, NH3, RNH2 et le pyrrole.
Les substances hétérocycliques sont souvent formées par des réactions ultérieures de la fonction carboxyle, en particulier avec des nucléophiles bifonctionnels :
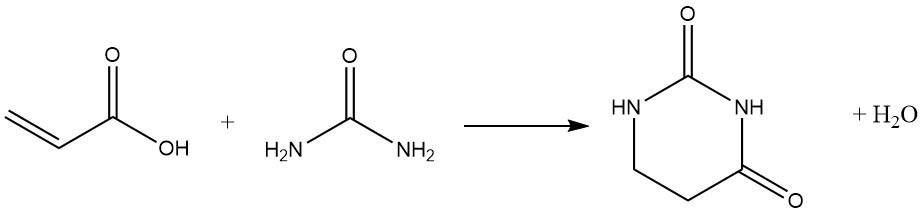
A des températures élevées ou lors d’un stockage prolongé, l’acide acrylique se dimérise :
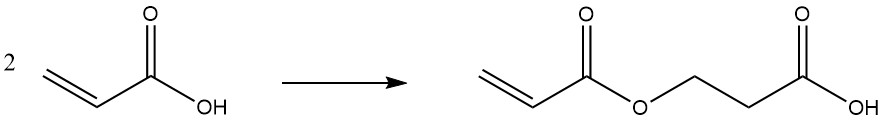
2.2. Réactions du groupe carboxyle
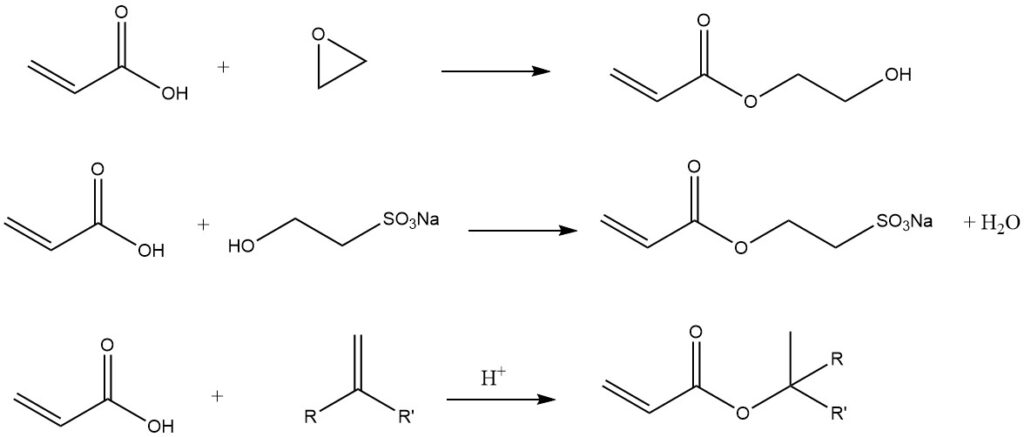
L’acide acrylique peut être facilement converti en ses sels correspondants, transformé en anhydride acrylique par réaction avec l’anhydride acétique, ou converti en chlorure d’acryloyle par réaction avec le chlorure de benzoyle ou de thionyle. L’estérification de l’acide acrylique et la transestérification des esters acryliques sont des réactions économiquement importantes.
Quelques autres exemples des reactions de groupe carboxylique sont :
3. Production d’acide acrylique
L’acide acrylique commercial est principalement produit à partir de propène, qui est également utilisé comme matière première pour la production d’acroléine. Dans le passé, divers procédés étaient utilisés pour la production d’acide acrylique et de ses esters, dont certains sont encore utilisés dans une mesure limitée.
1. Procédés à base d’acétylène :
L’acide acrylique et ses esters peuvent être synthétisés à partir d’acétylène en présence d’acide et de nickel carbonyle à pression atmosphérique et 40°C :
4 C2H2 + 4 ROH + 2 HCl + Ni(CO)4 → 4 H2C=CHCOOR + NiCl2 + H2
Cependant, cette méthode a été abandonnée en raison des défis associés à la manipulation de nickel carbonyle toxique et corrosif.
2. Processus Reppe à haute pression :
BASF a utilisé un procédé utilisant un catalyseur au bromure de nickel-bromure de cuivre (II) à environ 14 MPa et 200 ° C pour produire de l’acide acrylique à partir d’acétylène, de CO et d’eau. Néanmoins, ce procédé a été remplacé par l’oxydation directe plus économique du propène.
3. Hydrolyse de l’acrylonitrile :
Cette méthode, qui implique l’hydrolyse de l’acrylonitrile, s’est avérée économiquement peu attrayante en raison du faible rendement et des grandes quantités de déchets NH4HSO4. Certaines entreprises ont abandonné ce procédé, à l’exception d’Asahi Chemical qui l’utilise toujours.
4. Processus Ketene :
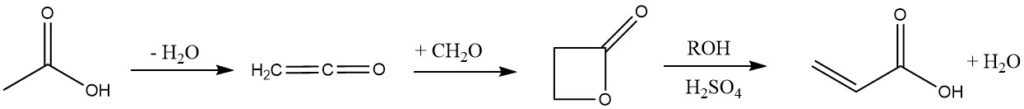
Dans ce processus, l’acide acétique ou l’acétone est pyrolysé en cétène, mais il a été abandonné par des sociétés comme Celanese et BF Goodrich en raison de ses nombreuses étapes et de la toxicité de la β-propiolactone.
5. Dépolymérisation thermique de Polypropiolactone :
Novomer a développé des catalyseurs exclusifs pour produire de la polypropiolactone (PPL) en tant qu’intermédiaire pouvant être dépolymérisé thermiquement en acide acrylique ou en esters d’acrylate, répondant aux défis du transport et réduisant la complexité de la fabrication.
6. Processus d’éthylène cyanhydrine :
La cyanohydrine d’éthylène est générée en ajoutant du cyanure d’hydrogène à l’oxyde d’éthylène, puis déshydratée catalytiquement pour produire de l’acide acrylique à l’aide d’acide sulfurique. Ce procédé a été utilisé par Union Carbide et Rohm & Haas mais a été abandonné en raison de difficultés de traitement des déchets HCN et NH4HSO4.
7. Oxydation partielle de l’éther allylique :
Un système catalytique à base d’oxyde de manganèse mésoporeux dopé Li peut catalyser l’oxydation partielle aérobie de l’éther diallylique en acrylate d’allyle dans des conditions ambiantes dans un solvant acétonitrile.
3.1. Production d’acide acrylique par oxydation du propène
La production d’acide acrylique à partir de propène implique une oxydation catalytique hétérogène en phase vapeur, utilisant de l’air et de la vapeur. Le produit résultant est généralement absorbé dans l’eau, suivi d’une extraction avec un solvant approprié, puis distillé pour obtenir de l’acide acrylique glacial de qualité technique.
La recherche sur les catalyseurs pour l’oxydation du propène en acide acrylique a commencé à la fin des années 1950, avec deux méthodes d’oxydation en phase gazeuse catalysée de manière hétérogène du propène : les procédés en une étape et en deux étapes.
Dans le procédé en une seule étape, le rendement est limité, environ 50-60 % au mieux, et la durée de vie du catalyseur est courte en raison de la présence d’oxyde de tellure, qui a tendance à se sublimer.
Le procédé en deux étapes implique des conditions de réaction et des catalyseurs différents pour obtenir une conversion et une sélectivité optimales à chaque étape. Les catalyseurs de première étape sont utilisés pour l’oxydation sélective du propène à l’acroléine, produisant plus de 85% d’acroléine et d’acide acrylique.
Les premiers catalyseurs de deuxième étape pour l’oxydation de l’acroléine en acide acrylique étaient principalement basés sur des oxydes de cobalt-molybdène, offrant des rendements inférieurs à 70 % en moles. Cependant, d’autres recherches ont montré que divers catalyseurs à base d’oxydes métalliques à plusieurs composants, notamment le molybdène et le vanadium, ainsi que d’autres éléments et supports, pouvaient augmenter l’activité et le rendement.
La récupération et la purification de l’acide consistent à refroidir le gaz effluent et à le laver avec de l’eau pour obtenir une solution aqueuse d’acide acrylique. Cette solution est ensuite purifiée par extraction avec un solvant organique, distillation et addition d’inhibiteur pour empêcher la polymérisation pendant la distillation. La pureté de l’acide acrylique résultant dépasse généralement 99,5 % en poids, avec un rendement purifié d’environ 98 %.
Différentes méthodes de purification, telles que l’oligomérisation et l’estérification directe, ont été explorées, mais le procédé d’extraction par solvant léger reste le plus adapté aux usines commerciales en raison de son efficacité énergétique et de la qualité du produit. D’autres méthodes n’ont pas été largement adoptées commercialement en raison de leur forte consommation d’énergie ou des problèmes de qualité des produits.
3.2. Acide Acrylique Biosourcé
Les technologies biosourcées pour la production d’acide acrylique impliquent la fermentation de substances dérivées de la biomasse, telles que les sucres, pour produire de l’acide lactique, de l’acide 3-hydroxypropanoïque et du 3-hydroxypropanal. Par la suite, ces intermédiaires de fermentation subissent une transformation chimique pour donner de l’acide acrylique.
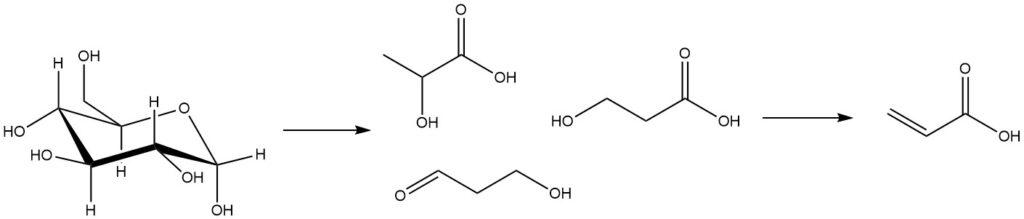
La déshydratation de l’acide lactique intermédiaire se produit généralement par acétoxylation, où l’acide acétique est utilisé comme solvant azéotropique.
De 2008 à 2010, plusieurs technologies biosourcées pour la production d’acide acrylique ont été lancées, utilisant des matières premières comme le glucose, le glycol, l’acide lactique et la biomasse.
Des coentreprises et des sociétés individuelles, telles que Cargill/Novozymes/BASF, OPXBio/Dow, Arkema/THE, Nippon Shokubai, Geneomatica et Choren, ont été activement impliquées dans le développement de ces technologies. Certaines de ces approches devraient être commercialisées d’ici 2025.
Diverses coentreprises, dont Cargill/Novozymes/BASF et OPXBio/Dow, se concentrent sur l’ingénierie d’enzymes ou de micro-organismes pour produire de l’acide acrylique à partir de matières premières renouvelables comme le maïs et la canne à sucre.
Arkema, en partenariat avec HTE, travaille au développement de catalyseurs de production d’acide acrylique à partir de glycérol via l’acroléine. Nippon Shokubai explore un procédé en phase gazeuse pour produire de l’acide acrylique à partir de glycérol obtenu comme sous-produit de la production de biodiesel à partir d’huiles végétales. Le potentiel de commercialisation de ces procédés dépend de la disponibilité et du prix du glycérol.
L’approche de Genomatica implique la fermentation du sucre en acide fumarique, suivie d’une métathèse croisée avec l’éthylène pour produire de l’acide acrylique. Bien que cette technologie ait été brevetée, il reste encore d’importants défis techniques à surmonter.
Le progrès et le succès de ces biotechnologies dépendront non seulement des avancées technologiques, mais aussi des pressions et des demandes sociétales pour produire des biens et des produits chimiques à partir de sources renouvelables et durables.
4. Utilisations de l’acide acrylique
L’acide acrylique sert d’intermédiaire dans la production d’acrylates. Les acrylates sont un groupe de composés dérivés de l’acide acrylique et sont largement utilisés dans diverses industries pour leur polyvalence et leurs propriétés de performance.
De plus, l’acide acrylique et ses sels de sodium trouvent des applications croissantes en tant que floculants et dispersants. Ces formes polymères d’acide acrylique, en particulier les sels de sodium polymères, gagnent en importance industrielle en raison de leurs propriétés efficaces pour favoriser la floculation (agglutination des particules) et la dispersion (répartition uniforme des particules) dans divers procédés et applications.
En 2014, les capacités de production mondiales d’acide acrylique et de ses esters étaient respectivement de plus de 5,2 millions de tonnes par an et de 3,6 millions de tonnes par an.
La Chine est devenue un marché à forte croissance pour l’acide acrylique, dépassant la demande combinée en Amérique du Nord et en Europe. Entre 2002 et 2014, la capacité de production d’acide acrylique de la Chine a presque quadruplé, indiquant son rôle important dans l’industrie.
En 2014, 50 % de la consommation totale d’acide acrylique ont été utilisés comme intermédiaire dans la production d’esters, tandis que les 50 % restants ont été transformés pour produire de l’acide acétique glacial.
5. Toxicologie et santé au travail
L’acide acrylique est modérément toxique et hautement corrosif. L’ingestion peut entraîner de graves brûlures gastro-intestinales et ses vapeurs sont irritantes pour les yeux et les voies respiratoires. Le contact avec la peau peut provoquer des brûlures. Les données de réponse physiologique suivantes sont disponibles :
– LD50 : 340 mg/kg (rat, voie orale)
– CL50 : 3600 mg/m3 (rat, inhalation, 5 L, 4 heures)
– LD50 : 280 mg/kg (lapin, peau)
La valeur limite d’exposition (TLV) pour l’acide acrylique sur une moyenne pondérée dans le temps (TWA) est fixée à 10 ppm (parties par million) ou 30 mg/m3. Cette valeur sert de ligne directrice pour contrôler les niveaux d’exposition en milieu de travail.
Référence
- Acrylic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_161.pub4
Questions fréquemment posées (FAQ) sur l’acide acrylique
L’acide acrylique est un composé organique liquide incolore de formule chimique CH2=CHCOOH. Il appartient à la famille des acides carboxyliques insaturés et a une odeur forte et piquante. L’acide acrylique est hautement réactif en raison de la présence de deux centres insaturés, ce qui en fait un élément essentiel pour divers processus chimiques et polymérisations.
L’acide acrylique est principalement utilisé comme intermédiaire dans la production d’acrylates, un groupe polyvalent de composés largement utilisé dans la fabrication de peintures, d’adhésifs, de revêtements et de polymères superabsorbants. De plus, l’acide acrylique et ses sels de sodium sont utilisés comme floculants et dispersants dans diverses applications industrielles.
L’acide acrylique est généralement produit par l’oxydation catalytique du propène en phase vapeur, en utilisant de l’air et de la vapeur. Le processus en deux étapes implique l’oxydation du propène en acroléine, suivie de la poursuite de l’oxydation de l’acroléine en acide acrylique.
Le polymère d’acide acrylique fait référence au produit de polymérisation de l’acide acrylique. Il est communément appelé acide polyacrylique (PAA) lorsqu’il est sous sa forme soluble ou polyacrylate de sodium lorsqu’il est sous sa forme de sel de sodium. Ces polymères sont solubles dans l’eau et possèdent d’excellentes propriétés de floculation et de dispersion, ce qui les rend précieux dans des applications telles que le traitement des eaux usées, les formulations détergentes et les produits de soins personnels.
L’acide acrylique est considéré comme un acide faible. Dans sa forme pure, il présente des propriétés acides, mais sa force est relativement inférieure à celle des acides minéraux forts comme l’acide sulfurique ou l’acide chlorhydrique. Dans les solutions aqueuses, l’acide acrylique se dissocie partiellement pour libérer des ions hydrogène, lui conférant un comportement acide caractéristique.
