Métodos de producción de alcoholes alifáticos
Industrialmente, varios alcoholes vitales tienen una importancia significativa. Estos incluyen metanol, etanol, 1-propanol, 1-butanol y 2-metil-1-propanol (también conocido como alcohol isobutílico).
Además, los alcoholes plastificantes (que van de C6 a C11) y los alcoholes grasos (C12 a C18) se utilizan ampliamente en la producción de detergentes. Estos alcoholes se obtienen principalmente mediante diferentes procesos: gas de síntesis (metanol), oxosíntesis de olefinas o el proceso de Ziegler.
Además de las aplicaciones mencionadas, los alcoholes sirven como disolventes y diluyentes eficaces para pinturas, utilizando principalmente alcoholes C1-C6. También actúan como intermediarios esenciales en la producción de ésteres y diversos compuestos orgánicos. Los alcoholes encuentran aplicaciones como agentes de flotación, lubricantes y aditivos para combustibles, incluidos metanol, etanol y alcohol terc-butílico.
Para aplicaciones industriales, a menudo se prefieren las mezclas isoméricas debido a consideraciones de costo, ya que los alcoholes puros pueden ser costosos. Además, las mezclas con números de átomos de carbono variables pueden ofrecer ventajas para propósitos específicos. De este modo, la disponibilidad en el mercado de mezclas de alcoholes es comparable a la de los alcoholes individuales puros.
Tabla de contenido
Introducción
La producción de alcoholes alifáticos se produce mediante diversos procesos industriales, algunos de los cuales se enumeran a continuación:
- Síntesis a partir de monóxido de carbono e hidrógeno (C1)
- Síntesis de oxo, a menudo acompañada de hidrogenación de aldehídos inicialmente formados (C3 – C20)
- Hidrogenación de aldehídos, ácidos carboxílicos o ésteres.
- Condensación aldólica de aldehídos inferiores seguida de hidrogenación de los alquenales (C3 → C6, C4 → C8, C8 → C16)
- Oxidación de compuestos de trialquilaluminio (proceso Ziegler)
- Oxidación de hidrocarburos saturados.
- Hidratación de olefinas (C2-C4)
- Homologación de alcoholes.
- Hidrocarbonilación por el proceso de Reppe.
- hidrocarboximetilación
- Procesos de fermentación (C2-C5)
- proceso Guerbet
Entre estos procesos, la síntesis de metanol y etanol es de suma importancia, con producciones anuales de aproximadamente 49 × 106 t y 99 × 106 t, respectivamente. La síntesis oxo también tiene una importante relevancia industrial, ya que representa alrededor de 6,3 × 106 t de producción anual.
Además, la hidratación de etileno y propeno para producir etanol y 2-propanol, así como la oxidación de compuestos de trialquilaluminio (proceso Alfol o proceso Ziegler), han adquirido una importancia comercial sustancial.
Además, los procesos de fermentación, especialmente para la producción de etanol, han recuperado importancia en determinadas regiones debido al aumento de los precios del petróleo.
1. Síntesis de monóxido de carbono e hidrógeno
Sólo el metanol se produce comercialmente a partir de gas de síntesis. En el pasado se utilizaban procesos como Synol, isobutilol y oxyl, lo que daba lugar a mezclas de compuestos que contienen oxígeno y con alcoholes como componentes principales. Sin embargo, estos métodos ya no se utilizan en el mundo occidental. Los desarrollos más recientes generan compuestos que contienen oxígeno o mezclas de alcoholes.
Uno de esos procesos es el método IFP (Inst. Français du Pétrole) para alcoholes superiores. Emplea catalizadores altamente activados en condiciones de síntesis de metanol a baja presión. El catalizador está formado por óxidos mixtos de cobre y cobalto, combinados con al menos otro metal (Al, Ce, Cr, Fe, La, Mn, Pr, Nd, Y o Zn), así como al menos un grupo I o II compuesto metálico.
Al ajustar la composición del catalizador, el mayor contenido de alcohol en el producto se puede variar entre 20 y 50% en peso. Sin embargo, este proceso da como resultado la formación de varios subproductos, como hidrocarburos, ésteres y cetonas.
A pesar de estos avances, ninguno de los procesos más nuevos mencionados anteriormente se emplea actualmente en la industria. Sin embargo, en la síntesis de Fischer-Tropsch se producen pequeñas cantidades de alcoholes superiores como subproductos.
2. Oxo Síntesis
La oxosíntesis es un método utilizado para preparar alcoholes en el rango de C3 a C20. En este proceso, las olefinas (hidrocarburos insaturados) reaccionan con el gas de síntesis (una mezcla de monóxido de carbono e hidrógeno) para formar aldehídos. Posteriormente, estos aldehídos se hidrogenan para producir los alcoholes deseados.
Una versión específica de la oxosíntesis se conoce como proceso Shell, que emplea el catalizador HCo(CO)3PR3, que exhibe una fuerte actividad hidrogenante. Este catalizador facilita la hidrogenación directa del aldehído formado inicialmente dentro del oxorreactor.

El proceso Shell se aplicó comercialmente por primera vez utilizando propeno en 1963 para la producción de 1-butanol y 2-etilhexanol. Posteriormente, en 1965, se desarrolló aún más para fabricar alcoholes detergentes. Su principal aplicación es en la producción de alcoholes superiores.
Una ventaja significativa del proceso Shell es su capacidad para hidroformilar olefinas con dobles enlaces internos. Las condiciones de reacción promueven la isomerización del doble enlace, lo que conduce a la formación de α-olefinas.
Por ejemplo, las fracciones de ω-olefina obtenidas a partir de etileno mediante el «proceso SHOP» de Shell se pueden convertir en alcoholes utilizando gas de síntesis. Las mezclas de alcohol resultantes constan de hasta un 80% de compuestos lineales y se utilizan en las industrias de plastificantes y detergentes.
3. Hidrogenación de aldehídos, ácidos carboxílicos y ésteres
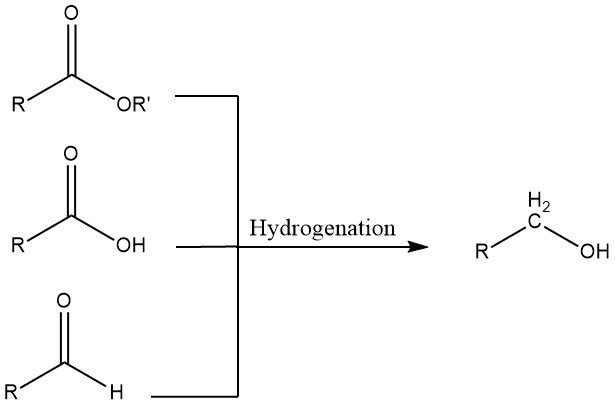
Los aldehídos pueden sufrir hidrogenación utilizando catalizadores homogéneos o heterogéneos. Los sistemas homogéneos son ventajosos cuando los materiales de partida contienen azufre, que envenenaría los catalizadores heterogéneos, o cuando el hidrógeno utilizado para la hidrogenación contiene monóxido de carbono.
Sin embargo, en la mayoría de los casos se prefieren catalizadores heterogéneos. Estos catalizadores son eficaces tanto en reacciones en fase gaseosa a temperaturas de 90 a 180 °C y presiones de 25 bar, como en reacciones en fase líquida a 80 a 220 °C y presiones de hasta 300 bar. La temperatura de hidrogenación utilizada en los procesos industriales se elige como un compromiso entre la utilización óptima de la energía y una larga vida útil del catalizador.
Para procesos continuos, se prefieren los sistemas de lecho fijo con catalizadores. El aldehído, ya sea en forma de vapor diluido con un exceso de hidrógeno o en forma líquida con hidrógeno, se hace pasar a través del tubo de alta presión que contiene el lecho de catalizador.
Para disipar el calor generado por la reacción, se hace circular hidrógeno a través de un intercambiador de calor. La hidrogenación de 2-etil-2-hexenal, una reacción especialmente importante, normalmente se lleva a cabo en un solo paso utilizando un catalizador que contiene níquel.
Se han propuesto procesos similares de un solo paso. Sin embargo, también son comunes los procesos de dos pasos, donde la hidrogenación primaria ocurre en la fase gaseosa (por ejemplo, usando catalizadores que contienen cobre) y la hidrogenación secundaria ocurre en la fase líquida o proceso de lecho percolador (por ejemplo, con catalizadores que contienen níquel). catalizadores).
Estos catalizadores suelen estar soportados sobre óxido de aluminio o gel de sílice. Además del níquel y el cobre, se han desarrollado catalizadores exitosos utilizando zinc, cromo y combinaciones de estos metales.
Para la producción de alcoholes grasos se hidrogenan los correspondientes ésteres de ácidos carboxílicos. Las grasas y aceites naturales sirven como materiales de partida, que inicialmente se transesterifican para formar ésteres metílicos y luego se reducen a alcoholes, ya sea usando sodio (reducción de Bouveault-Blanc) o hidrogenación catalítica.
La reducción de sodio permite la preparación de alcoholes grasos insaturados a partir de ésteres de ácidos grasos insaturados.
La hidrogenación de ácidos grasos y ésteres de ácidos grasos requiere condiciones más severas en comparación con la hidrogenación de aldehídos. El proceso puede realizarse de forma continua o discontinua utilizando catalizadores de óxido de cobre-cromo (catalizadores Adkins), ya sea en suspensión o en lecho fijo.
Son típicas temperaturas de reacción de 240 a 300 °C y presiones de 200 a 300 bar. Modificando los catalizadores (por ejemplo, añadiendo cadmio), los ésteres de ácidos grasos insaturados se pueden convertir directamente en alcoholes grasos insaturados.
4. Condensación aldólica de aldehídos inferiores e hidrogenación de alquenales
En los procesos industriales, la síntesis oxo es la única fuente de aldehídos utilizados para la condensación aldólica.
Después de la eliminación de isoaldehídos y subproductos, la reacción de condensación es catalizada por ácidos o bases. La reactividad de cada aldehído está influenciada por la longitud de su cadena y el grado de ramificación, lo que requiere condiciones de reacción específicas adaptadas a cada compuesto individual.
Los aldoles formados en la condensación se deshidratan, dando como resultado la formación de alquenales. Estos alquenales se hidrogenan a continuación con ayuda de catalizadores heterogéneos. Normalmente, para este proceso se utilizan los mismos catalizadores empleados para la hidrogenación de oxoaldehídos.
Mediante este método, se pueden preparar 2-etilhexanol, 2-metilpentanol y cantidades limitadas de alcoholes isoméricos C16 y C18 altamente ramificados.
Sin embargo, el proceso aldox, que implica someter la mezcla de aldehídos formada en la síntesis oxo a condensación aldólica dentro del reactor oxo, no ha ganado una aceptación generalizada debido a la presencia de aldoles mixtos en los productos finales. Sin embargo, ciertos aldoles mixtos, como los del acetaldehído con aldehídos superiores, tienen importancia en aplicaciones específicas.
5. Oxidación de compuestos de trialquilaluminio
El etileno tiene la capacidad de sufrir adición con trietilaluminio, lo que da como resultado una mezcla de compuestos de trialquilaluminio con mayor masa molecular. Estos productos pueden someterse a oxidación con aire, dando lugar a la formación de los correspondientes alcóxidos de aluminio.
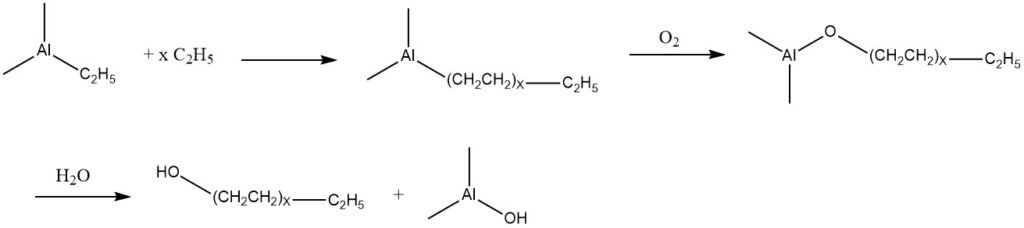
Posteriormente, estos alcóxidos sufren hidrólisis, produciendo una mezcla de alcoholes primarios lineales que poseen el mismo número de átomos de carbono que los grupos alquilo presentes en los componentes de trialquilaluminio.
A partir de esta reacción, conocida como proceso Ziegler, se han desarrollado dos procesos comerciales. Uno es el de Conoco, que opera en Estados Unidos desde 1962 y el de Condea Chemie (Conoco y Deutsche Texaco) en Alemania desde 1964.
El otro es de Ethyl Corp., que opera desde 1965. Las principales diferencias entre los dos procesos radican en la distribución de la longitud de la cadena y la linealidad de los alcoholes resultantes, así como en las características técnicas involucradas en la generación y control de este. distribución.
En el proceso de alcohol alfol (proceso Conoco), la reacción de crecimiento de la cadena se lleva a cabo a la temperatura más baja posible para evitar reacciones de desplazamiento que podrían conducir a la formación de olefinas. Los alcoholes resultantes muestran una distribución de longitud de cadena que se asemeja a una curva de Poisson y son prácticamente 100% lineales.
El proceso de alcohol alfol normalmente produce una amplia gama de alcoholes (C2-C28) y, aunque se pueden hacer ajustes para aumentar o disminuir la longitud de la cadena de los alcoholes fabricados, el patrón de distribución sigue siendo consistente.
Por otro lado, Ethyl Corp. ha desarrollado con éxito un proceso con crecimiento lineal controlado de cadena, que produce predominantemente alcoholes C12 y C14. Estos alcoholes tienen hasta un 95% de estructura lineal.
6. Oxidación de Hidrocarburos Saturados
La oxidación de Bashkirov implica la oxidación de hidrocarburos alifáticos con aire en presencia de ácido bórico, lo que da como resultado altos rendimientos de ésteres de ácido bórico.
Estos ésteres luego se hidrolizan en un paso posterior, produciendo alcoholes secundarios donde los grupos hidroxilo se distribuyen estadísticamente a lo largo de la cadena molecular. La reacción transcurre a través de un hidroperóxido secundario intermedio.
La oxidación normalmente se lleva a cabo en fase líquida a temperaturas entre 150 y 170 °C, con la presencia de 4 a 5 % en peso de ácido metabórico. Se utiliza una mezcla de nitrógeno y oxígeno (aproximadamente 3,5% de O2) a presión normal o ligeramente elevada.
Algunas plantas más nuevas incorporan aminas como cocatalizadores. Para lograr selectividades económicamente aceptables del 80 al 85 %, el nivel de conversión se mantiene por debajo del 20 %.
La evaporación instantánea se utiliza para eliminar los materiales de partida y los subproductos de la oxidación, seguida de la limpieza en depuradores alcalinos y de agua, y se reciclan los n-hidrocarburos.
Los ésteres del ácido metabórico o boroxinas obtenidos son resistentes a la oxidación y térmicamente estables. Tras la destilación fraccionada se obtienen alcoholes con una pureza superior al 98%.
El proceso concluye con un «hidroacabado» (hidrogenación sobre catalizadores heterogéneos de níquel) para eliminar sustancias coloreadas y olorosas.
El ácido ortobórico en la solución acuosa se convierte en ácido metabórico mediante deshidratación y la recuperación también se puede lograr mediante cristalización.
En algunas variantes recientes del proceso, el concentrado de ácido bórico se mezcla con los n-hidrocarburos, y la mezcla se deshidrata para evitar aglomeraciones y paros. Luego, la suspensión seca se devuelve al reactor de oxidación.
Bashkirov originalmente desarrolló el trabajo alemán en un proceso comercial en la década de 1950. La primera planta inició su producción en Shebekino/Belgorod, URSS, en 1959. También funcionaron plantas en la Unión Soviética y Japón. Sin embargo, la planta de Union Carbide (UCC) en Estados Unidos cerró en 1977.
Los alcoholes secundarios producidos en este proceso generalmente se convierten en etóxidos de alquilfenol y se utilizan como detergentes. Sin embargo, debido a la costosa recirculación de hidrocarburos y ácido bórico, así como a las desventajas en la aplicación de alcoholes secundarios, este proceso no ha adquirido una importancia significativa en el mundo occidental.
Aparte de la oxidación de Bashkirov, otro uso importante de la oxidación catalizada por ácido bórico es la preparación de ciclohexanol y ciclohexanona a partir de ciclohexano, como productos intermedios en la fabricación de caprolactama, ácido adípico y fenol.
Además, se utiliza en la síntesis de ciclododecanol (un producto intermedio en la síntesis del nailon 12) y ciclododecanona a partir de ciclododecano. El proceso implica oxidación con hidroperóxidos de alquilo, donde las porfirinas de hierro sirven como catalizadores útiles.
Los alcoholes se pueden obtener a partir de ácidos grasos mediante la esterificación de ácidos crudos fraccionados (principalmente en el rango C10-C15) con metanol o butanol, seguida de hidrogenación. Cuando se utilizan hidrocarburos lineales como materiales de partida, se pueden producir alcoholes lineales.
Sin embargo, dependiendo del hidrocarburo específico, el catalizador y las condiciones de reacción, la mezcla de alcoholes puede contener entre un 5% y un 15% de alcoholes de cadena ramificada. Debido a las impurezas presentes en los ácidos grasos, los alcoholes derivados de ellos pueden contener sustancias olorosas, lo que limita su espectro de aplicaciones.
7. Hidratación de olefinas
La hidratación de alquenos es un método común para la producción de alcoholes inferiores. Según la regla de Markovnikov, en esta reacción se forman alcoholes secundarios y terciarios (excepto en el caso del etileno).
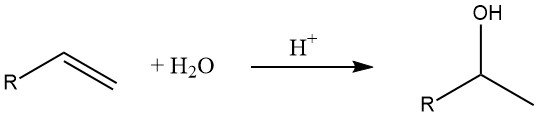
La velocidad de la reacción de hidratación depende de la estabilidad del ion carbenio intermedio, siendo los iones carbenio terciarios más estables que los secundarios y primarios.
Por lo tanto, la hidratación del isobuteno ocurre fácilmente a temperatura ambiente en presencia de bajas concentraciones de ion H⁺ debido a la relativa estabilidad del ion carbenio terciario intermedio. Por otro lado, la hidratación del etileno requiere temperaturas y presiones elevadas.
En entornos industriales, se utilizan dos variantes de la reacción de hidratación. En el proceso indirecto, la reacción en fase líquida se produce en dos pasos. Inicialmente, la olefina reacciona con ácido sulfúrico para formar mono y dialquilsulfatos, que luego se hidrolizan para producir el alcohol después de diluirlo con agua. Sin embargo, este proceso requiere una costosa etapa de reconcentración para reciclar el ácido sulfúrico.
En el proceso directo, la hidratación tiene lugar en fase gaseosa. Como la reacción es exotérmica y conduce a una reducción de volumen (2 moles de reactivo forman 1 mol de producto), la formación de alcohol se ve favorecida por la alta presión y la baja temperatura.
Debido a una conversión incompleta, en este proceso es necesario un costoso reciclaje de gas. Los catalizadores eficaces para la reacción de hidratación directa incluyen materiales que contienen ácido fosfórico como la celita, aunque también se utilizan cada vez más intercambiadores de iones.
La hidratación directa se emplea principalmente en la producción de etanol a partir de etileno y alcohol isopropílico a partir de propeno. También desempeña un papel importante en la fabricación de 2-butanol a partir de una mezcla de 1-buteno y 2-buteno (refinado II) y alcohol terc-butílico a partir de isobuteno.
8. Homologación de Alcoholes
La homologación es una reacción química en la que los alcoholes reaccionan con el gas de síntesis en presencia de sistemas catalíticos complejos de múltiples componentes. Dependiendo de las condiciones de reacción específicas, los productos obtenidos pueden ser aldehídos o alcoholes con un grupo CH2 adicional en comparación con los materiales de partida.
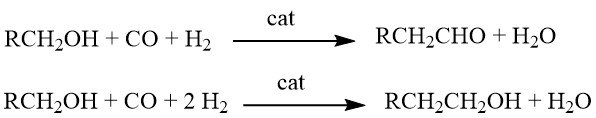
Originalmente, esta reacción se desarrolló para la síntesis de etanol a partir de metanol. Sin embargo, sus aplicaciones se han ampliado para incluir la producción de aldehídos homólogos (como acetaldehído a partir de metanol), ácidos carboxílicos (p. ej., ácido propiónico a partir de ácido acético), ésteres de ácidos carboxílicos (p. ej., acetato de etilo a partir de acetato de metilo) e incluso el síntesis de estireno (mediante homologación del alcohol bencílico a 2-feniletanol, seguida de deshidratación).
A pesar de los importantes avances en esta área, el proceso de homologación no se ha implementado a escala industrial debido a varios desafíos. La conversión y la selectividad conseguidas hasta ahora son todavía insuficientes para el uso industrial práctico y existen dificultades asociadas con el reciclado de los complejos catalizadores de homologación. Como resultado, la aplicación a escala industrial de la reacción de homologación sigue siendo limitada.
9. Proceso de repetición
El proceso de hidrocarbonilación de Reppe implica la reacción de olefinas con monóxido de carbono y agua, utilizando sales de amonio de tetracarbonildihidrido hierro como catalizador, para producir alcoholes. De manera similar a la oxosíntesis, este proceso también produce productos de cadena ramificada, lo que da como resultado una relación molar de alcoholes lineales a alcoholes de cadena ramificada de aproximadamente 9:1.

Por ejemplo, el propeno reacciona a temperaturas de 90 a 110 °C y presiones entre 5 y 20 bar para producir butanoles con un alto rendimiento del 90 %. Alrededor del 4% del propeno se hidrogena para formar propano. Sin embargo, la conversión de olefinas superiores requiere condiciones de reacción más severas.
A pesar de su potencial, el proceso de hidroformilación de Reppe no puede competir con la hidroformilación en términos de importancia industrial. La única planta conocida que utiliza este proceso para fabricar butanol a partir de propeno (Japan Butanol Co., con una capacidad de 30.000 t/a) dejó de funcionar a principios de los años 1980.
10. Hidrocarboximetilación
La hidrocarboximetilación es una variación del proceso de Reppe en el que las olefinas superiores se someten a una reacción con monóxido de carbono y metanol, empleando un catalizador de cobalto-piridina.
Los productos resultantes son ésteres de ácidos carboxílicos que tienen un átomo de carbono más en la cadena original en comparación con la materia prima de olefina original. Estos ésteres se pueden hidrogenar adicionalmente para producir los alcoholes correspondientes.
Sin embargo, a pesar de su potencial, el proceso no ha adquirido una importancia industrial significativa debido a consideraciones económicas. Actualmente, los productos se pueden preparar de forma más económica utilizando materias primas naturales. Como resultado, la hidrocarboximetilación aún no ha alcanzado una importancia generalizada en aplicaciones industriales.
11. Fermentación
La fermentación, que se cree que es uno de los métodos más antiguos para producir etanol, todavía se practica ampliamente a gran escala. En menor escala, los pentanoles se recuperan de los alcoholes de fusel.
Recientemente, la fermentación de butanol-acetona de materias primas de carbohidratos ha adquirido una importancia cada vez mayor.
Empresas como Gevo y Butamax (una empresa conjunta entre BP y DuPont) han llevado a cabo investigaciones exhaustivas sobre la producción de butanol a partir de materias primas renovables. Esto significa un interés creciente en el uso de procesos de fermentación para fabricar butanol a partir de fuentes sostenibles.
12. Alcoholes Guerbet
En el proceso Guerbet, los alcoholes primarios saturados se dimerizan para producir alcoholes primarios ramificados en α. Normalmente, la reacción se lleva a cabo haciendo refluir el alcohol en presencia de un agente de condensación alcalino y un catalizador de hidrogenación-deshidrogenación, como se muestra a continuación:
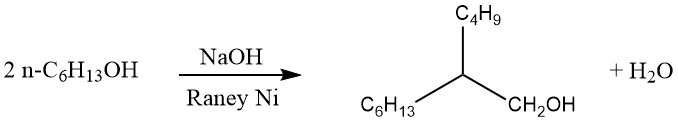
El agua y pequeñas cantidades de hidrógeno generados durante la reacción se eliminan continuamente. Si se calienta durante mucho tiempo, también se pueden formar alcoholes primarios triméricos ramificados en α.
El rendimiento de alcoholes diméricos en el proceso Guerbet es de aproximadamente el 80%. Este rendimiento puede mejorarse reciclando los residuos y añadiendo catalizador nuevo de forma incremental. Si bien se han propuesto diversas sustancias, incluido el sodio metálico, como agentes de condensación, los hidróxidos de metales alcalinos se prefieren comúnmente para aplicaciones industriales.
Los alcoholes de cadena corta con longitudes de cadena más cortas que el alcohol cetílico (C16) se dimerizan preferentemente a mayor presión. Mediante este proceso, es posible convertir alcoholes de cadena corta en alcoholes C10-C20. Por ejemplo, se producen 2-hexildecanol y 2-octildodecanol, que encuentran aplicación en cosmética como componentes oleosos con propiedades disolventes beneficiosas.
Sin embargo, la reacción de Guerbet no ha adquirido importancia industrial, ya que los alcoholes con ramificación α típica se preparan más fácilmente con otros métodos. Por ejemplo, el 2-etil-1-hexanol se puede obtener mediante hidroformilación de propeno para producir butanal, seguido de una etapa de condensación aldólica.
Debido a la disponibilidad de procesos alternativos para sintetizar alcoholes ramificados α, la reacción de Guerbet no se ha establecido como un proceso industrial a gran escala.
13. Otros procesos
La epoxidación de α-olefinas lineales seguida de una posterior escisión por hidrogenación es de gran interés comercial. Este proceso conduce a la producción de alcoholes plastificantes (C6-C10) o alcoholes detergentes (C10-C16).
Para la etapa de escisión por hidrogenación, se pueden utilizar varios catalizadores. La selectividad hacia los alcoholes primarios puede verse influenciada por la elección del catalizador, las condiciones del proceso de hidrogenación y el uso de disolventes.
Además, la hidrólisis de ésteres de ácidos carboxílicos tiene cierta importancia en aplicaciones industriales.
Referencia
- Alcohols, Aliphatic; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_279.pub2
