Ftalonitrilo: propiedades, reacciones, producción y usos
¿Qué es el ftalonitrilo?
El ftalonitrilo, también conocido como 1,2-dicianobenceno o 1,2-bencenodicarbonitrilo, es un compuesto orgánico con la fórmula C8H4N2. Es un polvo cristalino con un ligero color amarillo grisáceo y un ligero olor aromático, similar al benzonitrilo.
El ftalonitrilo se descubrió por primera vez en 1896, durante la diazotación del 2-aminobenzonitrilo.
Tabla de contenido
1. Propiedades físicas del ftalonitrilo
El ftalonitrilo es un sólido cristalino que no es soluble en agua (alrededor de 1 g/L), pero sí en solventes orgánicos como etanol, acetona, nitrobenceno, benzonitrilo y éter.
El ftalonitrilo no se puede destilar y sufre polimerización cuando se calienta por encima de su punto de fusión. No es explosivo y su ignición es difícil, pero el polvo puede explotar.
La Tabla 1 presenta las propiedades físicas importantes del ftalonitrilo.
| Propiedad | Valor |
|---|---|
| Número CAS | [91-15-6] |
| Fórmula | C6H4N2 |
| Peso molecular | 128,14 g/mol |
| Punto de fusión | 141 °C |
| Punto de ebullición | 304,5 °C (descomposición) |
| Densidad | 1,238 g/cm3 |
| Densidad aparente | ≈ 0,5 g/cm3 |
| Punto de inflamación | 162 °C |
| Calor de combustión | 4013 kJ/mol |
| Calor de evaporación | 67 kJ/mol |
| Capacidad calorífica específica (30 °C) | 1,30 J g-1 K-1 |
| Presión de vapor (20 °C) | 0,05 mbar |
| Temperatura de autoignición | > 580 °C |
2. Reacciones del ftalonitrilo
El ftalonitrilo experimenta varias reacciones importantes típicas de los grupos nitrilo y los compuestos aromáticos, algunos de los cuales se utilizan en la industria.
El ftalonitrilo reacciona con varios precursores metálicos, como el cloruro de cobre, a una temperatura de alrededor de 180 °C en un disolvente para formar pigmentos de ftalocianina de colores intensos y duraderos.
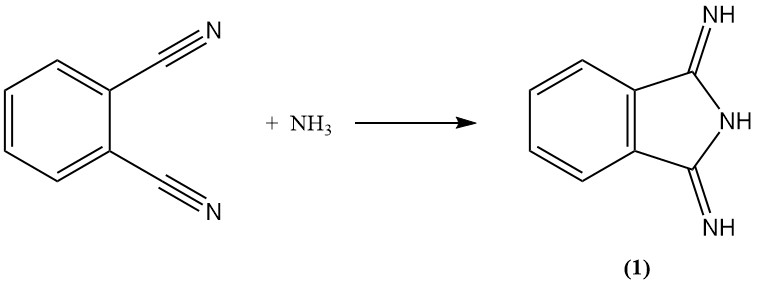
El ftalonitrilo reacciona con amoníaco para formar diiminoisoindolina (1). Este intermedio puede luego condensarse aún más con compuestos de metileno activos para producir pigmentos amarillos de importancia comercial.
El ftalonitrilo puede participar en reacciones de curado cuando se combina con promotores específicos, como compuestos que contienen grupos sulfhidrilo. Esta reacción tiene aplicaciones potenciales para crear nuevos materiales.
En condiciones específicas, pueden ocurrir reacciones en estado sólido entre el ftalonitrilo y otros compuestos. Por ejemplo, dopar el ftalonitrilo con diiminoisoindolina puede inducir reactividad térmica, lo que lleva a la formación de ftalocianina.
A temperaturas altas por encima del punto de fusión, el ftalonitrilo puede sufrir polimerización, donde sus moléculas individuales se unen para formar cadenas más grandes, creando un material polimérico a base de ftalonitrilo.
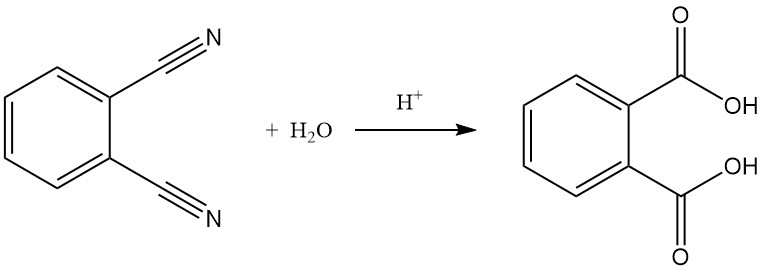
La hidrólisis del ftalonitrilo a ácido ftálico es posible, especialmente en condiciones duras como ácidos fuertes y temperaturas elevadas.
El ftalonitrilo puede experimentar reacciones de sustitución aromática limitadas, como halogenación, nitración, sulfonación, acilación y alquilación, en comparación con un anillo aromático simple como el benceno, debido al efecto desactivador de los grupos nitrilo.
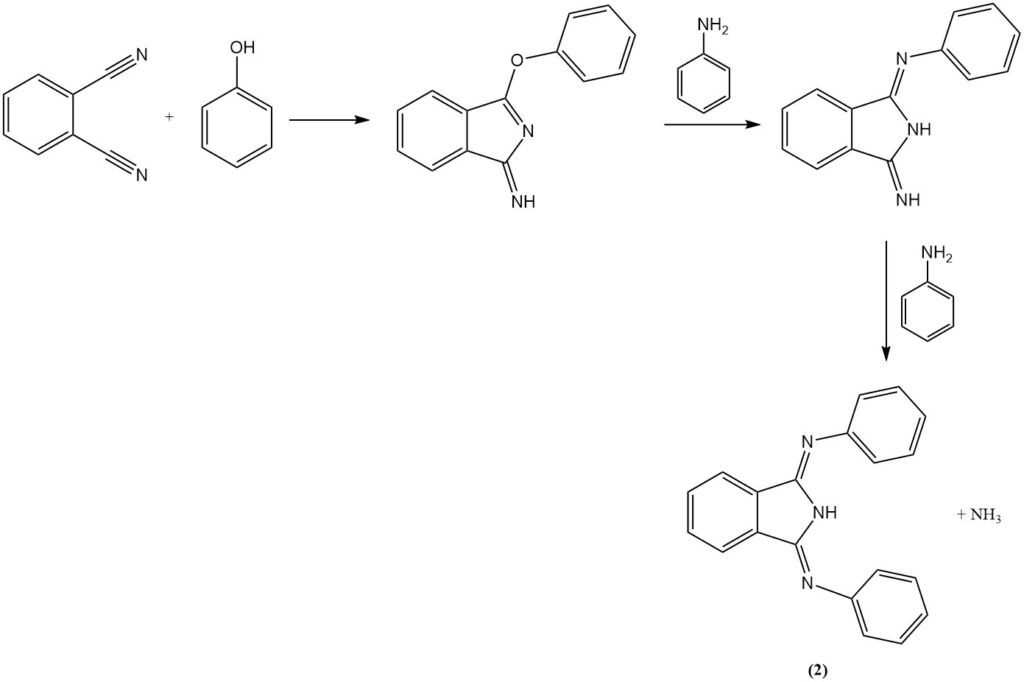
La reacción del ftalonitrilo con anilina en presencia de fenol produce un compuesto heterocíclico (2), y con diaminas produce macroheterociclos que contienen nitrógeno (hexaciclos) (3).
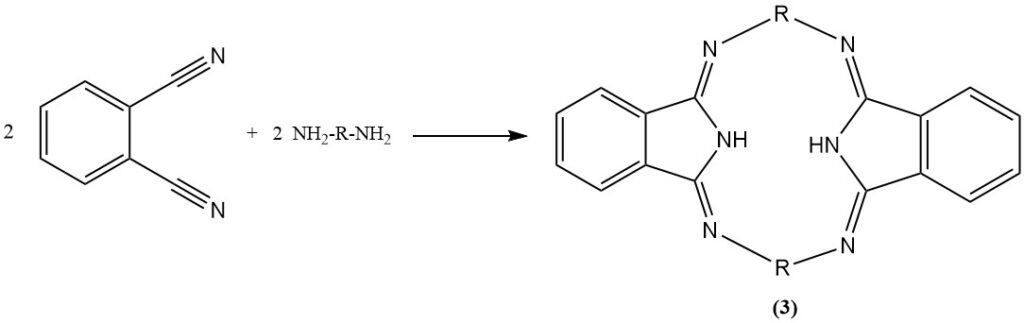
También es posible hidrogenar los grupos nitrilo del ftalonitrilo para producir un derivado de diamina.
3. Producción industrial de ftalonitrilo
El ftalonitrilo se produce comercialmente a partir de o-xileno, ácido ftálico, anhídrido ftálico, ftalamida o ftalimida.
3.1. Producción de ftalonitrilo a partir de o-xileno
Comercialmente, el ftalonitrilo se produce principalmente a partir de o-xileno mediante un proceso llamado amoxidación. Esta reacción continua en fase gaseosa de una sola etapa utiliza un reactor de lecho fluidizado para una conversión eficiente.
En el proceso de amoxidación, las mezclas de óxidos metálicos que contienen vanadio, antimonio, cromo y molibdeno soportados sobre alúmina o sílice son catalizadores comúnmente utilizados. Se pueden agregar óxidos de hierro, tungsteno y metales alcalinos para mejorar la actividad.
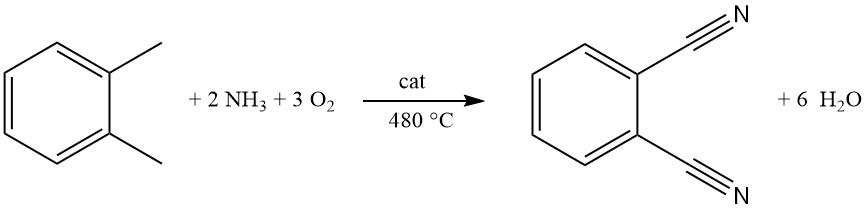
Una mezcla gaseosa de o-xileno, amoníaco y oxígeno se introduce en el reactor a través de una placa distribuidora. La temperatura óptima para este proceso sin presión es de alrededor de 480 °C.
Las temperaturas más bajas aumentan los subproductos como la ftalamida y la ftalimida (hasta un 10 %), mientras que las temperaturas más altas (>500 °C) provocan la combustión del amoníaco. Los sistemas de refrigeración integrados mantienen una temperatura constante a pesar de la reacción altamente exotérmica.
Los gases de reacción calientes se enfrían con una suspensión acuosa de ftalonitrilo en un decantador de productos. La mezcla enfriada se sedimenta y se decanta para separar y secar el producto de ftalonitrilo. Este producto de alta pureza con un contenido de ácido/ftalimida < 0,1 % y un contenido de agua < 0,1 % se puede utilizar directamente para la producción de pigmentos de ftalocianina, con lo que se logran rendimientos del 80-85 %.
El amoníaco se recupera de la corriente de gas posterior al sedimentador, que contiene NH3, CO2, CO, N2 y trazas de HCN, mediante una planta de recuperación de amoníaco dedicada. El gas de escape restante se quema y el amoníaco recuperado se recicla nuevamente en el proceso.
El o-xileno que no reaccionó y el o-toluonitrilo intermedio se pueden aislar o reintroducir en el reactor para su conversión completa en ftalonitrilo.
Los estudios de plantas piloto han explorado un proceso de amonolisis oxidativa continua para la síntesis de ftalonitrilo a partir de o-xileno. Este proceso utiliza un catalizador de óxido de vanadio-óxido de molibdeno sobre un soporte de alúmina o sílice a 350–450 °C.
Aquí, el catalizador de óxido metálico actúa como oxidante, y una parte se elimina, reoxida y recicla continuamente. El enfriamiento del ftalonitrilo y la gestión de los subproductos son similares al proceso de amoxidación.
Los subproductos como el o-toluonitrilo, la ftalamida y la ftalimida se pueden reintroducir en el reactor principal o convertirse en ftalonitrilo en un reactor independiente a una temperatura de 400 °C en presencia de amoníaco y un catalizador de fosfato de boro y alúmina.
El amoníaco se recupera de la mezcla de gases residuales, que contiene NH3, CO2, CO, N2 y trazas de HCN, y se recicla de nuevo al reactor. Los gases nocivos como el CO y el HCN se queman en un regenerador, mientras que el N2 y el CO2 se eliminan de la corriente de proceso.
3.2. Producción de ftalonitrilo a partir de derivados del ácido ftálico
El ftalonitrilo también se puede sintetizar a partir de varios derivados del ácido ftálico, incluidos el ácido ftálico, el anhídrido ftálico, la ftalamida y la ftalimida. Este proceso implica una reacción en fase gaseosa con eliminación de amoniaco y agua a temperaturas que oscilan entre 300 y 500 °C en presencia de un catalizador.
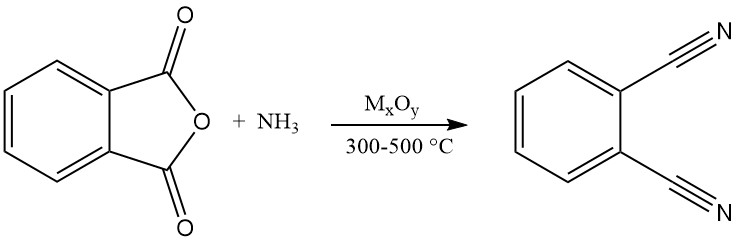
La literatura de patentes sugiere el uso de catalizadores de óxido metálico soportados sobre sílice, alúmina, fosfatos, silicatos, boratos o alúmina básica. Algunos ejemplos incluyen óxidos de torio, cobre, berilio, circonio o tungsteno.
El anhídrido ftálico fundido se calienta primero a alrededor de 160 °C y se vaporiza en un aparato dedicado. A continuación, se introduce en el vaporizador un gas circulante precalentado que contiene una alta concentración de amoníaco (NH3 ≈ 90%).
Esta mezcla reacciona a una presión cercana a la atmosférica a una temperatura entre 350 y 400 °C en un reactor de lecho fijo ubicado aguas abajo del vaporizador. En este reactor se utiliza típicamente un catalizador de alúmina.
El gas de reacción caliente que sale del reactor se enfría con agua. A continuación, el ftalonitrilo se separa de la suspensión acuosa resultante mediante procesos de decantación y secado. La concentración de amoníaco en el gas circulante se mantiene en alrededor del 90 % mediante la adición continua de amoníaco.
El ftalonitrilo se puede formar por deshidratación de ftalamida utilizando haluros de ácido como fosgeno o cloruro de tionilo. Sin embargo, este método requiere pasos adicionales para evitar la hidrólisis de la ftalamida por el ácido generado.
Las técnicas utilizadas para superar este problema incluyen la adición de diluyentes (benceno, clorobenceno) o el empleo de aminas terciarias (N,N-dietil-o-toluidina, piridina) o aminas secundarias aciladas (N-metilformamida) para neutralizar el ácido.
Este proceso alternativo generalmente implica procedimientos complejos y manipulación química adicional, lo que lo hace menos favorable para la producción a gran escala en comparación con las rutas establecidas.
4. Usos del ftalonitrilo
El ftalonitrilo se utiliza como materia prima en la producción de pigmentos de ftalocianina, abrillantadores fluorescentes y sensibilizadores fotográficos.
La producción de pigmentos de ftalocianina, conocidos por sus colores intensos y durabilidad excepcional, es la aplicación industrial más importante del ftalonitrilo. La reacción del ftalonitrilo con varios precursores metálicos da lugar a una amplia gama de colores. Estos pigmentos se utilizan en pinturas, plásticos, textiles y tintas.
5. Toxicología del ftalonitrilo
Toxicidad aguda
- DL50 oral (rata): 30-125 mg/kg.
- No se observó irritación cutánea ni ocular en conejos.
- No hay evidencia de sensibilización en trabajadores involucrados en la producción y el uso de ftalonitrilo.
Toxicidad por dosis repetidas
- Se observaron efectos neurotóxicos (convulsiones, aumento de la excitación) en ratas y ratones tras una exposición oral repetida.
- Se informó de un aumento de la actividad y una disminución del peso corporal en un estudio de neurotoxicidad en ratas de 13 semanas con 10 y 25 mg de ftalonitrilo/kg/día. No se encontró ningún vínculo histopatológico con los cambios de comportamiento. En este estudio, la NOAEL fue de 3 mg/kg/día.
- La exposición ocupacional ha provocado convulsiones epileptiformes tardías (de horas a días) que duran minutos en los trabajadores.
- Los exámenes clínicos de 81 trabajadores con una exposición media al ftalonitrilo de 8,5 años (incluidos 11 con intoxicaciones agudas) no mostraron anomalías en la química clínica, la hematología, la neurología o el EEG.
- La exposición dérmica también puede ser relevante.
- Las medidas contra el cianuro no se consideran eficaces debido a la falta de metabolismo del cianuro.
Genotoxicidad
- El ftalonitrilo no fue mutagénico en la prueba de Ames ni en el ensayo de mutación genética CHO/HGPRT.
- Resultados negativos en la prueba de micronúcleos en ratones.
- No se observaron mayores aberraciones cromosómicas en los trabajadores, incluidos aquellos con intoxicaciones agudas.
Carcinogenicidad
Los estudios informan sobre la inducción de leucemia en ratas y ratones después de la administración oral, subcutánea y percutánea (ratones). Sin embargo, las descripciones vagas de los estudios limitan la evaluación concluyente.
Referencias
- Phthalic Acid and Derivatives, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a20_181.pub2
- https://www.sciencedirect.com/science/article/abs/pii/S0032386118302945
- https://pubchem.ncbi.nlm.nih.gov/compound/Phthalonitrile
- Reaction of O-phthalonitrile with aniline. – https://link.springer.com/article/10.1007/BF00954275
