Buttersäure: Eigenschaften, Reaktionen, Herstellung und Verwendung
Was ist Buttersäure?
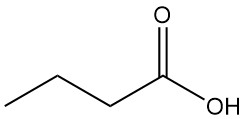
Buttersäure, auch bekannt als n-Butansäure, ist eine kurzkettige flüchtige Fettsäure mit der chemischen Formel C4H8O2. Es ist eine farblose, ölige Flüssigkeit mit einem unangenehmen, ranzigen Geruch, der mit Wasser und den meisten organischen Lösungsmitteln mischbar ist.
Buttersäure wurde 1869 von Lieben und Rossi entdeckt. Auf Latein bedeutet Buttersäure die Säure der Butter, da sie erstmals in ranziger Butter entdeckt wurde (Buttersäure wird aus dem Glycerid hydrolysiert und verursacht einen sehr unangenehmen Geruch).
Buttersäure ist eine kurzkettige gesättigte Fettsäure, die in Form von Estern in tierischen Fetten und Pflanzenölen vorkommt und auf natürliche Weise von anaeroben Bakterien produziert wird.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Buttersäure
Buttersäure ist eine Carbonsäure, die eine ölige, farblose Flüssigkeit bildet, die in Wasser, Ethanol und Ether löslich und in Tetrachlorkohlenstoff leicht löslich ist.
Tabelle 1 fasst die physikalischen Eigenschaften von Buttersäure zusammen.
| Eigenschaft | Wert |
|---|---|
| CAS-Nummer | [107-92-6] |
| Chemische Formel | C4H8O2 |
| Molekulargewicht | 88,1 g/mol |
| Schmelzpunkt | -7,9 °C |
| Siedepunkt Punkt | 163,5 °C |
| Dichte | 0,958 g/cm3 |
| pKa | 4,82 bei 25 °C |
| Viskosität bei 25 °C | 1,426 mPa.s |
| Brechungsindex | 1,3991 bei 20 °C |
| Kritische Temperatur | 342,05 °C |
| Kritischer Druck | 4,06 MPa |
| Dampfdruck | 1,65 mmHg |
| Flammpunkt | 72 °C |
| Zündungstemperatur | 443 °C |
2. Chemische Reaktionen von Buttersäure
Die Carboxylgruppe der Buttersäure unterliegt verschiedenen Arten von Reaktionen, hauptsächlich Deprotonierung, Reduktion und nukleophile Substitution. Andere Reaktionen finden aufgrund der Anwesenheit eines sauren Wasserstoffs an der α-Position der Carboxylgruppe statt.
Alkalimetallsalze der Buttersäure können leicht durch Neutralisierung mit einer Base (z. B. Natriumhydroxid) gewonnen werden. Ammoniumbutyrate werden durch Reaktion mit Ammoniak oder Aminen gewonnen.
n-Butanol kann durch Reduktion der Carboxylgruppe mit Reduktionsmitteln wie Lithiumaluminiumhydrid oder durch katalytische Hydrierung der Buttersäure oder ihrer Ester hergestellt werden.
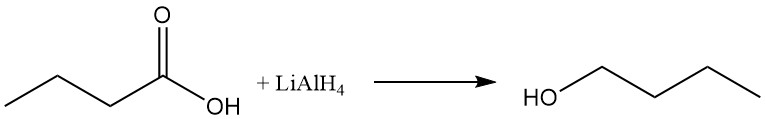
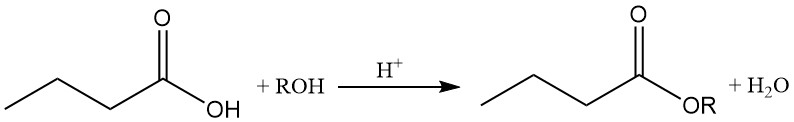
Buttersäureester entstehen durch eine säurekatalysierte Reaktion zwischen Buttersäure und Alkoholen oder Olefinen. Butyrate sind wichtige Zwischenprodukte in verschiedenen Industrien.
Buttersäureamide können direkt durch die Reaktion von Buttersäure mit Ammoniak oder Aminen synthetisiert werden. Da zuerst Ammoniumbutyrat entsteht, ist Erhitzen erforderlich, um Wasser zu entfernen und die Reaktion voranzutreiben.
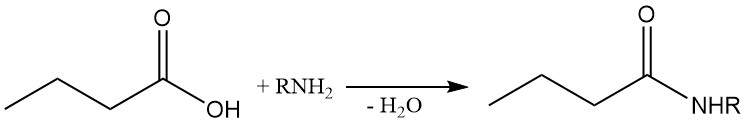
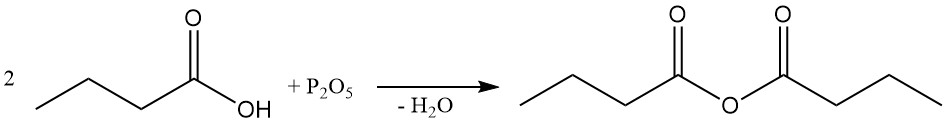
Buttersäureanhydrid wird durch Dehydratisierung von Buttersäure mithilfe eines Dehydratisierungsmittels (z. B. Phosphorpentoxid) oder vorzugsweise durch die Reaktion von Butyrylchlorid mit Buttersäure oder ihrem Salz hergestellt.
Butyrylhalogenide können aus Buttersäure unter Verwendung halogenierender Verbindungen wie Thionylhalogeniden, Phosphorhalogeniden oder Phosphoroxyhalogeniden gewonnen werden. Die hochreaktiven, hydrolyseempfindlichen Butyrylhalogenide sind eine wertvolle Klasse synthetischer Zwischenprodukte.
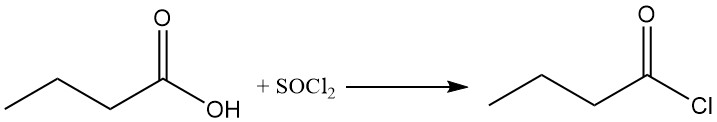
Die Oxidation von Buttersäure mit Wasserstoffperoxid ergibt Aceton, Kohlendioxid und Wasser.
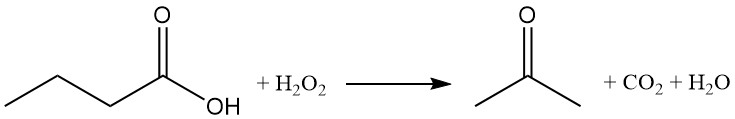
Unter bestimmten Bedingungen kann Buttersäure decarboxyliert werden.
Buttersäure mit mindestens einem Wasserstoff am Kohlenstoffatom neben der Carboxylfunktion kann ebenfalls in dieser α-Position deprotoniert werden, aber diese Tendenz ist bei weitem nicht so ausgeprägt wie bei Aldehyden und Ketonen. Zwei Äquivalente einer starken, nicht nukleophilen Base sind erforderlich.
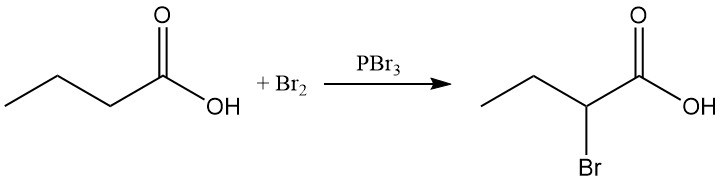
Bei der Hell-Volhard-Zelinsky-Halogenierung kann mit Brom und Phosphortribromid 2-Brombuttersäure synthetisiert werden.
3. Herstellung von Buttersäure
3.1. Chemische Herstellung von Buttersäure
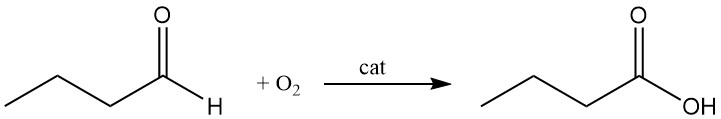
Kommerziell wird n-Buttersäure durch Flüssigphasenoxidation von n-Butanal mit Sauerstoff hergestellt. Dieser kontinuierliche Prozess ergibt eine farblose Flüssigkeit, die durch Rektifikation gereinigt wird.
Das Hydroformylierungsverfahren (Oxo-Verfahren) von Propylen ist die primäre Produktionsmethode für n-Butanal. Dabei wird Propylen unter Verwendung von Synthesegas (hauptsächlich Wasserstoff und Kohlenmonoxid) bei hohen Temperaturen (100–180 °C) und Drücken zwischen 20 und 30 MPa in Gegenwart eines metallischen Katalysators hydroformyliert.
Das LP-Oxo-Verfahren (Triphenylphosphin-modifizierte Rhodium-Oxo-Reaktion) ergibt bis zu 90 % Rohbuttersäure. Allerdings erzeugt das Oxo-Verfahren sowohl Butyraldehyd als auch Isobutyraldehyd, was die Buttersäureselektivität verringert. Darüber hinaus entstehen bei dem Verfahren umweltschädliche Nebenprodukte wie verbrauchte metallische Katalysatoren und giftige Verbindungen.
Um diese Probleme zu lösen, wurde eine einstufige Oxidation von Butyraldehyd zu Buttersäure unter Verwendung von molekularem Sauerstoff und heterogenen Katalysatoren entwickelt. Mit diesem Verfahren werden höhere Buttersäureausbeuten von über 99,5 % und eine Selektivität von über 95 % im Vergleich zum Oxo-Verfahren erzielt.
Bei diesem Verfahren werden hochaktive heterogene Katalysatoren wie Alkalimetall- und Kobaltsalze verwendet.
Laut einem Patent der Huntsman Petrochemical Corporation kann Buttersäure durch katalytische Hydrierung von Maleinsäureanhydrid mit einer Selektivität von 35 % für Buttersäure hergestellt werden.
Zu den wichtigsten Herstellern von Buttersäure zählen Oxea, Eastman und Perstorp.
3.2. Biosynthese von Buttersäure
Die Biosynthese von Buttersäure erfolgt unter anaeroben Bedingungen. Acetyl-CoA, das aus dem Abbau von Fettsäuren oder Pyruvat über Pyruvat-Ferredoxin-Oxidoreduktase gewonnen wird, dient als Vorläufer. Acetyl-CoA wird in Butyryl-CoA umgewandelt, wodurch anschließend Buttersäure entsteht.
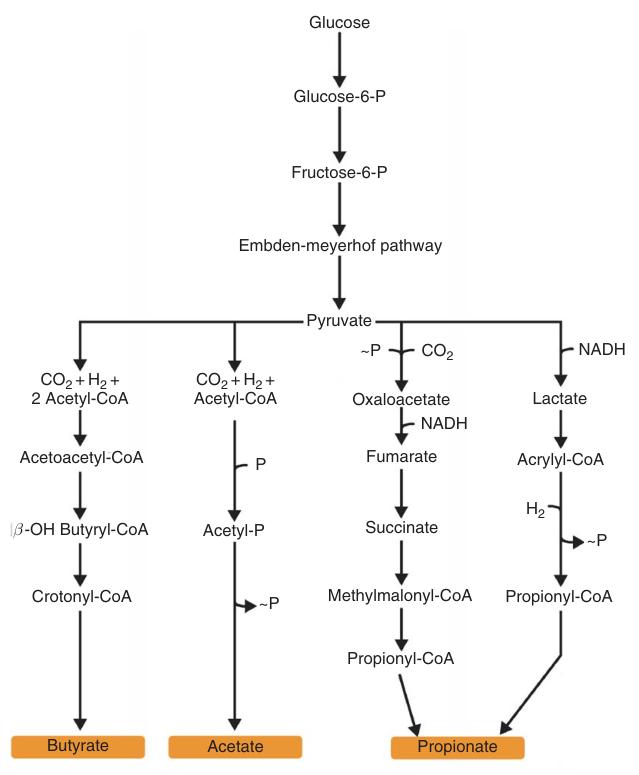
Bei der anaeroben Fermentation von Glucose zu Buttersäure werden drei ATP-Moleküle erzeugt, was die ATP-Ausbeute der Milchsäure/Ethanol-Fermentation (zwei ATP) übersteigt und der der Essigsäure-Fermentation (vier ATP) nahekommt.
Buttersäure ist ein Endprodukt der Fermentation, das von obligat anaeroben Bakterien mit Clostridium butyricum als Hauptorganismus produziert wird. Zu den anderen Buttersäure produzierenden Bakterien zählen Clostridium, Butyribacterium, Sarcina, Megasphera, Fusobacterium, Peptococcus, Butyrivibrio, Pseudobutyrivibrio und Eubacterium.
Optimale Wachstumsbedingungen sind 35–37 °C, eine CO2/N2-Atmosphäre und ein pH-Bereich von 4,5 bis 7,0. Hexosen, Pentosen und Polysaccharide können als Rohstoffe verwendet werden.
Die Buttersäureproduktion wird durch die Kontrolle der Nährstoffverfügbarkeit optimiert. Die Begrenzung von Glukose und essentiellen Elementen wie Phosphat und Stickstoff bei gleichzeitig langsamen Wachstumsbedingungen begünstigt die Bildung von Butyrat gegenüber anderen Produkten. Zur Steigerung der Effizienz können Batch-, Fed-Batch- oder kontinuierliche Fermentationsmethoden mit Zellretentionstechniken kombiniert werden.
Die Ansammlung von Buttersäure während des Fermentationsprozesses kann den Produktionsprozess verlangsamen. Um dies zu verhindern, wird die Konzentration der Buttersäure in der Fermentationsbrühe durch Destillation, Verdampfung, Permeatelektrodialyse, Adsorption, Extraktion oder Pertraktion reduziert.
4. Verwendung von Buttersäure
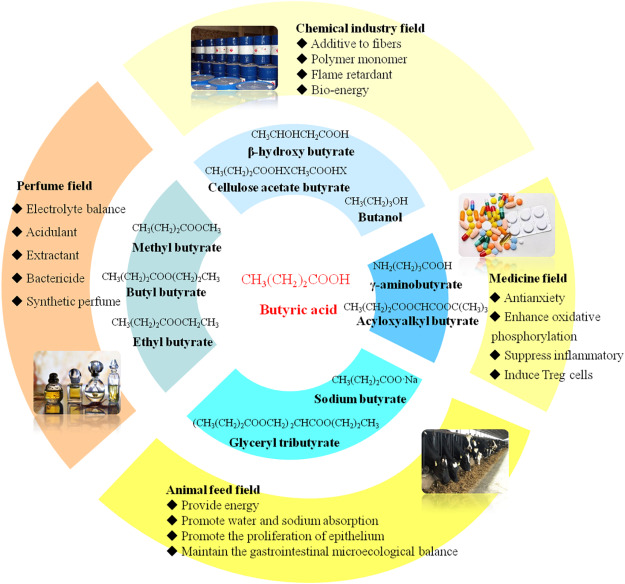
Buttersäure wird hauptsächlich zur Herstellung von Celluloseacetatbutyrat verwendet, einem Polymer, das bei der Herstellung von Kunststoffen, Beschichtungen und Textilien eingesetzt wird.
In der Lebensmittelindustrie werden Buttersäure und ihre Derivate als Aromastoffe verwendet und verleihen Butter, Käse und Süßwaren den charakteristischen Geschmack. Darüber hinaus wird sie aufgrund ihrer antimikrobiellen Eigenschaften als Lebensmittelkonservierungsmittel eingesetzt.
Buttersäureester werden in Parfüms verwendet, und einige dienen als Basis für künstliche Aromastoffe in bestimmten Spirituosen, Sodawassersirupen und Süßigkeiten.
Buttersäure wird aufgrund ihres starken Geruchs in Rezepturen zur Herstellung von Angelködern und Wildtierabwehrmitteln verwendet.
Buttersäure wird in Arzneimitteln als Histaminantagonist verwendet. Ihre Derivate haben Potenzial als Antikrebsmittel gezeigt, indem sie die Zelldifferenzierung induzieren. Buttersäure-Prodrugs wurden zur Behandlung von neoplastischen Erkrankungen und β-Globin-Störungen vorgeschlagen.
Es wird auch als Zwischenprodukt bei der Herstellung von Butyroperoxiden, Herbiziden, Emulgatoren, Desinfektionsmitteln und Tensiden verwendet.
In der Landwirtschaft wird Buttersäure als Futterzusatz und Nahrungsergänzungsmittel für Schweine, Rinder und Geflügel verwendet. Darüber hinaus hat sie sich als wirksam bei der Verhinderung von Pilzwachstum in Getreide mit hohem Feuchtigkeitsgehalt erwiesen.
Neuere Forschungen haben das Potenzial von Buttersäure als Vorläufer für die Produktion von Biokraftstoffen untersucht. Ihre Umwandlung in Butanol, einen energiereicheren Alkohol, ist ein aktives Forschungsgebiet.
5. Toxikologie der Buttersäure
Obwohl Buttersäure nicht in Verbraucherprodukten verwendet wird, kommt die allgemeine Bevölkerung hauptsächlich durch den Verzehr von Lebensmitteln, die sie enthalten, mit Buttersäure in Kontakt, wie z. B. tierischen Milchfetten, ätherischen Ölen, Pflanzenölen, tierischen Flüssigkeiten, fermentierten Produkten und bestimmten Früchten.
Buttersäure wird in der Leber schnell metabolisiert, hauptsächlich zu Essigsäure und Ketonkörpern (Aceton, Acetessigester und β-Hydroxybutyrat). Die Elimination von Buttersäure verläuft beim Menschen zweiphasig. Auf eine anfängliche schnelle Phase mit einer Halbwertszeit von 0,5 Minuten folgt eine langsamere Eliminationsphase mit einer Halbwertszeit von 13,7 Minuten.
Akute Toxizität
Buttersäure wird auf Grundlage der LD50-Werte in verschiedenen Tiermodellen als nicht toxisch eingestuft.
- Orale LD50 bei Ratten: 2940–8790 mg/kg
- Intraperitoneale oder subkutane LD50 bei Mäusen: 3180 mg/kg
- Inhalative LC50 bei Kaninchen: 440 mg/l
Buttersäure ist ein mäßig reizender Stoff für Haut und Augen. Bei Kaninchen wurden schwere Augenreizungen und Hornhautverbrennungen beobachtet. Bei Kaninchen, die Buttersäureaerosol (40 mg/l) ausgesetzt waren, wurden zunehmende Lethargie, Dyspnoe, Bronchial- und Kapillarerweiterung sowie Emphysem festgestellt.
Hohe intravenöse Dosen von Buttersäure (Natriumsalz) verursachen bei Kaninchen und Hunden eine vorübergehende Depression des ZNS. Bei Lämmern wurde nach intravenöser Verabreichung von Buttersäure eine erhöhte Plasmainsulinkonzentration beobachtet.
Akute Exposition von Menschen gegenüber Buttersäure führt hauptsächlich zu Reizungen oder Verbrennungen der Haut, Augen und Atemwege.
Bei Menschen umfassen Inhalationssymptome Halsschmerzen, Husten, Brennen, Kurzatmigkeit und Atemnot. Hautkontakt führt zu Schmerzen, Rötungen, Blasen und Hautverbrennungen. Augenkontakt verursacht Schmerzen, Rötungen, schwere Verbrennungen und möglichen Sehverlust.
Verschlucken führt zu Brennen, Bauchschmerzen, Schock und möglichem Kollaps.
Chronische Toxizität
In Tierstudien wurde wiederholte Exposition gegenüber mittleren bis hohen Dosen von n-Butylacetat und n-Butanol (Metaboliten der Buttersäure) von Tieren im Allgemeinen gut vertragen. Hohe Dosen von Buttersäure in der Nahrung führten jedoch bei Ratten zu Gewichtsverlust und Magengewebeanomalien.
In Studien an Menschen gilt Buttersäure als GRAS-Lebensmittelzusatzstoff (Generally Recognized As Safe). Chronische Exposition kann durch endogene Produktion und Nahrungsaufnahme erfolgen. Obwohl es sich um einen essentiellen Metaboliten handelt, kann eine längere Exposition die Lunge, das Nervensystem und die Schleimhäute schädigen.
Immuntoxizität
Längere Exposition von Mäusen, Ratten und Kaninchen gegenüber niedrigen atmosphärischen Konzentrationen von Buttersäure (0,1–0,2 mg/l) führte zu einem signifikanten Anstieg der zirkulierenden Lymphozyten und Neutrophilen.
Diese Immunreaktion wird in erster Linie der reizenden Wirkung der Buttersäure zugeschrieben und nicht einem spezifischen Angriff des Immunsystems.
Reproduktionstoxizität
Studien zur Reproduktionstoxizität von Buttersäure basieren in erster Linie auf ihren Metaboliten n-Butanol und n-Butylacetat.
Inhalationsstudien mit n-Butanol und n-Butylacetat zeigten bis zu bestimmten Konzentrationen keine negativen Auswirkungen auf die Reproduktionsparameter:
- Reproduktionstoxizität bei Frauen: 6000 ppm für n-Butanol und 1500 ppm für n-Butylacetat.
- Reproduktionstoxizität bei Männern: 3000 ppm für n-Butylacetat.
Entwicklungstoxizität
Die direkte Verabreichung von Buttersäure an trächtige Ratten führte bei hohen Dosen (100 und 133 mg/kg/Tag) zu einer hohen mütterlichen Mortalität und verringerter Gewichtszunahme. Trotz mütterlicher Toxizität wurden bei den Nachkommen keine nachteiligen Auswirkungen beobachtet.
Buttersäure verursacht bei Froschembryonen in einer Konzentration von 400 mg/l Missbildungen (Mikrozephalie, Augenschäden, Ödeme und Darmschäden).
Genotoxizität und Karzinogenität
Buttersäure ist nicht genotoxisch oder karzinogen.
Referenzen
- Carboxylic Acids, Aliphatic; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a05_235.pub2
- https://www.sciencedirect.com/science/article/abs/pii/B9780123864543005911
- https://www.sciencedirect.com/science/article/abs/pii/B9780128096338130833
- Process of Making Butyric Acid. – https://patents.justia.com/patent/20080009652
- https://www.sciencedirect.com/science/article/abs/pii/S0734975018301629
- https://onlinelibrary.wiley.com/doi/10.1100/2012/471417
- Fermentation process for producing butyric acid. – https://patents.google.com/patent/US2181310A/en
