Acide butyrique : propriétés, réactions, production et utilisations
Qu’est-ce que l’acide butyrique ?
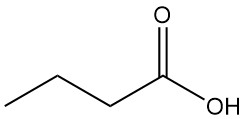
L’acide butyrique, également connu sous le nom d’acide n-butanoïque, est un acide gras volatil à chaîne courte dont la formule chimique est C4H8O2. C’est un liquide incolore et huileux avec une odeur désagréable et rance qui est missible avec l’eau et la plupart des solvants organiques.
L’acide butyrique a été découvert en 1869 par Lieben et Rossi. En latin, acide butyrique signifie l’acide du beurre, car il a été découvert pour la première fois dans le beurre rance (l’acide butyrique est hydrolysé à partir du glycéride et provoque une odeur très désagréable).
L’acide butyrique est un acide gras saturé à chaîne courte présent sous forme d’esters dans les graisses animales et les huiles végétales et est produit naturellement par des bactéries anaérobies.
Table des matières
1. Propriétés physiques de l’acide butyrique
L’acide butyrique est un acide carboxylique qui forme un liquide huileux et incolore, soluble dans l’eau, l’éthanol et l’éther et légèrement soluble dans le tétrachlorure de carbone.
Le tableau 1 résume les propriétés physiques de l’acide butyrique.
| Propriété | Valeur |
|---|---|
| Numéro CAS | [107-92-6] |
| Formule chimique | C4H8O2 |
| Poids moléculaire | 88,1 g/mol |
| Point de fusion | -7,9 °C |
| Point d'ébullition point | 163,5 °C |
| Densité | 0,958 g/cm3 |
| pKa | 4,82 à 25 °C |
| Viscosité à 25 °C | 1,426 mPa.s |
| Indice de réfraction | 1,3991 à 20 °C |
| Température critique | 342,05 °C |
| Critique pression | 4,06 MPa |
| Pression de vapeur | 1,65 mmHg |
| Point d'éclair | 72 °C |
| Température d'auto-inflammation | 443 °C |
2. Réactions chimiques de l’acide butyrique
Le groupe carboxylique de l’acide butyrique subit différents types de réactions, principalement la déprotonation, la réduction et la substitution nucléophile. D’autres réactions ont lieu en position α du groupe carboxylique en raison de la présence d’un hydrogène acide.
Les sels de métaux alcalins de l’acide butyrique sont facilement obtenus par neutralisation à l’aide d’une base (par exemple, l’hydroxyde de sodium). Les butyrates d’ammonium sont obtenus par réaction avec de l’ammoniac ou des amines.
Le n-butanol peut être préparé par réduction du groupe carboxyle à l’aide d’agents réducteurs tels que l’hydrure de lithium et d’aluminium ou par hydrogénation catalytique de l’acide butyrique ou de ses esters.
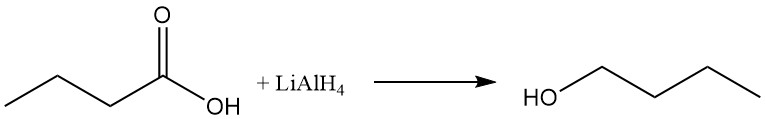
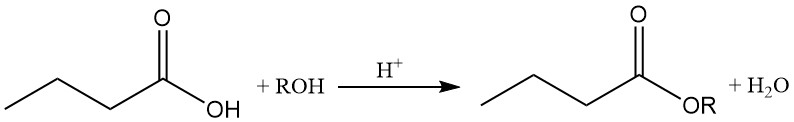
Les esters d’acide butyrique sont produits par une réaction acide-catalysée entre l’acide butyrique et des alcools ou des oléfines. Les butyrates sont des intermédiaires importants dans différentes industries.
Les amides butyriques peuvent être synthétisés directement en faisant réagir l’acide butyrique avec de l’ammoniac ou des amines. Comme le butyrate d’ammonium est formé en premier, un chauffage est nécessaire pour éliminer l’eau et accélérer la réaction.
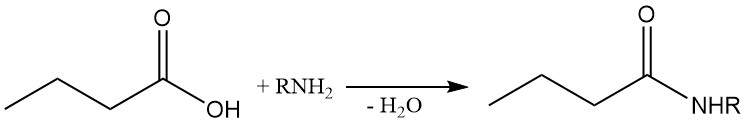
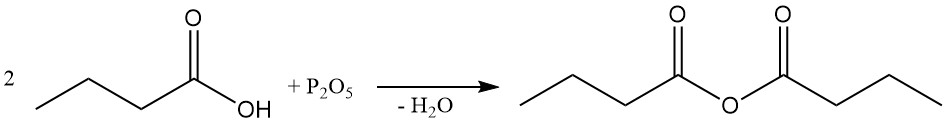
L’anhydride butyrique est préparé par déshydratation de l’acide butyrique à l’aide d’un agent déshydratant (par exemple, du pentoxyde de phosphore) ou, de préférence, par réaction de chlorure de butyryle avec de l’acide butyrique ou son sel.
Les halogénures de butyryle peuvent être obtenus à partir de l’acide butyrique en utilisant des composés halogénants tels que les halogénures de thionyle, les halogénures de phosphore ou les oxyhalogénures de phosphore. Les halogénures de butyryle, hautement réactifs et sensibles à l’hydrolyse, constituent une classe intéressante d’intermédiaires de synthèse.
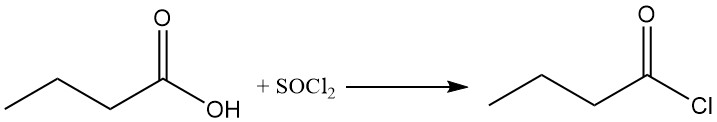
L’oxydation de l’acide butyrique avec du peroxyde d’hydrogène produit de l’acétone, du dioxyde de carbone et de l’eau.
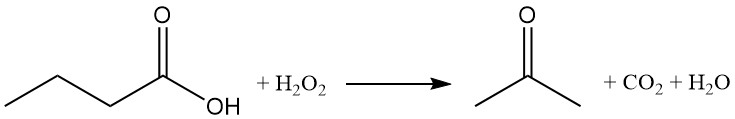
Dans certaines conditions, l’acide butyrique peut subir une décarboxylation.
L’acide butyrique ayant au moins un hydrogène sur le carbone à côté de la fonction carboxyle peut également être déprotoné dans cette position α, mais cette tendance est de loin moins prononcée que pour les aldéhydes et les cétones. Deux équivalents d’une base forte non nucléophile sont nécessaires.
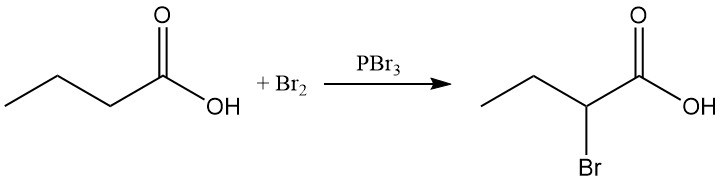
L’halogénation de Hell-Volhard-Zelinsky, en utilisant du brome et du tribromure de phosphore, permet de synthétiser l’acide 2-bromobutyrique.
3. Production d’acide butyrique
3.1. Production chimique d’acide butyrique
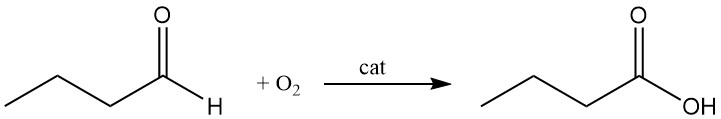
L’acide n-butyrique est produit commercialement par oxydation en phase liquide du n-butanal avec de l’oxygène. Ce procédé continu produit un liquide incolore, qui est purifié par rectification.
Le procédé d’hydroformylation (procédé Oxo) du propylène est la principale méthode de production de n-butanal. Il implique l’hydroformylation du propylène à l’aide de gaz de synthèse (principalement de l’hydrogène et du monoxyde de carbone) à des températures élevées (100-180 °C) et à des pressions comprises entre 20 et 30 MPa en présence d’un catalyseur métallique.
Le procédé LP Oxo (réaction oxo au rhodium modifiée par la triphénylphosphine) produit jusqu’à 90 % d’acide butyrique brut. Cependant, le procédé Oxo génère à la fois du butyraldéhyde et de l’isobutyraldéhyde, ce qui réduit la sélectivité de l’acide butyrique. De plus, le procédé produit des sous-produits nocifs pour l’environnement, tels que des catalyseurs métalliques usés et des composés toxiques.
Pour surmonter ces problèmes, une oxydation en une étape du butyraldéhyde en acide butyrique à l’aide d’oxygène moléculaire et de catalyseurs hétérogènes a été développée. Ce procédé permet d’obtenir des rendements d’acide butyrique supérieurs à 99,5 % et une sélectivité supérieure à 95 % par rapport au procédé Oxo.
Les sels de métaux alcalins et de cobalt sont des catalyseurs hétérogènes hautement actifs utilisés dans ce procédé.
Dans un brevet de Huntsman Petrochemical Corporation, l’acide butyrique peut être produit par hydrogénation catalytique de l’anhydride maléique avec une sélectivité de 35 % pour l’acide butyrique.
Les principaux fabricants d’acide butyrique sont Oxea, Eastman et Perstorp.
3.2. Biosynthèse de l’acide butyrique
La biosynthèse de l’acide butyrique se produit dans des conditions anaérobies. L’acétyl-CoA, dérivé de la dégradation des acides gras ou du pyruvate via la pyruvate-ferredoxine oxydoréductase, sert de précurseur. L’acétyl-CoA est transformé en butyryl-CoA, donnant ensuite de l’acide butyrique.
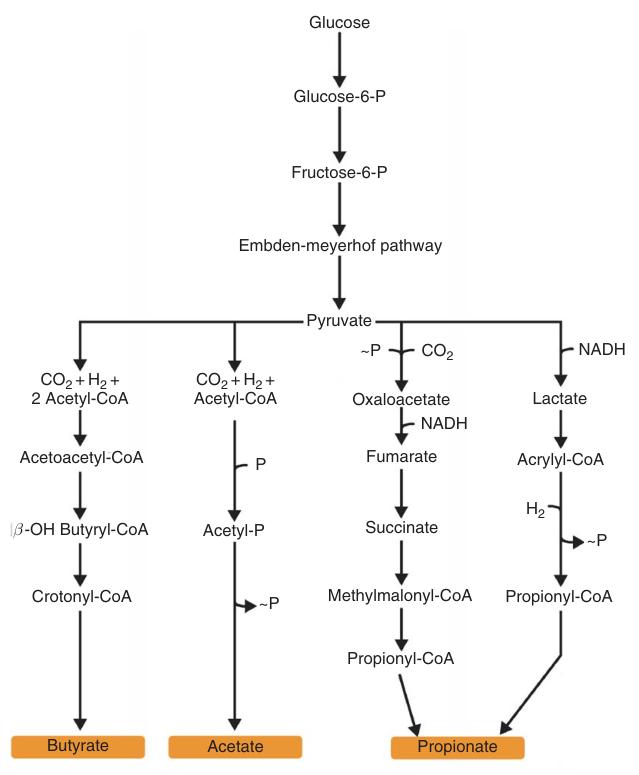
La fermentation anaérobie du glucose en acide butyrique génère trois molécules d’ATP, dépassant le rendement en ATP de la fermentation acide lactique/éthanol (deux ATP) et approchant celui de la fermentation acide acétique (quatre ATP).
L’acide butyrique est un produit final de fermentation produit par des bactéries anaérobies obligatoires, avec Clostridium butyricum comme organisme principal. D’autres bactéries productrices d’acide butyrique comprennent les espèces Clostridium, Butyribacterium, Sarcina, Megasphera, Fusobacterium, Peptococcus, Butyrivibrio, Pseudobutyrivibrio et Eubacterium.
Les conditions de croissance optimales englobent une température de 35 à 37 °C, une atmosphère de CO2/N2 et une plage de pH de 4,5 à 7,0. Les hexoses, les pentoses et les polysaccharides peuvent être utilisés comme matières premières.
La production d’acide butyrique est optimisée en contrôlant la disponibilité des nutriments. La limitation du glucose et des éléments essentiels comme le phosphate et l’azote tout en utilisant des conditions de croissance lente favorise la formation de butyrate par rapport à d’autres produits. Pour améliorer l’efficacité, les méthodes de fermentation par lots, par lots alimentés ou en continu peuvent être combinées avec des techniques de rétention cellulaire.
L’accumulation d’acide butyrique pendant le processus de fermentation peut réduire le processus de production. Pour éviter cela, la concentration d’acide butyrique dans le bouillon de fermentation est réduite par distillation, évaporation, électrodialyse par perméat, adsorption, extraction ou pertraction.
4. Utilisations de l’acide butyrique
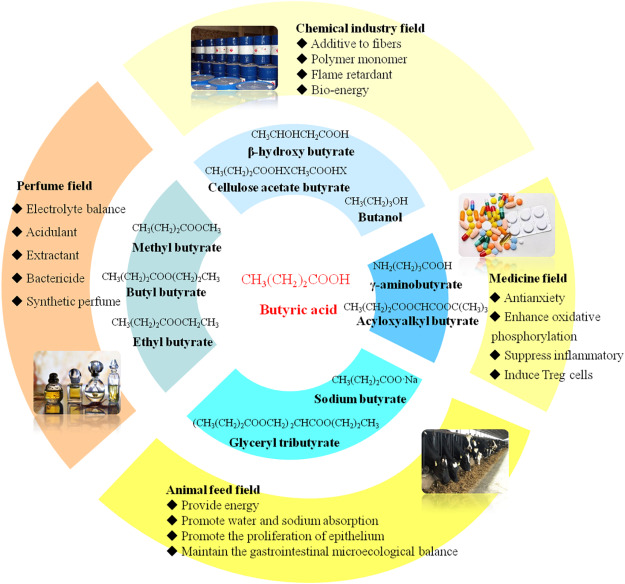
L’acide butyrique est principalement utilisé dans la production d’acétate butyrate de cellulose, un polymère utilisé dans la fabrication de plastiques, de revêtements et de textiles.
Dans l’industrie alimentaire, l’acide butyrique et ses dérivés sont utilisés comme agents aromatisants, contribuant au goût caractéristique du beurre, du fromage et des confiseries. De plus, il est utilisé comme conservateur alimentaire en raison de ses propriétés antimicrobiennes.
Les esters d’acide butyrique sont utilisés dans les parfums et certains servent de base à des ingrédients aromatisants artificiels dans certaines liqueurs, sirops d’eau gazeuse et bonbons.
L’acide butyrique est utilisé dans les formulations pour la préparation d’appâts de pêche et de répulsifs pour la faune en raison de sa puissante odeur.
L’acide butyrique est utilisé dans les produits pharmaceutiques comme antagoniste de l’histamine. Ses dérivés ont démontré un potentiel en tant qu’agents anticancéreux en induisant la différenciation cellulaire. Des promédicaments à base d’acide butyrique ont été suggérés pour le traitement des maladies néoplasiques et des troubles de la β-globine.
Il est également utilisé comme intermédiaire dans la production de butyroperoxydes, d’herbicides, d’émulsifiants, de désinfectants et de tensioactifs.
Dans l’industrie agricole, l’acide butyrique est utilisé comme additif alimentaire et complément alimentaire pour les élevages de porcs, de bovins et de volailles. De plus, il s’est avéré efficace pour prévenir la croissance fongique dans les céréales à forte teneur en humidité.
Des recherches récentes ont exploré le potentiel de l’acide butyrique comme précurseur pour la production de biocarburants. Sa conversion en butanol, un alcool à haute énergie, est un domaine de recherche actif.
5. Toxicologie de l’acide butyrique
Bien que l’acide butyrique ne soit pas utilisé dans les produits de consommation, l’exposition de la population générale se produit principalement lors de la consommation d’aliments qui en contiennent, tels que les matières grasses du lait animal, les huiles essentielles, les huiles végétales, les fluides animaux, les produits fermentés et dans certains fruits.
L’acide butyrique est rapidement métabolisé dans le foie, principalement en acide acétique et en corps cétoniques (acétone, acétoacétate et β-hydroxybutyrate). L’élimination de l’acide butyrique suit un schéma biphasique chez l’homme. Une phase initiale rapide avec une demi-vie de 0,5 minute est suivie d’une phase d’élimination plus lente avec une demi-vie de 13,7 minutes.
Toxicité aiguë
L’acide butyrique est classé comme non toxique sur la base des valeurs de DL50 dans divers modèles animaux.
- DL50 orale chez le rat : 2 940 – 8 790 mg/kg
- DL50 intrapéritonéale ou sous-cutanée chez la souris : 3 180 mg/kg
- CL50 par inhalation chez le lapin : 440 mg/l
L’acide butyrique est un irritant modéré pour la peau et les yeux. Une irritation oculaire grave et des brûlures cornéennes ont été observées chez les lapins. Une léthargie accrue, une dyspnée, une dilatation bronchique et capillaire et un emphysème ont été observés chez les lapins exposés à l’aérosol d’acide butyrique (40 mg/l).
Des doses intraveineuses élevées d’acide butyrique (sel de sodium) provoquent une dépression temporaire du système nerveux central chez les lapins et les chiens. Une augmentation de la concentration plasmatique d’insuline a été observée chez les agneaux après administration intraveineuse d’acide butyrique.
L’exposition aiguë à l’acide butyrique chez l’homme entraîne principalement une irritation ou des brûlures de la peau, des yeux et des voies respiratoires.
Chez l’homme, les symptômes d’inhalation comprennent un mal de gorge, une toux, une sensation de brûlure, un essoufflement et une respiration difficile. Le contact cutané entraîne des douleurs, des rougeurs, des cloques et des brûlures cutanées. Le contact avec les yeux provoque des douleurs, des rougeurs, des brûlures graves et une perte de vision potentielle.
L’ingestion entraîne une sensation de brûlure, des douleurs abdominales, un choc et un effondrement potentiel.
Toxicité chronique
Dans les études animales, l’exposition répétée à des doses modérées à élevées d’acétate de n-butyle et de n-butanol (métabolites de l’acide butyrique) est généralement bien tolérée chez les animaux. Cependant, des doses élevées d’acide butyrique dans l’alimentation ont entraîné une perte de poids et des anomalies des tissus gastriques chez les rats.
Dans les études sur l’homme, l’acide butyrique est considéré comme un additif alimentaire GRAS (Generally Recognized As Safe). Une exposition chronique peut se produire par production endogène et par ingestion alimentaire. Bien qu’il s’agisse d’un métabolite essentiel, une exposition prolongée peut endommager les poumons, le système nerveux et les muqueuses.
Immunotoxicité
L’exposition prolongée de souris, de rats et de lapins à de faibles concentrations atmosphériques d’acide butyrique (0,1-0,2 mg/l) a entraîné une augmentation significative des lymphocytes et des neutrophiles circulants.
Cette réponse immunitaire est principalement attribuée à la nature irritante de l’acide butyrique plutôt qu’à un ciblage spécifique du système immunitaire.
Toxicité pour la reproduction
Les études sur la toxicité reproductive de l’acide butyrique sont principalement basées sur ses métabolites, le n-butanol et l’acétate de n-butyle.
Les études d’inhalation sur le n-butanol et l’acétate de n-butyle n’ont montré aucun effet nocif sur les paramètres de reproduction jusqu’à certaines concentrations :
- Toxicité pour la reproduction chez la femelle : 6 000 ppm pour le n-butanol et 1 500 ppm pour l’acétate de n-butyle.
- Toxicité pour la reproduction chez l’homme : 3 000 ppm pour l’acétate de n-butyle.
Toxicité pour le développement
L’administration directe d’acide butyrique à des rates gravides a entraîné une mortalité maternelle élevée et une réduction du gain de poids corporel à des doses élevées (100 et 133 mg/kg/jour). Malgré la toxicité maternelle, aucun effet indésirable n’a été observé chez la progéniture.
L’acide butyrique induit des malformations (microcéphalie, malformations oculaires, œdèmes et malformations intestinales) chez les embryons de grenouille à une concentration de 400 mg/l.
Génotoxicité et cancérogénicité
L’acide butyrique n’est ni génotoxique ni cancérigène.
Références
- Carboxylic Acids, Aliphatic; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a05_235.pub2
- https://www.sciencedirect.com/science/article/abs/pii/B9780123864543005911
- https://www.sciencedirect.com/science/article/abs/pii/B9780128096338130833
- Process of Making Butyric Acid. – https://patents.justia.com/patent/20080009652
- https://www.sciencedirect.com/science/article/abs/pii/S0734975018301629
- https://onlinelibrary.wiley.com/doi/10.1100/2012/471417
- Fermentation process for producing butyric acid. – https://patents.google.com/patent/US2181310A/en
