Acétylation

En chimie, l’acétylation est une réaction organique dans laquelle un groupe acétyle (CH3CO-) est introduit dans une molécule. Cette réaction implique généralement l’utilisation d’acide acétique (CH3COOH) ou anhydride acétique (CH3CO)2O comme l’agent acétylant. Le produit obtenu est appelé acétate.
En biologie, l’acétylation est un type de modification post-traductionnelle qui implique l’ajout d’un groupe acétyle à une protéine. Cette modification peut altérer l’activité, la stabilité ou les interactions de la protéine avec d’autres molécules. L’acétylation est un processus réversible régulé par des enzymes appelées histones acétyltransférases (HAT) et histones désacétylases (HDAC).
Dans cet article, nous nous concentrons uniquement sur l’acétylation en chimie.
1. Mécanisme de réaction d’acétylation
Le mécanisme spécifique d’acétylation peut varier en fonction des réactifs impliqués et des substrats modifiés.
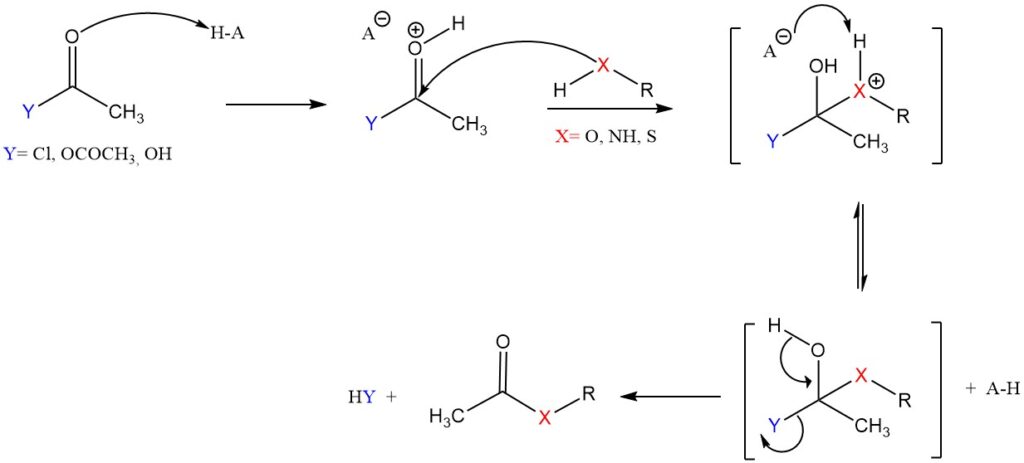
La substitution nucléophile acyle est couramment utilisée en chimie organique, où un groupe acétyle provenant d’un agent acétylant (comme l’anhydride acétique ou le chlorure d’acétyle) remplace un atome d’hydrogène sur la molécule cible.
- L’agent acétylant réagit avec un catalyseur acide homogène ou hétérogène pour générer un intermédiaire plus réactif, un cation.
- Ce cation, électrophile, sera attaqué par l’atome nucléophile (O, N ou S) du substrat pour former un intermédiaire tétraédrique.
- Le groupe partant (chlorure ou acétate) part pour former le produit acétylé final et régénérer le catalyseur acide.
La température, le pH et la présence de catalyseurs peuvent avoir un impact significatif sur la vitesse et l’efficacité du processus d’acétylation. De plus, les propriétés chimiques et la disposition spatiale de la molécule cible peuvent influencer l’accessibilité du site pour l’acétylation.
2. Agents d’acétylation
Les réactifs d’acétylation couramment utilisés en chimie organique et industrielle sont l’anhydride acétique, le chlorure d’acétyle et l’acide acétique.
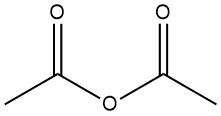
L’anhydride acétique est le réactif le plus couramment utilisé pour l’acétylation en laboratoire et dans l’industrie pharmaceutique. C’est relativement peu coûteux et facile à manipuler. Cependant, il présente l’inconvénient de générer de l’acide acétique comme sous-produit, qui peut parfois interférer avec la réaction.

Le chlorure d’acétyle est un autre réactif courant pour l’acétylation. Il est plus réactif que l’anhydride acétique, mais il est également plus corrosif et peut générer du chlorure d’hydrogène gazeux comme sous-produit, ce qui est nocif et corrosif pour les équipements.

L’acide acétique est peu coûteux et largement disponible et peut également être utilisé comme agent d’acétylation, mais il donne un faible rendement et nécessite un catalyseur de déshydratation pour minimiser l’eau produite comme sous-produit, ce qui favorise la réaction réversible ( désacétylation).
Le choix du meilleur réactif d’acétylation pour une réaction particulière dépendra de plusieurs facteurs, notamment le substrat, la sélectivité souhaitée et le coût.
3. Exemples de réactions d’acétylation importantes
L’aspirine (acide acétylsalicylique) est un analgésique et un anti-inflammatoire bien connu, produit par l’acétylation de l’acide salicylique.
L’acétaminophène (N-acétyl-p-aminophénol) est un autre analgésique et anti-inflammatoire courant, souvent utilisé chez les enfants et les personnes ayant l’estomac sensible. Il est obtenu par N-acétylation du p-aminophénol.
L’acétate de cellulose est un type de fibre synthétique utilisé dans les vêtements et les tissus d’ameublement. , et des filtres à cigarettes. Il est fabriqué par acétylation de cellulose.
Les monoglycérides acétylés sont utilisés comme émulsifiants et stabilisants alimentaires dans le pain, les glaces et d’autres aliments transformés.
L’acétate d’éthyle est un solvant courant produit par l’acétylation de l’éthanol et utilisé dans les peintures, les revêtements et les adhésifs.
La N-acétylcystéine (NAC), formée par N-acétylation de la cystéine, est un supplément antioxydant parfois utilisé pour traiter les problèmes respiratoires et d’autres affections.
3.1. Acétylation de l’Aniline
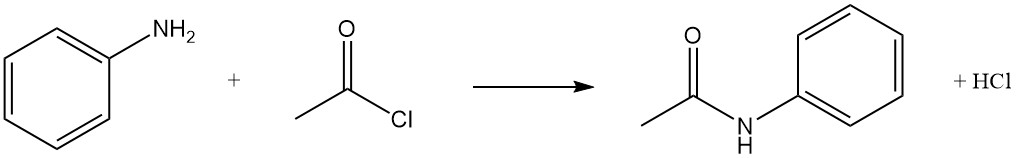
L’acétylation de l’aniline est une réaction fondamentale en chimie organique, transformant une amine basique en un intermédiaire précieux avec diverses applications industrielles et pharmaceutiques.
Dans cette réaction, l’aniline est acétylée par l’anhydride acétique ou le chlorure d’acétyle pour produire de l’acétanilide, souvent utilisé comme intermédiaire dans la synthèse des colorants et des produits pharmaceutiques. Selon l’agent acétylant choisi, de l’acide acétique ou du chlorure d’hydrogène se forment comme sous-produits.
3.2. Acétylation de l’acide salicylique

L’acétylation de l’acide salicylique, également connue sous le nom de synthèse de l’aspirine, est un exemple classique de chimie organique transformant une simple molécule en agent pharmaceutique.
L’acide salicylique (C₇H₆O₃) est un composé naturel présent dans l’écorce de saule et d’autres plantes. Il possède des propriétés analgésiques et anti-inflammatoires. Cependant, cela peut aussi irriter l’estomac.
L’acide acétylsalicylique, qui possède des effets analgésiques et anti-inflammatoires améliorés avec une irritation gastrique réduite par rapport à l’acide salicylique, est produit par acétylation de l’acide salicylique avec de l’anhydride acétique dans un milieu acide (par exemple, de l’acide sulfurique concentré). L’acide acétique est un sous-produit de la réaction.
3.3. Acétylation des acides aminés
L’acétylation des acides aminés est une modification post-traductionnelle (PTM) dynamique et répandue qui joue un rôle crucial dans la régulation de la fonction, de la stabilité et de l’interaction des protéines avec d’autres molécules. Cela implique l’ajout d’un groupe acétyle à des résidus d’acides aminés spécifiques, le plus souvent le groupe α-amino N-terminal ou le groupe ε-amino des résidus lysine.
Cette simple modification peut avoir des effets profonds sur le comportement des protéines, en influençant divers processus cellulaires tels que :
- Expression génique : l’acétylation des histones, où des groupes acétyle sont ajoutés aux protéines histones encapsulant l’ADN, affecte la structure et l’accessibilité de la chromatine, régulant ainsi la transcription des gènes.
- Activité enzymatique : l’acétylation peut activer ou désactiver les enzymes en modifiant leur structure, leur liaison au substrat ou leur interaction avec d’autres protéines régulatrices.
- Interactions protéine-protéine : en affectant les charges de surface et la conformation des protéines, l’acétylation peut moduler la façon dont les protéines interagissent entre elles, ce qui a un impact sur les voies de signalisation et réponses cellulaires.
- Dégradation des protéines : l’acétylation peut influencer la reconnaissance des protéines par les mécanismes de dégradation, en les marquant pour leur destruction ou en les protégeant de la dégradation.
Il existe deux principaux types d’acétylation des acides aminés :
- α-acétylation N-terminale : il s’agit du type le plus courant, se produisant sur le groupe α-amino N-terminal des molécules nouvellement synthétisées. protéines chez les eucaryotes. Il facilite le repliement et la stabilité des protéines, et sert souvent de signal pour le tri et le transport des protéines.
- ε-acétylation de la lysine : ce type implique l’ajout d’un groupe acétyle à la chaîne latérale des résidus lysine dans la séquence protéique. Cela peut se produire à la fois de manière co-traductionnelle (pendant la synthèse des protéines) et de manière post-traductionnelle (après la synthèse des protéines). Cette modification dynamique joue un large éventail de rôles régulateurs, en fonction de la protéine spécifique et du site d’acétylation.
