Ftalimida: propiedades, reacciones, producción y usos
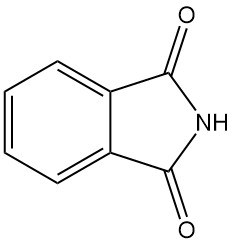
¿Qué es la ftalimida?
La ftalimida, también conocida como 1,3-dioxoisoindolina, es un compuesto orgánico con la fórmula química C8H5O2N. Es un sólido blanco ligeramente soluble en agua y soluble en soluciones básicas.
Tabla de contenido
1. Propiedades físicas de la ftalimida
La ftalimida es un compuesto heterocíclico que forma agujas o prismas blancos cuando se cristaliza en solución y plaquetas por sublimación.
Tiene una solubilidad limitada en agua (0,3 g a 20 °C, 0,9 g a 50 °C y 2,2 g a 100 °C por cada 100 g de agua). Sin embargo, se disuelve fácilmente en ácido acético, solución de hidróxido de sodio y solución de hidróxido de potasio.
La ftalimida sublima cuando se calienta por encima de su punto de fusión. Esta propiedad facilita su purificación.
Algunas de las propiedades físicas de la ftalimida se enumeran en la siguiente tabla:
| Propiedad | Valor |
|---|---|
| Número CAS | [85-41-6] |
| Fórmula | C8H5NO2 |
| Peso molecular | 147,14 g/mol |
| Punto de fusión | 238 °C |
| pKa | 8,30 |
| Calor de combustión | 3560 kJ/mol |
| Calor de fusión | 187,6 J/g |
| Capacidad calorífica específica (100 °C) | 1,21 J g-1 K-1 |
| Presión de vapor | |
| a 120 °C | 0,10 mbar |
| a 150 °C | 0,95 mbar |
| a 180 °C | 5,93 mbar |
| a 220 °C | 30,7 mbar |
| a 254 °C | 187,6 mbar |
| Punto de inflamación | 214 °C |
| Temperatura de ignición | 530 °C |
2. Reacciones de la ftalimida
La ftalimida reacciona con bases para formar sales solubles en agua. Estas sales pueden experimentar reacciones posteriores con halógenos (Cl2, Br2 e I2) para producir los derivados N-cloro, N-bromo o N-yodo correspondientes de la ftalimida.
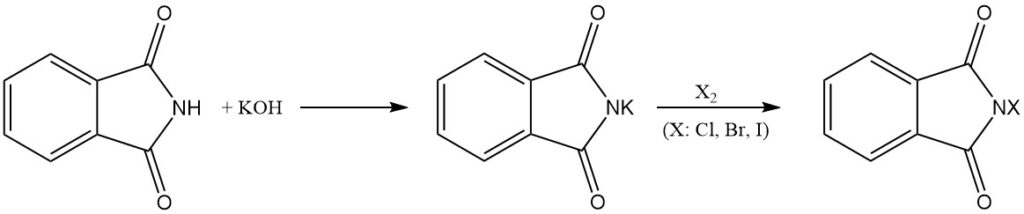
Los derivados N-halo también pueden obtenerse mediante el tratamiento de ftalimidas de metales alcalinos (por ejemplo, ftalimida de potasio) con ácido hipocloroso (HOCl) o hipobromoso (HOBr).
Al calentarlos, los derivados N-halo sufren una degradación de Hofmann, lo que da como resultado la formación de anhídrido isatoico (1) o ácido antranílico (ácido o-aminobenzoico) (2).
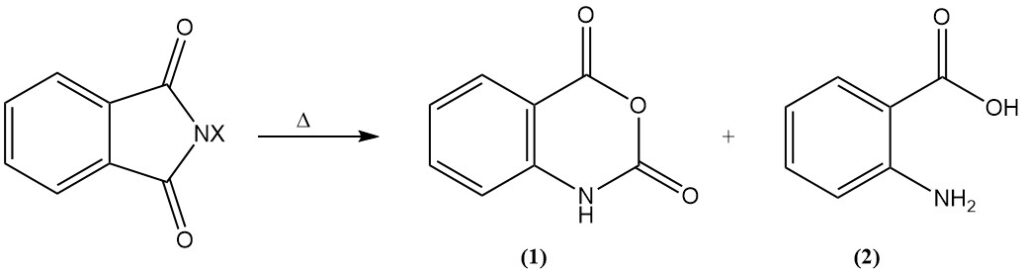
La reacción de ftalimidas de metales alcalinos con haluros de alquilo (RX) produce N-alquilftalimidas. La hidrólisis posterior o el tratamiento con hidrazina (hidrazinolisis) de estas N-alquilftalimidas forman aminas primarias. Esta secuencia de reacción se conoce como síntesis de Gabriel.
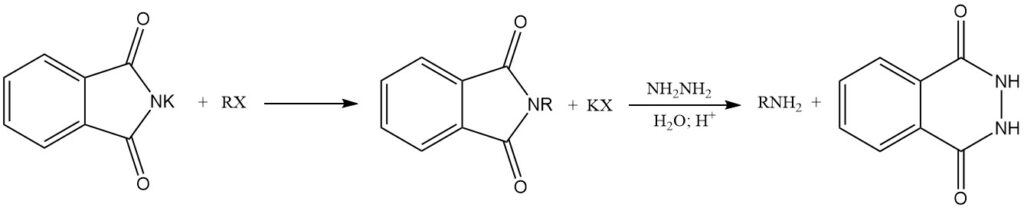
3. Producción industrial de ftalimida
La ftalimida se sintetiza principalmente a partir de anhídrido ftálico y amoníaco, aunque existen métodos alternativos que utilizan urea o amoxidación de o-xileno.
3.1. Producción de ftalimida a partir de anhídrido ftálico y amoníaco
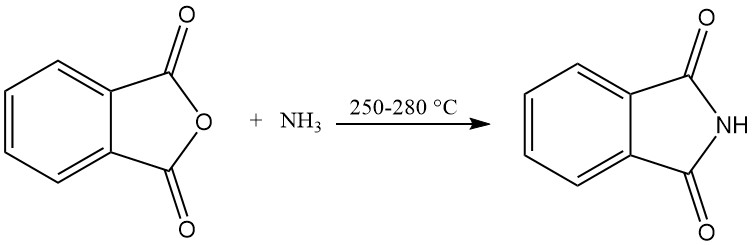
En la producción de ftalimida a escala industrial se utilizan procesos continuos.
El proceso de tubo de reacción vertical utiliza un tubo de reacción vertical calentado externamente y lleno de material de relleno. El anhídrido ftálico fundido y el exceso de amoníaco se introducen continuamente en la parte superior del tubo y reaccionan a 250–280 °C.
A continuación, los gases de reacción se enfrían en una cámara de sublimación, donde la ftalimida sólida se deposita y se descarga. El exceso de amoníaco y agua se eliminan a través de un tubo de gases de escape. Este proceso produce ftalimida con una pureza del 99 % y un alto rendimiento del 98 %.
En el proceso de contracorriente, el anhídrido ftálico fundido se introduce continuamente en la parte superior de un reactor, mientras que el amoníaco se introduce continuamente en la parte inferior. La temperatura aumenta gradualmente desde alrededor de 150 °C en la parte superior hasta un máximo de 270 °C en la parte inferior.
La ftalimida fundida con una pureza del 99 % sale del reactor y se enfría y se descascara. Se puede disolver en una solución alcalina acuosa para su uso posterior.
El gas de escape de la cabeza del reactor, que contiene vapor de agua, ftalimida sublimada y componentes que no han reaccionado, se depura con ftalimida fundida del fondo del reactor en contracorriente. Este proceso de depuración purifica el escape y permite la recuperación de los materiales de partida que no han reaccionado.
3.2. Producción de ftalimida a partir de anhídrido ftálico y urea
La ftalimida se puede producir a partir de anhídrido ftálico y urea en un proceso sin disolventes o en un disolvente.
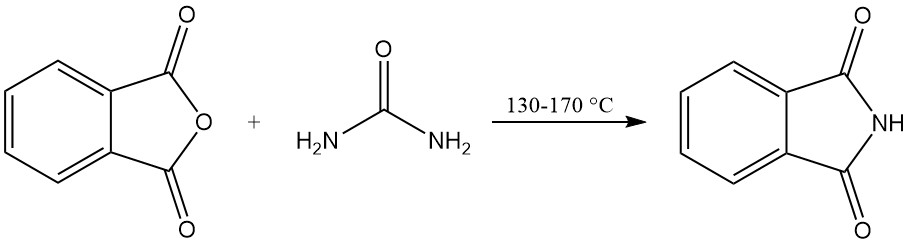
En el proceso sin disolventes, se calienta una mezcla de anhídrido ftálico y urea en un recipiente sellado. La reacción se lleva a cabo a 130–140 °C, con dióxido de carbono y vapor de agua como gases subproductos. La temperatura aumenta a alrededor de 160 °C debido a la reacción exotérmica.
La reacción se completa cuando cesa el desprendimiento de gas. A continuación, la mezcla de reacción solidificada se enfría, se muele y se utiliza directamente sin purificación adicional. Este método ofrece altos rendimientos, superiores al 90%.
En el proceso que utiliza un disolvente, el disolvente suele ser un hidrocarburo sustituido o no sustituido, un compuesto aromático o un compuesto heteroaromático (p. ej., n-propilbenceno, cumeno, 1,2-diclorobenceno, picolina).
El disolvente debe elegirse de forma que la urea sea insoluble, mientras que el ácido ftálico o anhídrido ftálico tenga una solubilidad limitada. La reacción se produce por debajo del punto de ebullición del disolvente (normalmente 160–170 °C). Una vez finalizado el proceso, el producto ftalimida puro se aísla mediante filtración y lavado con agua, consiguiendo rendimientos del 95-100 %.
3.3. Producción de ftalimida a partir de o-xileno
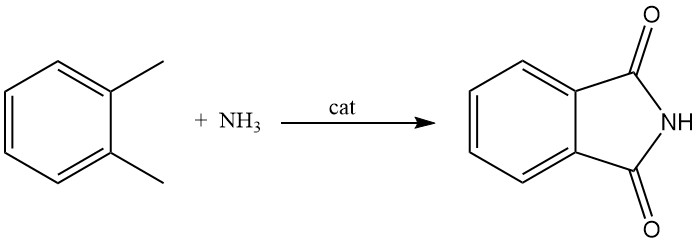
Aunque es menos común que los métodos que utilizan anhídrido ftálico, la ftalimida también se puede producir a partir de o-xileno. Este proceso implica la reacción de o-xileno en fase gaseosa con amoníaco en presencia de un catalizador de óxido metálico. Este catalizador también actúa como donante de oxígeno.
Dependiendo de las condiciones de reacción y el control, este proceso puede producir selectivamente ftalimida, ftalamida o ftalonitrilo.
4. Usos de la ftalimida
La ftalimida se utiliza como materia prima en varias industrias. Es un precursor para la producción de ácido antranílico por degradación de Hofmann y se utiliza en la síntesis de Gabriel para producir una amplia gama de aminas primarias.
La ftalimida se utiliza como grupo protector en química orgánica, particularmente en la síntesis de péptidos. Al reaccionar con el grupo amino, evita reacciones no deseadas mientras que el resto de la molécula se puede transformar. Se puede eliminar selectivamente para dar la amina libre.
También se utiliza como intermediario en la producción de pesticidas agrícolas, conservantes de madera, ciertos pigmentos y productos farmacéuticos como la talidomida, la anfotalida, la taltrimida, el talmetoprim y el apremilast.
5. Toxicología de la ftalimida
Aunque los datos sobre la toxicidad de la ftalimida son limitados, la información disponible sugiere que tiene una toxicidad baja.
La ftalimida se descompone en el cuerpo en ácido ftálico y amoníaco.
Los estudios con ratas y ratones indican una toxicidad oral aguda baja (LD50 > 5000 mg/kg). No se observó irritación cutánea ni ocular en estudios con conejos.
Los estudios de inhalación en ratas a diversas concentraciones no revelaron ningún efecto adverso relacionado con la sustancia. Faltan estudios a largo plazo.
Las pruebas de Ames no mostraron ningún efecto genotóxico (que dañe el ADN).
No hay datos fiables disponibles sobre toxicidad reproductiva.
Referencias
- Phthalic Acid and Derivatives, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a20_181.pub2
- PRACTICAL CONSIDERATIONS IN PREPARATION OF AMINES. – https://www.sciencedirect.com/science/article/abs/pii/B9780080119137500136
- https://go.drugbank.com/categories/DBCAT000722
