Ftaalimide: eigenschappen, reacties, productie en toepassingen
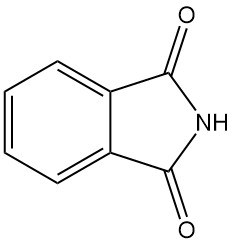
Wat is ftaalimide?
Ftaalimide, ook bekend als 1,3-dioxoisoindoline, is een organische verbinding met de chemische formule C8H5O2N. Het is een witte vaste stof die licht oplosbaar is in water en oplosbaar in basische oplossingen.
Inhoudsopgave
1. Fysieke eigenschappen van ftaalimide
Ftaalimide is een heterocyclische verbinding die witte naalden of prisma’s vormt wanneer gekristalliseerd uit oplossing en bloedplaatjes door sublimatie.
Het heeft een beperkte oplosbaarheid in water (0,3 g bij 20 °C, 0,9 g bij 50 °C en 2,2 g bij 100 °C per 100 g water). Het lost echter gemakkelijk op in azijnzuur, natriumhydroxide-oplossing en kaliumhydroxide-oplossing.
Ftaalimide sublimeert wanneer het wordt verhit boven het smeltpunt. Deze eigenschap maakt de zuivering ervan gemakkelijker.
Enkele van de fysieke eigenschappen van ftaalimide worden vermeld in de volgende tabel:
| Eigenschap | Waarde |
|---|---|
| CAS-nummer | [85-41-6] |
| Formule | C8H5NO2 |
| Moleculair gewicht | 147,14 g/mol |
| Smeltpunt | 238 °C |
| pKa | 8,30 |
| Verbrandingswarmte | 3560 kJ/mol |
| Smeltwarmte | 187,6 J/g |
| Specifieke warmtecapaciteit (100 °C) | 1,21 J g-1 K-1 |
| Dampspanning | |
| bij 120 °C | 0,10 mbar |
| bij 150 °C | 0,95 mbar |
| bij 180 °C | 5,93 mbar |
| bij 220 °C | 30,7 mbar |
| bij 254 °C | 187,6 mbar |
| Vlampunt | 214 °C |
| Ontstekingstemperatuur | 530 °C |
2. Reacties van ftaalimide
Ftaalimide reageert met basen om in water oplosbare zouten te vormen. Deze zouten kunnen vervolgens verdere reacties ondergaan met halogenen (Cl2, Br2 en I2) om de overeenkomstige N-chloor-, N-broom- of N-joodderivaten van ftaalimide te verkrijgen.
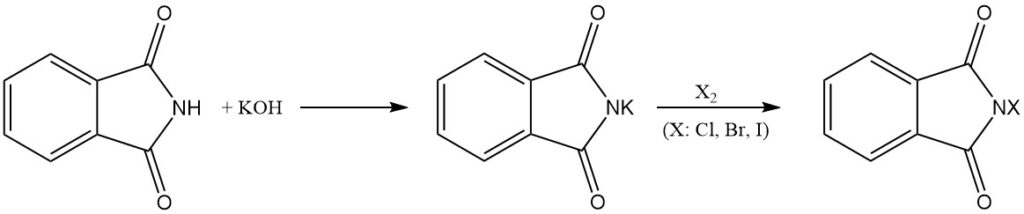
N-haloderivaten kunnen ook worden verkregen door alkalimetaalftaalimiden (bijv. kaliumftaalimide) te behandelen met hypochloorzuur (HOCl) of hypobromigzuur (HOBr).
Bij verhitting ondergaan de N-haloderivaten Hofmann-degradatie, wat resulteert in de vorming van isatoïnezuuranhydride (1) of antranilzuur (o-aminobenzoëzuur) (2).
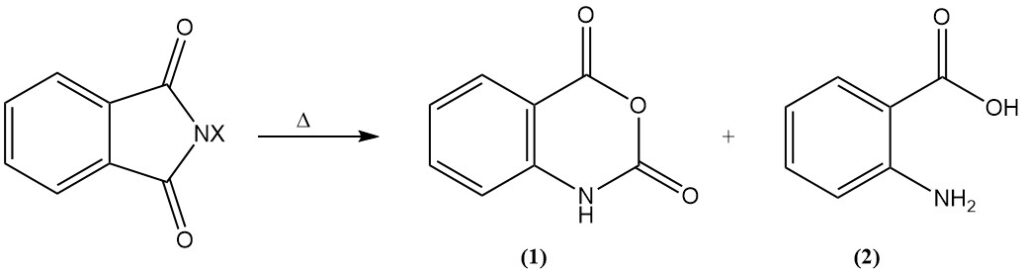
De reactie van alkalimetaalftaalimiden met alkylhaliden (RX) levert N-alkylftaalimiden op. Vervolgens hydrolyse of behandeling met hydrazine (hydrazinolyse) van deze N-alkylftaalimiden vormt primaire aminen. Deze reactievolgorde staat bekend als de Gabriel-synthese.
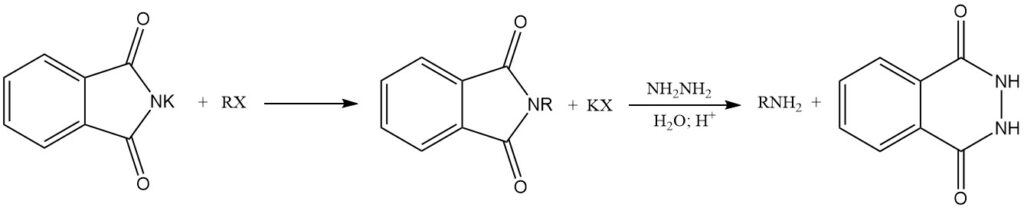
3. Industriële productie van ftaalimide
Ftaalimide wordt voornamelijk gesynthetiseerd uit ftaalzuuranhydride en ammoniak, hoewel er alternatieve methoden bestaan met behulp van ureum of o-xyleenammoxidatie.
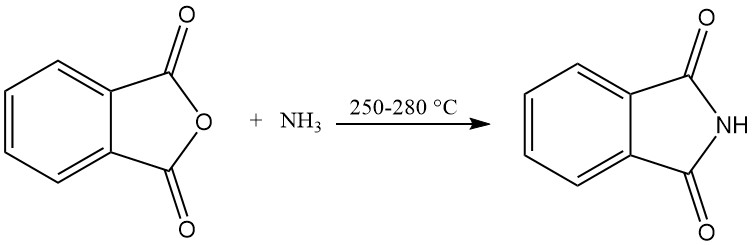
3.1. Productie van ftaalimide uit ftaalzuuranhydride en ammoniak
Continue processen worden gebruikt bij de productie van ftaalimide op industriële schaal.
Het verticale reactiebuisproces gebruikt een extern verwarmde verticale reactiebuis gevuld met pakkingmateriaal. Gesmolten ftaalimide en overtollige ammoniak worden continu in de bovenkant van de buis gevoerd en reageren bij 250–280 °C.
De reactiegassen worden vervolgens gekoeld in een sublimatiekamer, waar vast ftaalimide neerslaat en wordt afgevoerd. Overtollige ammoniak en water worden verwijderd via een uitlaatgasleiding. Dit proces levert ftaalimide op met een zuiverheid van 99% en een hoge opbrengst van 98%.
In het tegenstroomproces wordt gesmolten ftaalimide continu naar de bovenkant van een reactor gevoerd, terwijl ammoniak continu naar de onderkant wordt gevoerd. De temperatuur neemt geleidelijk toe van ongeveer 150 °C aan de bovenkant tot maximaal 270 °C aan de onderkant.
Gesmolten ftaalimide met een zuiverheid van 99% verlaat de reactor en wordt gekoeld en in vlokken verdeeld. Het kan worden opgelost in een waterige alkali-oplossing voor verder gebruik.
Het uitlaatgas van de reactorkop, dat waterdamp, gesublimeerd ftaalimide en niet-gereageerde componenten bevat, wordt op een tegenstroomse manier gewassen met gesmolten ftaalimide van de reactorbodem. Dit wasproces zuivert de uitlaatgassen en maakt het mogelijk om niet-gereageerde startmaterialen te winnen.
3.2. Productie van ftaalimide uit ftalzuuranhydride en ureum
Ftaalimide kan worden geproduceerd uit ftalzuuranhydride en ureum in een oplosmiddelvrij proces of in een oplosmiddel.
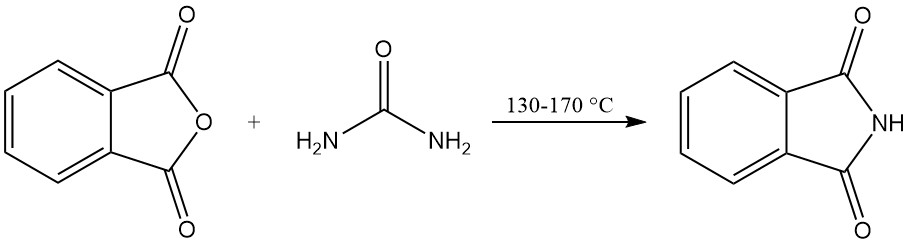
In het oplosmiddelvrije proces wordt een mengsel van ftaalzuuranhydride en ureum verhit in een afgesloten vat. De reactie verloopt bij 130–140 °C, met koolstofdioxide en waterdamp als bijproductgassen. De temperatuur stijgt tot ongeveer 160 °C vanwege de exotherme reactie.
De reactie is voltooid wanneer de gasontwikkeling stopt. Het gestolde reactiemengsel wordt vervolgens gekoeld, gemalen en direct gebruikt zonder verdere zuivering. Deze methode biedt hoge opbrengsten, meer dan 90%.
In het proces met een oplosmiddel is het oplosmiddel doorgaans een gesubstitueerde of ongesubstitueerde koolwaterstof, aromatische verbinding of heteroaromatische verbinding (bijv. n-propylbenzeen, cumeen, 1,2-dichloorbenzeen, picoline).
Het oplosmiddel moet zo worden gekozen dat ureum onoplosbaar is, terwijl ftaalzuur of anhydride een beperkte oplosbaarheid heeft. De reactie vindt plaats onder het kookpunt van het oplosmiddel (meestal 160–170 °C). Na voltooiing wordt het zuivere ftaalimideproduct geïsoleerd door filtratie en waterwassen, waarbij opbrengsten van 95–100% worden bereikt.
3.3. Productie van ftaalimide uit o-xyleen
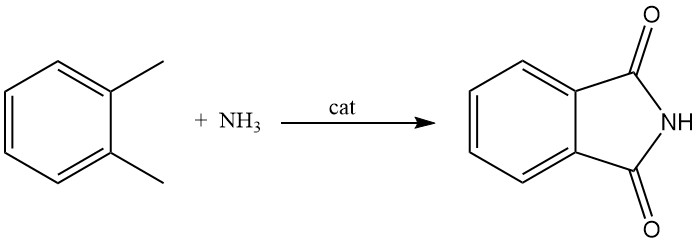
Hoewel minder gebruikelijk dan de methoden met behulp van ftaalzuuranhydride, kan ftaalimide ook worden geproduceerd uit o-xyleen. Dit proces omvat het laten reageren van o-xyleen in de gasfase met ammoniak in aanwezigheid van een metaaloxidekatalysator. Deze katalysator fungeert ook als zuurstofdonor.
Afhankelijk van de reactieomstandigheden en -controle kan dit proces selectief ftaalimide, ftaalamide of ftaalonitril produceren.
4. Toepassingen van ftaalimide
Ftaalimide wordt gebruikt als grondstof in verschillende industrieën. Het is een voorloper voor de productie van antranilzuur door Hofmann-degradatie en wordt gebruikt in de Gabriel-synthese om een breed scala aan primaire aminen te produceren.
Ftaalimide wordt gebruikt als een beschermende groep in de organische chemie, met name peptidesynthese. Door te reageren met de aminogroep voorkomt het ongewenste reacties terwijl de rest van het molecuul kan worden getransformeerd. Het kan selectief worden verwijderd om het vrije amine te geven.
Het wordt ook gebruikt als tussenproduct bij de productie van landbouwpesticiden, houtconserveringsmiddelen, bepaalde pigmenten en farmaceutische producten zoals Thalidomide, Amphotalide, Taltrimide, Talmetoprim en Apremilast.
5. Toxicologie van ftaalimide
Hoewel gegevens over de toxiciteit van ftaalimide beperkt zijn, suggereert de beschikbare informatie dat het een lage toxiciteit heeft.
Ftaalimide wordt in het lichaam afgebroken tot ftaalzuur en ammoniak.
Studies met ratten en muizen wijzen op een lage acute orale toxiciteit (LD50 > 5000 mg/kg). Er werd geen huid- of oogirritatie waargenomen in konijnenstudies.
Inhalatiestudies bij ratten bij verschillende concentraties lieten geen aan de stof gerelateerde bijwerkingen zien. Langetermijnstudies ontbreken.
Ames-testen lieten geen genotoxische (DNA-beschadigende) effecten zien.
Er zijn geen betrouwbare gegevens over reproductietoxiciteit beschikbaar.
Referenties
- Phthalic Acid and Derivatives, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a20_181.pub2
- PRACTICAL CONSIDERATIONS IN PREPARATION OF AMINES. – https://www.sciencedirect.com/science/article/abs/pii/B9780080119137500136
- https://go.drugbank.com/categories/DBCAT000722
