Phthalimid: Eigenschaften, Reaktionen, Herstellung und Verwendung
Was ist Phthalimid?
Phthalimid, auch bekannt als 1,3-Dioxoisoindolin, ist eine organische Verbindung mit der chemischen Formel C8H5O2N. Es ist ein weißer Feststoff, der in Wasser leicht löslich und in basischen Lösungen löslich ist.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Phthalimid
Phthalimid ist eine heterozyklische Verbindung, die beim Kristallisieren aus einer Lösung weiße Nadeln oder Prismen und beim Sublimationsvorgang Plättchen bildet.
Die Löslichkeit in Wasser ist begrenzt (0,3 g bei 20 °C, 0,9 g bei 50 °C und 2,2 g bei 100 °C pro 100 g Wasser). Es löst sich jedoch leicht in Essigsäure, Natriumhydroxidlösung und Kaliumhydroxidlösung.
Phthalimid sublimiert, wenn es über seinen Schmelzpunkt erhitzt wird. Diese Eigenschaft erleichtert seine Reinigung.
Einige der physikalischen Eigenschaften von Phthalimid sind in der folgenden Tabelle aufgeführt:
| Eigenschaft | Wert |
|---|---|
| CAS-Nummer | [85-41-6] |
| Formel | C8H5NO2 |
| Molekulargewicht | 147,14 g/mol |
| Schmelzpunkt | 238 °C |
| pKa | 8,30 |
| Verbrennungswärme | 3560 kJ/mol |
| Schmelzwärme | 187,6 J/g |
| Spezifische Wärmekapazität (100 °C) | 1,21 J g-1 K-1 |
| Dampfdruck | |
| bei 120 °C | 0,10 mbar |
| bei 150 °C | 0,95 mbar |
| bei 180 °C | 5,93 mbar |
| bei 220 °C | 30,7 mbar |
| bei 254 °C | 187,6 mbar |
| Flammpunkt | 214 °C |
| Zündtemperatur | 530 °C |
2. Reaktionen von Phthalimid
Phthalimid reagiert mit Basen zu wasserlöslichen Salzen. Diese Salze können dann weitere Reaktionen mit Halogenen (Cl2, Br2 und I2) eingehen, um die entsprechenden N-Chlor-, N-Brom- oder N-Iod-Derivate von Phthalimid zu ergeben.
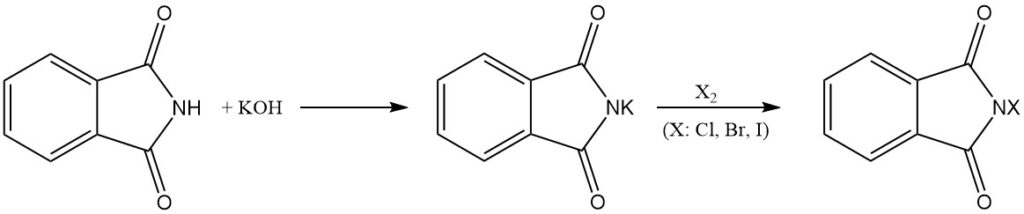
N-Halogenderivate können auch durch Behandlung von Alkalimetallphthalimiden (z. B. Kaliumphthalimid) mit hypochloriger (HOCl) oder hypobromiger (HOBr) Säure gewonnen werden.
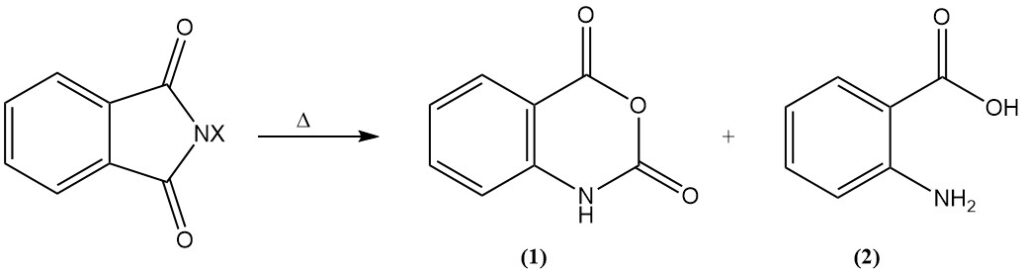
Beim Erhitzen unterliegen die N-Halogenderivate einem Hofmann-Abbau, wobei entweder Isatosäureanhydrid (1) oder Anthranilsäure (o-Aminobenzoesäure) (2) entsteht.
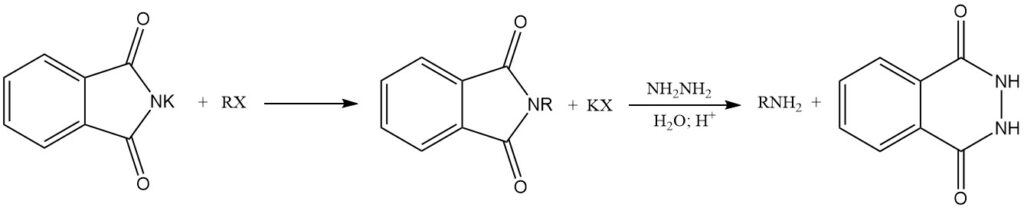
Die Reaktion von Alkalimetallphthalimiden mit Alkylhalogeniden (RX) ergibt N-Alkylphthalimide. Durch anschließende Hydrolyse oder Behandlung mit Hydrazin (Hydrazinolyse) dieser N-Alkylphthalimide entstehen primäre Amine. Diese Reaktionsfolge wird als Gabriel-Synthese bezeichnet.
3. Industrielle Herstellung von Phthalimid
Phthalimid wird hauptsächlich aus Phthalsäureanhydrid und Ammoniak synthetisiert, obwohl es alternative Methoden unter Verwendung von Harnstoff oder o-Xylol-Ammoxidation gibt.
3.1. Herstellung von Phthalimid aus Phthalsäureanhydrid und Ammoniak
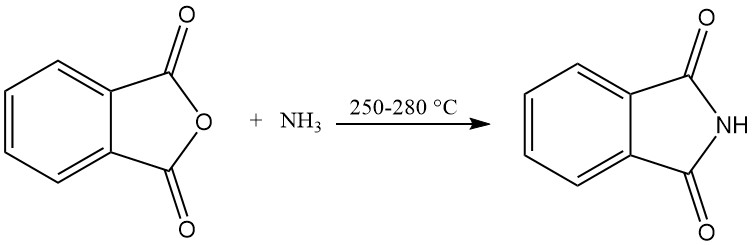
Bei der großtechnischen Herstellung von Phthalimid werden kontinuierliche Verfahren eingesetzt.
Beim vertikalen Reaktionsrohrverfahren wird ein von außen beheiztes vertikales Reaktionsrohr verwendet, das mit Füllmaterial gefüllt ist. Geschmolzenes Phthalsäureanhydrid und überschüssiges Ammoniak werden kontinuierlich in den oberen Teil des Rohrs eingeleitet und reagieren bei 250–280 °C.
Die Reaktionsgase werden dann in einer Sublimationskammer abgekühlt, wo sich festes Phthalimid absetzt und abgelassen wird. Überschüssiges Ammoniak und Wasser werden durch ein Abgasrohr entfernt. Dieses Verfahren ergibt Phthalimid mit einer Reinheit von 99 % und einer hohen Ausbeute von 98 %.
Beim Gegenstromverfahren wird geschmolzenes Phthalsäureanhydrid kontinuierlich in den oberen Teil eines Reaktors eingeleitet, während Ammoniak kontinuierlich in den unteren Teil eingeleitet wird. Die Temperatur steigt allmählich von etwa 150 °C oben auf maximal 270 °C unten an.
Geschmolzenes Phthalimid mit einer Reinheit von 99 % verlässt den Reaktor und wird gekühlt und zu Flocken verarbeitet. Es kann zur weiteren Verwendung in einer wässrigen alkalischen Lösung gelöst werden.
Das Abgas aus dem Reaktorkopf, das Wasserdampf, sublimiertes Phthalimid und nicht umgesetzte Komponenten enthält, wird im Gegenstromverfahren mit geschmolzenem Phthalimid vom Reaktorboden gewaschen. Dieser Waschvorgang reinigt das Abgas und ermöglicht die Rückgewinnung nicht umgesetzter Ausgangsstoffe.
3.2. Herstellung von Phthalimid aus Phthalsäureanhydrid und Harnstoff
Phthalimid kann aus Phthalsäureanhydrid und Harnstoff in einem lösungsmittelfreien Verfahren oder in einem Lösungsmittel hergestellt werden.
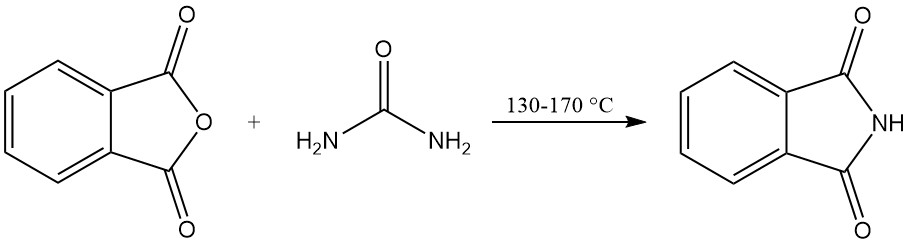
Beim lösungsmittelfreien Verfahren wird eine Mischung aus Phthalsäureanhydrid und Harnstoff in einem verschlossenen Gefäß erhitzt. Die Reaktion läuft bei 130–140 °C ab, wobei Kohlendioxid und Wasserdampf als Nebenprodukte entstehen. Aufgrund der exothermen Reaktion steigt die Temperatur auf etwa 160 °C.
Die Reaktion ist abgeschlossen, wenn die Gasentwicklung aufhört. Das erstarrte Reaktionsgemisch wird dann abgekühlt, gemahlen und ohne weitere Reinigung direkt verwendet. Diese Methode bietet hohe Ausbeuten von über 90 %.
Beim Verfahren mit Lösungsmittel ist das Lösungsmittel typischerweise ein substituierter oder unsubstituierter Kohlenwasserstoff, eine aromatische Verbindung oder eine heteroaromatische Verbindung (z. B. n-Propylbenzol, Cumol, 1,2-Dichlorbenzol, Picolin).
Das Lösungsmittel muss so gewählt werden, dass Harnstoff unlöslich ist, während Phthalsäure oder -anhydrid nur eine begrenzte Löslichkeit aufweisen. Die Reaktion findet unterhalb des Siedepunkts des Lösungsmittels statt (normalerweise 160–170 °C). Nach Abschluss wird das reine Phthalimidprodukt durch Filtration und Wasserwäsche isoliert, wodurch Ausbeuten von 95–100 % erreicht werden.
3.3. Herstellung von Phthalimid aus o-Xylol
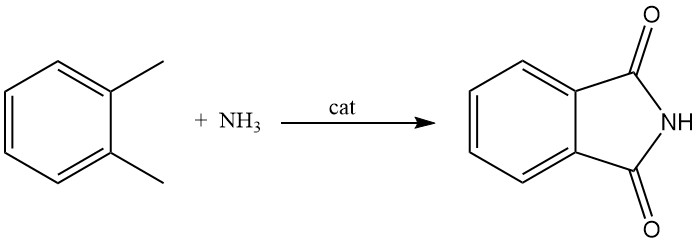
Obwohl weniger gebräuchlich als die Verfahren mit Phthalsäureanhydrid, kann Phthalimid auch aus o-Xylol hergestellt werden. Bei diesem Verfahren wird o-Xylol in der Gasphase in Gegenwart eines Metalloxidkatalysators mit Ammoniak umgesetzt. Dieser Katalysator wirkt auch als Sauerstoffspender.
Je nach Reaktionsbedingungen und -steuerung kann dieses Verfahren selektiv Phthalimid, Phthalamid oder Phthalonitril produzieren.
4. Verwendung von Phthalimid
Phthalimid wird in mehreren Industrien als Rohstoff verwendet. Es ist ein Vorläufer für die Herstellung von Anthranilsäure durch Hofmann-Abbau und wird in der Gabriel-Synthese zur Herstellung einer breiten Palette primärer Amine verwendet.
Phthalimid wird als Schutzgruppe in der organischen Chemie verwendet, insbesondere bei der Peptidsynthese. Durch die Reaktion mit der Aminogruppe verhindert es unerwünschte Reaktionen, während der Rest des Moleküls umgewandelt werden kann. Es kann selektiv entfernt werden, um das freie Amin zu erhalten.
Es wird auch als Zwischenprodukt bei der Herstellung von landwirtschaftlichen Pestiziden, Holzschutzmitteln, bestimmten Pigmenten und Arzneimitteln wie Thalidomid, Amphotalid, Taltrimid, Talmetoprim und Apremilast verwendet.
5. Toxikologie von Phthalimid
Obwohl nur wenige Daten zur Toxizität von Phthalimid vorliegen, deuten die verfügbaren Informationen darauf hin, dass es nur eine geringe Toxizität aufweist.
Phthalimid wird im Körper in Phthalsäure und Ammoniak abgebaut.
Studien mit Ratten und Mäusen weisen auf eine geringe akute orale Toxizität hin (LD50 > 5000 mg/kg). In Studien mit Kaninchen wurden keine Haut- oder Augenreizungen beobachtet.
Inhalationsstudien an Ratten mit verschiedenen Konzentrationen ergaben keine substanzbedingten Nebenwirkungen. Langzeitstudien fehlen.
Ames-Tests zeigten keine genotoxischen (DNA-schädigenden) Wirkungen.
Es liegen keine zuverlässigen Daten zur Reproduktionstoxizität vor.
Referenzen
- Phthalic Acid and Derivatives, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a20_181.pub2
- PRACTICAL CONSIDERATIONS IN PREPARATION OF AMINES. – https://www.sciencedirect.com/science/article/abs/pii/B9780080119137500136
- https://go.drugbank.com/categories/DBCAT000722
