Ftalonitrile: proprietà, reazioni, produzione e usi
Cos’è il ftalonitrile?
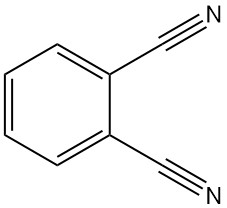
Il ftalonitrile, noto anche come 1,2-dicianobenzene o 1,2-benzenedicarbonitrile, è un composto organico con formula C8H4N2. È una polvere cristallina con un leggero colore giallo-grigiastro e un leggero odore aromatico, simile al benzonitrile.
Il ftalonitrile fu scoperto per la prima volta nel 1896, durante la diazotazione del 2-amminobenzonitrile.
Sommario
1. Proprietà fisiche del ftalonitrile
Il ftalonitrile è un solido cristallino che non è solubile in acqua (circa 1 g/L) ma è solubile in solventi organici come etanolo, acetone, nitrobenzene, benzonitrile ed etere.
Il ftalonitrile non può essere distillato e subisce polimerizzazione quando riscaldato oltre il suo punto di fusione. Non è esplosivo e la sua accensione è difficile, ma la polvere può esplodere.
La tabella 1 presenta le importanti proprietà fisiche del ftalonitrile.
| Proprietà | Valore |
|---|---|
| Numero CAS | [91-15-6] |
| Formula | C6H4N2 |
| Peso molecolare | 128,14 g/mol |
| Punto di fusione | 141 °C |
| Punto di ebollizione | 304,5 °C (decomposizione) |
| Densità | 1,238 g/cm3 |
| Densità apparente | ≈ 0,5 g/cm3 |
| Punto di infiammabilità | 162 °C |
| Calore di combustione | 4013 kJ/mol |
| Calore di evaporazione | 67 kJ/mol |
| Capacità termica specifica (30 °C) | 1,30 J g-1 K-1 |
| Pressione di vapore (20 °C) | 0,05 mbar |
| Temperatura di autoaccensione | > 580 °C |
2. Reazioni del ftalonitrile
Il ftalonitrile subisce diverse importanti reazioni tipiche dei gruppi nitrilici e dei composti aromatici, alcuni dei quali sono utilizzati nell’industria.
Il ftalonitrile reagisce con vari precursori metallici, come il cloruro di rame, a una temperatura di circa 180 °C in un solvente per formare pigmenti di ftalocianina intensamente colorati e durevoli.
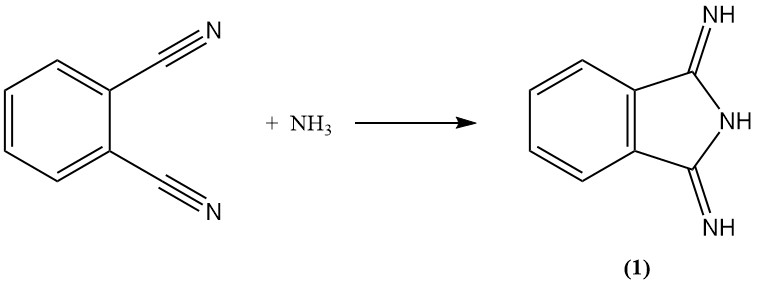
Il ftalonitrile reagisce con l’ammoniaca per formare diiminoisoindolina (1). Questo intermedio può quindi essere ulteriormente condensato con composti metilenici attivi per produrre pigmenti gialli commercialmente importanti.
Il ftalonitrile può partecipare alle reazioni di polimerizzazione quando combinato con promotori specifici, come composti contenenti gruppi sulfidrilici. Questa reazione ha potenziali applicazioni per la creazione di nuovi materiali.
In condizioni specifiche, possono verificarsi reazioni allo stato solido tra il ftalonitrile e altri composti. Ad esempio, il drogaggio del ftalonitrile con diiminoisoindolina può indurre reattività termica, portando alla formazione di ftalocianina.
A temperature elevate al di sopra del punto di fusione, il ftalonitrile può subire polimerizzazione, dove le sue singole molecole si legano per formare catene più grandi, creando un materiale polimerico a base di ftalonitrile.
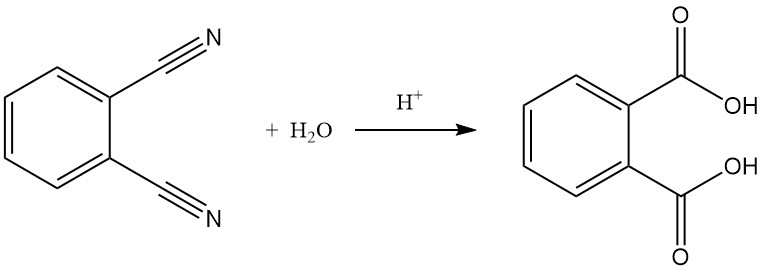
L’idrolisi del ftalonitrile in acido ftalico è possibile, specialmente in condizioni difficili come acidi forti e temperature elevate.
Il ftalonitrile può subire limitate reazioni di sostituzione aromatica come alogenazione, nitrazione, solfonazione, acilazione e alchilazione rispetto a un semplice anello aromatico come il benzene a causa dell’effetto disattivante dei gruppi nitrilici.
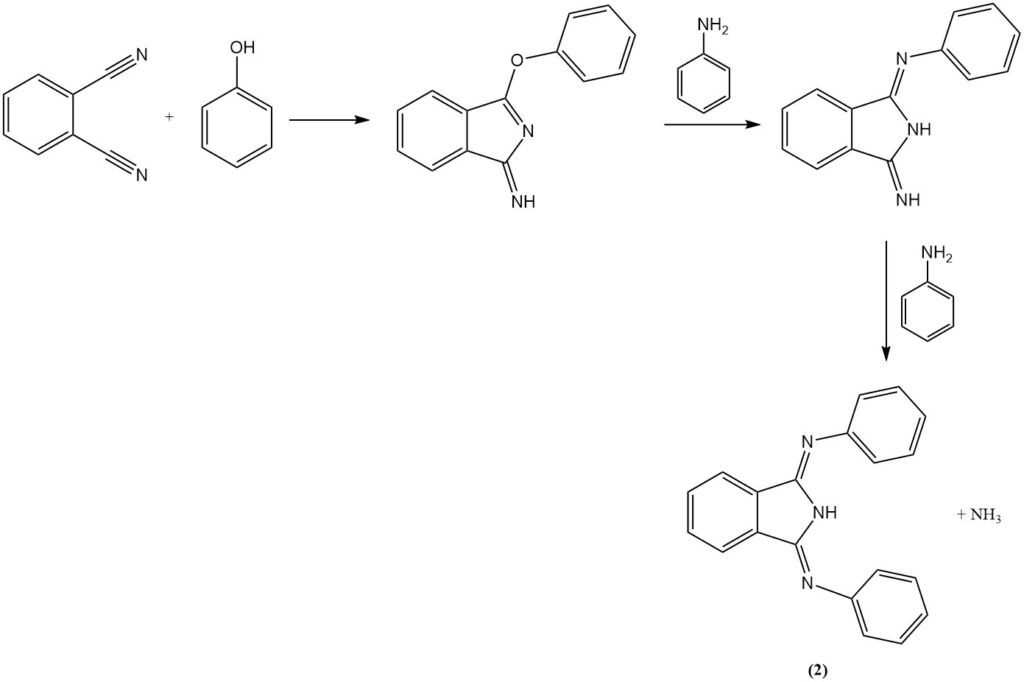
La reazione del ftalonitrile con anilina in presenza di fenolo produce un composto eterociclico (2) e con diammine produce macroeterocicli contenenti azoto (esazocielani) (3).
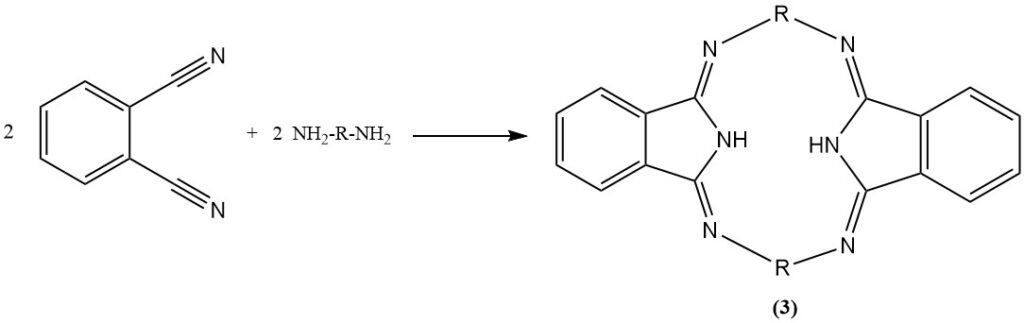
È anche possibile idrogenare i gruppi nitrilici del ftalonitrile per produrre un derivato diamminico.
3. Produzione industriale del ftalonitrile
Il ftalonitrile è prodotto commercialmente da o-xilene, acido ftalico, anidride ftalica, ftalamide o ftalimmide.
3.1. Produzione del ftalonitrile da o-xilene
Commercialmente, il ftalonitrile è prodotto principalmente da o-xilene mediante un processo chiamato ammossidazione. Questa reazione in fase gassosa continua e monostadio utilizza un reattore a letto fluidizzato per una conversione efficiente.
Nel processo di ammossidazione, le miscele di ossidi metallici contenenti vanadio, antimonio, cromo e molibdeno supportate su allumina o silice sono comunemente utilizzate come catalizzatori. Possono essere aggiunti ossidi di ferro, tungsteno e metalli alcalini per migliorare l’attività.
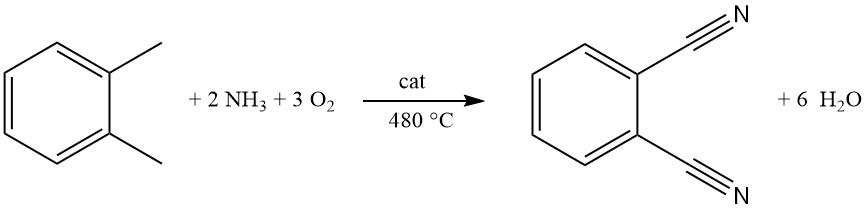
Una miscela gassosa di o-xilene, ammoniaca e ossigeno viene immessa nel reattore attraverso una piastra di distribuzione. La temperatura ottimale per questo processo senza pressione è di circa 480 °C.
Temperature più basse aumentano i sottoprodotti come ftalamide e ftalimmide (fino al 10%), mentre temperature più alte (>500 °C) portano alla combustione dell’ammoniaca. I sistemi di raffreddamento integrati mantengono una temperatura costante nonostante la reazione altamente esotermica.
I gas di reazione caldi vengono spenti con una sospensione acquosa di ftalonitrile in un sedimentatore di prodotto. La miscela raffreddata viene depositata e decantata per separare e asciugare il prodotto ftalonitrile. Questo prodotto ad alta purezza con contenuto di acido/ftalimmide < 0,1% e contenuto di acqua < 0,1% può essere utilizzato direttamente per la produzione di pigmenti di ftalocianina, ottenendo rese dell’80-85%.
L’ammoniaca viene recuperata dal flusso di gas post-decantatore, che contiene NH3, CO2, CO, N2 e tracce di HCN, utilizzando un impianto dedicato al recupero dell’ammoniaca. Il gas di scarico rimanente viene bruciato e l’ammoniaca recuperata viene riciclata nel processo.
L’o-xilene non reagito e l’o-toluonitrile intermedio possono essere isolati o reimmessi nel reattore per la conversione completa in ftalonitrile.
Studi su impianti pilota hanno esplorato un processo di ammonolisi ossidativa continua per la sintesi di ftalonitrile da o-xilene. Questo processo utilizza un catalizzatore di ossido di vanadio-ossido di molibdeno su supporto di allumina o silice a 350-450 °C.
Qui, il catalizzatore di ossido di metallo agisce come ossidante, con una porzione continuamente rimossa, riossidata e riciclata. La tempra del ftalonitrile e la gestione dei sottoprodotti sono simili al processo di ammossidazione.
Sottoprodotti come o-toluonitrile, ftalammide e ftalimmide possono essere reimmessi nel reattore principale o convertiti in ftalonitrile in un reattore separato a una temperatura di 400 °C in presenza di ammoniaca e un catalizzatore di fosfato di boro-allumina.
L’ammoniaca viene recuperata dalla miscela di gas residua, che contiene NH3, CO2, CO, N2 e tracce di HCN, e riciclata nel reattore. I gas nocivi come CO e HCN vengono bruciati in un rigeneratore, mentre N2 e CO2 vengono eliminati dal flusso di processo.
3.2. Produzione di ftalonitrile da derivati dell’acido ftalico
Il ftalonitrile può anche essere sintetizzato da vari derivati dell’acido ftalico, tra cui acido ftalico, anidride ftalica, ftalamide e ftalimmide. Questo processo comporta una reazione in fase gassosa con eliminazione di ammoniaca e acqua a temperature comprese tra 300 e 500 °C in presenza di un catalizzatore.
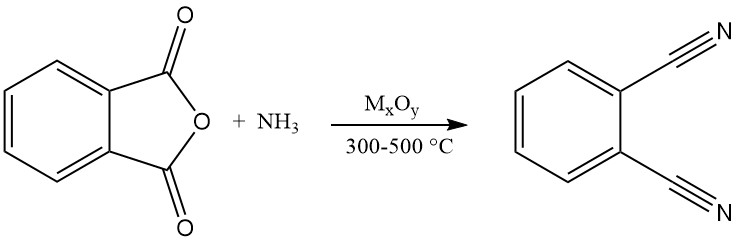
La letteratura brevettuale suggerisce l’uso di catalizzatori di ossido metallico supportati su silice, allumina, fosfati, silicati, borati o allumina basica. Esempi includono ossidi di torio, rame, berillio, zirconio o tungsteno.
L’anidride ftalica fusa viene prima riscaldata a circa 160 °C e vaporizzata in un apparato dedicato. Il gas circolante preriscaldato contenente un’elevata concentrazione di ammoniaca (NH3 ≈ 90%) viene quindi introdotto nel vaporizzatore.
Questa miscela reagisce a una pressione quasi atmosferica a una temperatura compresa tra 350 e 400 °C in un reattore a letto fisso posizionato a valle del vaporizzatore. In questo reattore viene solitamente utilizzato un catalizzatore di allumina.
Il gas di reazione caldo che esce dal reattore viene spento con acqua. Il ftalonitrile viene quindi separato dalla sospensione acquosa risultante mediante processi di decantazione ed essiccazione. La concentrazione di ammoniaca nel gas circolante viene mantenuta a circa il 90% mediante l’aggiunta continua di ammoniaca.
Il ftalonitrile può essere formato mediante disidratazione della ftalamide utilizzando alogenuri acidi come fosgene o cloruro di tionile. Tuttavia, questo metodo richiede ulteriori passaggi per impedire l’idrolisi della ftalamide da parte dell’acido generato.
Le tecniche utilizzate per superare questo problema includono l’aggiunta di diluenti (benzene, clorobenzene) o l’impiego di ammine terziarie (N,N-dietil-o-toluidina, piridina) o ammine secondarie acilate (N-metilformammide) per neutralizzare l’acido.
Questo processo alternativo generalmente comporta procedure complesse e ulteriore manipolazione chimica, rendendolo meno favorevole per la produzione su larga scala rispetto ai percorsi stabiliti.
4. Utilizzi del ftalonitrile
Il ftalonitrile è utilizzato come materia prima nella produzione di pigmenti di ftalocianina, sbiancanti fluorescenti e sensibilizzanti fotografici.
La produzione di pigmenti di ftalocianina, noti per i loro colori intensi e la loro eccezionale durata, è l’applicazione industriale più importante del ftalonitrile. La reazione del ftalonitrile con vari precursori metallici produce un’ampia gamma di colori. Questi pigmenti sono utilizzati in vernici, materie plastiche, tessuti e inchiostri.
5. Tossicologia del ftalonitrile
Tossicità acuta
- LD50 orale (ratto): 30-125 mg/kg.
- Non è stata osservata alcuna irritazione cutanea o oculare nei conigli.
- Non vi sono prove di sensibilizzazione nei lavoratori coinvolti nella produzione e nell’uso del ftalonitrile.
Tossicità a dosi ripetute
Sono stati osservati effetti neurotossici (convulsioni, aumento dell’eccitazione) nei ratti e nei topi a seguito di ripetute esposizioni orali.
Sono stati segnalati un aumento dell’attività e una diminuzione del peso corporeo in uno studio di neurotossicità sui ratti di 13 settimane a 10 e 25 mg di ftalonitrile/kg/giorno. Non è stato trovato alcun collegamento istopatologico per i cambiamenti comportamentali. Il NOAEL in questo studio era di 3 mg/kg/giorno.
L’esposizione professionale ha causato convulsioni epilettiformi ritardate (ore o giorni) della durata di minuti nei lavoratori.
Gli esami clinici di 81 lavoratori con un’esposizione media di 8,5 anni al ftalonitrile (inclusi 11 con intossicazioni acute) non hanno mostrato anomalie nella chimica clinica, ematologia, neurologia o EEG.
Anche l’esposizione cutanea può essere rilevante.
Le misure anticianuro non sono considerate efficaci a causa della mancanza di metabolismo del cianuro.
Genotossicità
Il ftalonitrile non è risultato mutageno nel test di Ames o nel test di mutazione genetica CHO/HGPRT.
Risultati negativi nel test del micronucleo del topo.
Non sono state osservate aberrazioni cromosomiche aumentate nei lavoratori, inclusi quelli con intossicazioni acute.
Carcinogenicità
Studi segnalano l’induzione di leucemia nei ratti e nei topi dopo somministrazione orale, sottocutanea e percutanea (topi). Tuttavia, descrizioni vaghe degli studi limitano la valutazione conclusiva.
Riferimenti
- Phthalic Acid and Derivatives, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a20_181.pub2
- https://www.sciencedirect.com/science/article/abs/pii/S0032386118302945
- https://pubchem.ncbi.nlm.nih.gov/compound/Phthalonitrile
- Reaction of O-phthalonitrile with aniline. – https://link.springer.com/article/10.1007/BF00954275
