Acido acrilico: proprietà, reazioni, produzione e usi
Cos’è l’acido acrilico?
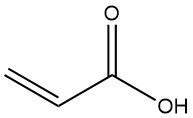
L’acido acrilico, noto anche come acido 2-propenoico, è l’acido carbossilico insaturo più semplice con la formula CH2=CHCOOH. È un liquido incolore, infiammabile, volatile e leggermente tossico.
Per prevenire la polimerizzazione, le preparazioni commerciali in genere incorporano idrochinone o il suo etere monometilico.
In passato, la produzione industriale di acido acrilico prevedeva vari metodi come l’idrolisi dell’acrilonitrile e il processo Reppe modificato. Tuttavia, significativi progressi nell’ossidazione catalitica, in particolare nella conversione del propene in acido acrilico tramite acroleina, hanno quasi completamente soppiantato queste tecniche precedenti.
Sommario
1. Proprietà fisiche dell’acido acrilico
L’acido acrilico è un liquido trasparente e incolore con un punto di ebollizione di 141,0 °C a 101,3 kPa e un punto di fusione di 13,5 °C, che forma aghi cristallini quando solidificato.
Presenta un’elevata miscibilità con acqua, alcoli, esteri e vari altri solventi organici, rendendolo facilmente solubile in queste sostanze.
Di seguito sono elencate altre importanti proprietà fisiche:
| Proprietà | Valore |
|---|---|
| Massa molare | 72,06 g/mol |
| Indice di rifrazione | 1,421 |
| Densità | 1,05 g/cm³ |
| Viscosità | 1,15 mPa.s (a 25°C) |
| Temperatura critica | 380 °C |
| Pressione critica | 5,06 Mpa |
| Costante di dissociazione | 5,46 x 10-5 (a 25°C) |
| pKa | 4,25 |
2. Reazioni chimiche dell’acido acrilico
L’acido acrilico presenta reazioni distintive caratteristiche sia dei composti insaturi che degli acidi carbossilici alifatici. La sua elevata reattività può essere attribuita alla presenza di due centri insaturi in posizione coniugata.
L’atomo di carbonio β, polarizzato dal gruppo carbonilico, agisce come elettrofilo, consentendo l’aggiunta di vari nucleofili e composti di idrogeno attivo al gruppo vinilico.
Inoltre, il doppio legame carbonio-carbonio partecipa alle reazioni di addizione avviate da radicali, alle reazioni di Diels-Alder con dieni e alle reazioni di polimerizzazione.
Per quanto riguarda la funzione carbossilica, subisce reazioni di spostamento tipiche degli acidi alifatici, come l’esterificazione.
Quando le funzioni vinilica e carbossilica reagiscono congiuntamente, specialmente con reagenti bifunzionali, spesso fungono da percorsi convenienti per formare sostanze policicliche ed eterocicliche.
L’acido acrilico subisce facilmente la polimerizzazione, che può essere catalizzata da calore, luce e perossidi, ma inibita da stabilizzanti come l’etere monometilico dell’idrochinone o l’idrochinone stesso.
In particolare, questi inibitori fenolici sono efficaci solo in presenza di ossigeno. Il processo di polimerizzazione dell’acido acrilico è altamente esotermico e può essere estremamente vigoroso.
2.1. Reazioni di addizione
L’acido acrilico subisce facilmente reazioni di addizione con varie sostanze, come idrogeno, alogenuri di idrogeno e acido cianidrico, che vengono comunemente aggiunti alle olefine:
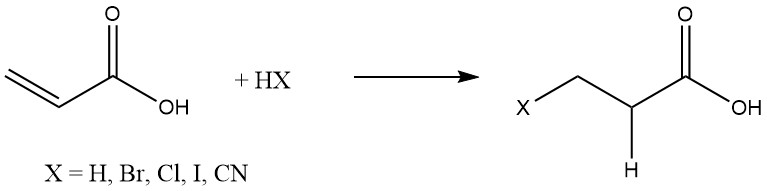
Le aggiunte di Michael di sostanze organiche si verificano in presenza di catalizzatori basici come ammine terziarie, sali di ammonio quaternari e alcossidi alcalini.
L’ammoniaca e le ammine, essendo sufficientemente basiche, possono reagire senza la necessità di un catalizzatore. L’aggiunta di una singola molecola di NH3 può essere ottenuta utilizzando una soluzione acquosa di ammoniaca e carbonato di ammonio.
L’aggiunta di ammine aromatiche o ammidi e ammine primarie tert-alchiliche è promossa più efficacemente dagli acidi. Le ammine possono attaccare sia la funzione vinilica che quella carbossilica, ma i prodotti risultanti da tali reazioni si decompongono per dare ammidi N-sostituite.
In condizioni basiche, anche alcoli, fenoli, acido solfidrico e tioli subiscono reazioni di addizione. L’acido solfidrico, quando combinato con catalizzatori di zolfo e polisolfuro di ammonio o ammine, dà acidi politiodipropionici. Nel frattempo, le aggiunte di idrocarburi aromatici sono promosse in modo più efficiente dagli acidi di Lewis.
Se nel prodotto di addizione sono disponibili atomi di idrogeno acidi aggiuntivi, una seconda (e terza) molecola di acido acrilico può aggiungersi. Ciò avviene nella reazione dell’acido acrilico con H2S, NH3, RNH2 e pirrolo.
Le sostanze eterocicliche sono spesso formate tramite reazioni successive della funzione carbossilica, in particolare con nucleofili bifunzionali:
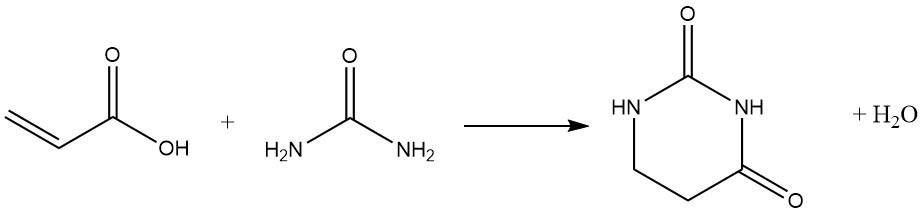
A temperature elevate o durante uno stoccaggio prolungato, l’acido acrilico dimerizza:
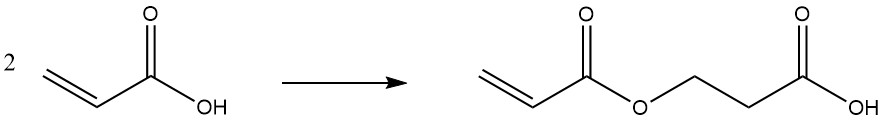
2.2. Reazioni del gruppo carbossilico
L’acido acrilico può essere facilmente convertito nei suoi sali corrispondenti, trasformato in anidride acrilica mediante reazione con anidride acetica o convertito in cloruro di acriloile mediante reazione con cloruro di benzoile o tionile. L’esterificazione dell’acido acrilico e la transesterificazione degli esteri acrilici sono reazioni economicamente significative.
Altri esempi di gruppo carbossilico sono:
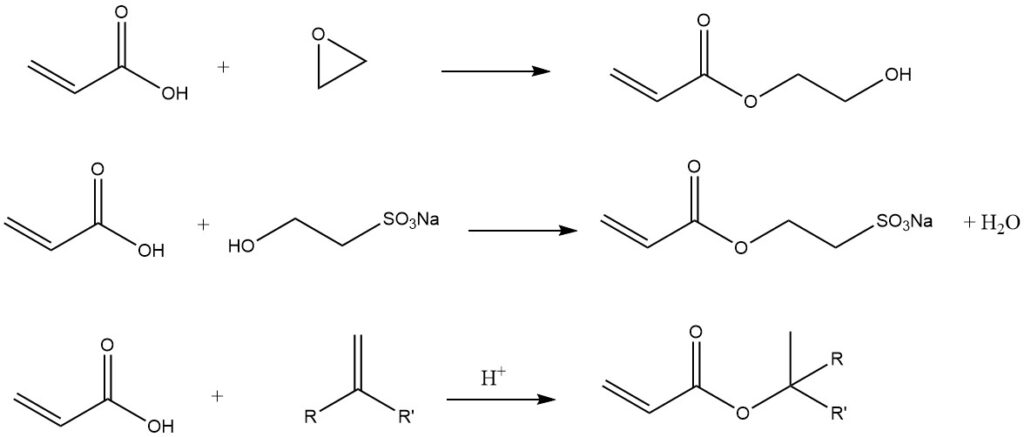
3. Produzione di acido acrilico
L’acido acrilico commerciale è prodotto principalmente dal propene, che è anche utilizzato come materia prima per la produzione di acroleina. In passato, sono stati impiegati vari processi per la produzione di acido acrilico e dei suoi esteri, alcuni dei quali sono ancora in uso in misura limitata.
1. Processi basati su acetilene:
L’acido acrilico e i suoi esteri possono essere sintetizzati dall’acetilene in presenza di acido e nichel carbonile a pressione atmosferica e 40 °C:
4 C2H2 + 4 ROH + 2 HCl + Ni(CO)4 → 4 H2C=CHCOOR + NiCl2 + H2
Tuttavia, questo metodo è stato abbandonato a causa delle sfide associate alla gestione del nichel carbonile tossico e corrosivo.
2. Processo Reppe ad alta pressione:
BASF ha impiegato un processo che utilizza un catalizzatore bromuro di nichel-bromuro di rame(II) a circa 14 MPa e 200 °C per produrre acido acrilico da acetilene, CO e acqua. Tuttavia, questo processo è stato sostituito dalla più economica ossidazione diretta del propene.
3. Idrolisi dell’acrilonitrile:
Questo metodo, che prevede l’idrolisi dell’acrilonitrile, è stato ritenuto economicamente poco attraente a causa della bassa resa e delle grandi quantità di rifiuti di NH4HSO4. Alcune aziende hanno abbandonato questo processo, ad eccezione di Asahi Chemical, che lo utilizza ancora.
4. Processo del chetene:
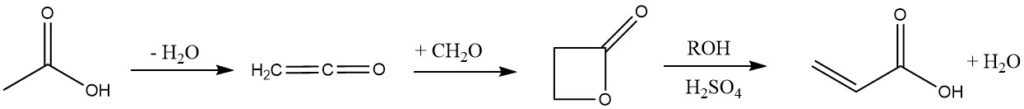
In questo processo, l’acido acetico o acetone viene pirolizzato in chetene, ma è stato abbandonato da aziende come Celanese e B. F. Goodrich a causa dei suoi numerosi passaggi e della tossicità del β-propiolattone.
5. Depolimerizzazione termica del polipropiolattone:
Novomer ha sviluppato catalizzatori proprietari per produrre polipropiolattone (PPL) come intermedio che può essere depolimerizzato termicamente in acido acrilico o esteri acrilici, affrontando le sfide del trasporto e riducendo la complessità di produzione.
6. Processo di etilene cianidrina:
L’etilene cianidrina viene generata aggiungendo acido cianidrico all’ossido di etilene, quindi disidratata cataliticamente per produrre acido acrilico utilizzando acido solforico. Questo processo è stato utilizzato da Union Carbide e Rohm & Haas ma abbandonato a causa di difficoltà di gestione con HCN e rifiuti di NH4HSO4.
7. Ossidazione parziale di etere allilico:
Un sistema catalitico basato su ossido di manganese mesoporoso drogato con Li può catalizzare l’ossidazione parziale aerobica di etere diallilico in acrilato di allile in condizioni ambientali in solvente acetonitrile.
3.1. Produzione di acido acrilico mediante ossidazione del propene
La produzione di acido acrilico dal propene comporta l’ossidazione catalitica eterogenea in fase vapore, utilizzando aria e vapore. Il prodotto risultante viene in genere assorbito in acqua, seguito da estrazione con un solvente adatto e quindi distillato per ottenere acido acrilico glaciale di grado tecnico.
La ricerca sui catalizzatori per l’ossidazione del propene in acido acrilico è iniziata alla fine degli anni ’50, con due metodi per l’ossidazione in fase gassosa catalizzata in modo eterogeneo del propene: processi in un unico passaggio e in due passaggi.
Nel processo in un unico passaggio, la resa è limitata, circa il 50-60% al massimo, e la durata del catalizzatore è breve a causa della presenza di ossido di tellurio, che tende a sublimare.
Il processo in due passaggi prevede diverse condizioni di reazione e catalizzatori per ottenere una conversione e una selettività ottimali in ogni passaggio. I catalizzatori di prima fase vengono utilizzati per l’ossidazione selettiva del propene con acroleina, producendo oltre l’85% di acroleina e acido acrilico.
I primi catalizzatori di seconda fase per l’ossidazione dell’acroleina in acido acrilico erano basati principalmente su ossidi di cobalto-molibdeno, che fornivano rese inferiori al 70% in moli. Tuttavia, ulteriori ricerche hanno dimostrato che vari catalizzatori multicomponenti di ossido metallico, tra cui molibdeno e vanadio, insieme ad altri elementi e vettori, potrebbero aumentare l’attività e la resa.
Il recupero e la purificazione dell’acido comportano il raffreddamento del gas effluente e il suo lavaggio con acqua per ottenere una soluzione acquosa di acido acrilico. Questa soluzione viene quindi purificata tramite estrazione con un solvente organico, distillazione e aggiunta di inibitori per impedire la polimerizzazione durante la distillazione. La purezza dell’acido acrilico risultante di solito supera il 99,5% in peso, con una resa purificata di circa il 98%.
Sono stati esplorati diversi metodi di purificazione, come l’oligomerizzazione e l’esterificazione diretta, ma il processo di estrazione con solvente leggero rimane il più adatto per gli impianti commerciali grazie alla sua efficienza energetica e alla qualità del prodotto. Altri metodi non sono stati ampiamente adottati a livello commerciale a causa del loro elevato consumo energetico o di problemi di qualità del prodotto.
3.2. Acido acrilico di origine biologica
Le tecnologie di origine biologica per la produzione di acido acrilico comportano la fermentazione di sostanze derivate dalla biomassa, come gli zuccheri, per produrre acido lattico, acido 3-idrossipropanoico e 3-idrossipropanale. Successivamente, questi intermedi di fermentazione subiscono una trasformazione chimica per produrre acido acrilico.
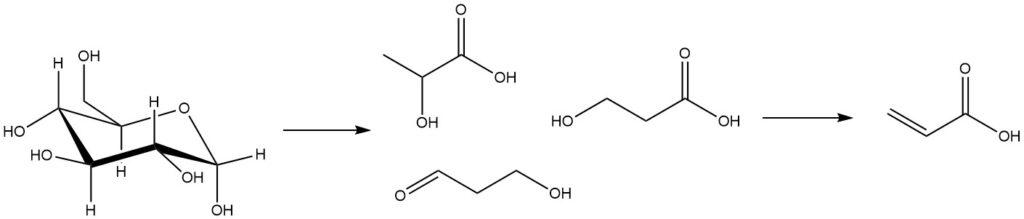
La disidratazione dell’acido lattico intermedio avviene in genere tramite acetossilazione, dove l’acido acetico viene utilizzato come solvente azeotropico.
Dal 2008 al 2010 sono state avviate diverse tecnologie biobased per la produzione di acido acrilico, utilizzando materie prime come glucosio, glicole, acido lattico e biomassa.
Joint venture e singole aziende, come Cargill/Novozymes/BASF, OPXBio/Dow, Arkema/THE, Nippon Shokubai, Geneomatica e Choren, sono state attivamente coinvolte nello sviluppo di queste tecnologie. Si prevede che alcuni di questi approcci saranno commercializzati entro il 2025.
Varie joint venture, tra cui Cargill/Novozymes/BASF e OPXBio/Dow, si concentrano sulla progettazione di enzimi o microrganismi per produrre acido acrilico da materie prime rinnovabili come mais e canna da zucchero.
Arkema, in collaborazione con HTE, sta lavorando allo sviluppo di catalizzatori per la produzione di acido acrilico dal glicerolo tramite acroleina. Nippon Shokubai sta esplorando un processo in fase gassosa per produrre acido acrilico dal glicerolo ottenuto come sottoprodotto nella produzione di biodiesel da oli vegetali. Il potenziale di commercializzazione di questi processi dipende dalla disponibilità e dal prezzo del glicerolo.
L’approccio di Genomatica prevede la fermentazione dello zucchero in acido fumarico, seguita da metatesi incrociata con etilene per produrre acido acrilico. Sebbene questa tecnologia sia stata brevettata, ci sono ancora notevoli sfide tecniche da superare.
Il progresso e il successo di queste tecnologie basate sulla biologia non dipenderanno solo dai progressi tecnologici, ma anche dalle pressioni e dalle richieste della società di produrre beni e prodotti chimici da fonti rinnovabili e sostenibili.
4. Usi dell’acido acrilico
L’acido acrilico funge da intermedio nella produzione di acrilati. Gli acrilati sono un gruppo di composti derivati dall’acido acrilico e sono ampiamente utilizzati in vari settori per la loro versatilità e proprietà prestazionali.
Inoltre, l’acido acrilico e i suoi sali di sodio trovano sempre più applicazioni come flocculanti e disperdenti. Queste forme polimeriche di acido acrilico, in particolare i sali di sodio polimerici, stanno acquisendo sempre più importanza industriale grazie alle loro efficaci proprietà nel promuovere la flocculazione (aggregazione di particelle) e la dispersione (distribuzione uniforme di particelle) in vari processi e applicazioni.
A partire dal 2014, le capacità di produzione globali di acido acrilico e dei suoi esteri erano rispettivamente di oltre 5,2 milioni di tonnellate all’anno e 3,6 milioni di tonnellate all’anno.
La Cina è emersa come un mercato in forte crescita per l’acido acrilico, superando la domanda combinata in Nord America ed Europa. Tra il 2002 e il 2014, la capacità produttiva cinese di acido acrilico è quasi quadruplicata, indicando il suo ruolo significativo nel settore.
Nel 2014, il 50% del consumo totale di acido acrilico è stato utilizzato come intermedio nella produzione di esteri, mentre l’altro 50% è stato lavorato per produrre acido acetico glaciale.
5. Tossicologia e salute sul lavoro
L’acido acrilico è moderatamente tossico e altamente corrosivo. L’ingestione può causare gravi ustioni gastrointestinali e il suo vapore è irritante per gli occhi e le vie respiratorie. Il contatto con la pelle può causare ustioni. Sono disponibili i seguenti dati sulla risposta fisiologica:
- LD50: 340 mg/kg (ratto, orale)
- LC50: 3600 mg/m³ (ratto, inalazione, 5 L, 4 ore)
- LD50: 280 mg/kg (coniglio, pelle)
Il valore limite di soglia (TLV) per l’acido acrilico su una media ponderata nel tempo (TWA) è fissato a 10 ppm (parti per milione) o 30 mg/m³. Questo valore funge da linea guida per controllare i livelli di esposizione in contesti occupazionali.
Riferimento
- Acrylic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_161.pub4
