Idrochinone: produzione, reazioni e usi
Cos’è l’idrochinone?
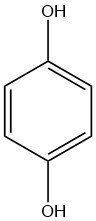
L’idrochinone, noto anche come 1,4-benzenediolo, è un solido cristallino incolore quando puro, con formula chimica C6H4(OH)2. È un diolo aromatico (un para-isomero del catecolo).
La scoperta dell’idrochinone risale al 1844, quando WOEHLER ne riferì per la prima volta l’esistenza. È un solido cristallino incolore che viene sintetizzato aggiungendo idrogeno al 1,4-benzoquinone.
L’idrochinone si trova anche in natura come idrochinone β-D-glucopiranoside (arbutina) in varie piante, come l’uva ursina, il mirtillo rosso, il mirtillo rosso americano e alcuni tipi di pera, spesso insieme al suo etere metilico, la metilarbutina.
In condizioni acide e acquose diluite e calde, l’arbutina viene facilmente idrolizzata in idrochinone e glucosio. Allo stesso modo, l’idrolisi della metilarbutina determina la formazione di idrochinone monometil etere e glucosio.
Sommario
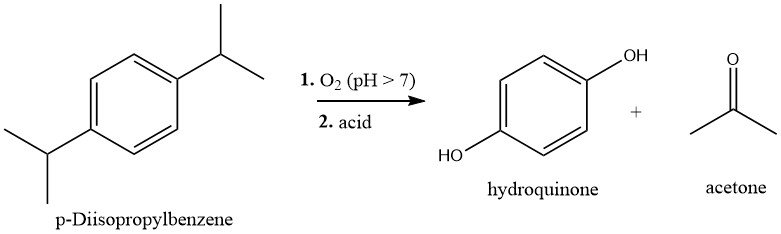
Il p-diisopropilbenzene (p-DIPB) viene sintetizzato mediante l’alchilazione di Friedel-Crafts del benzene con propene. Il p-DIPB risultante viene purificato e quindi ossidato con aria in condizioni leggermente alcaline a 80-90 °C per formare diidroperossido.
Il diidroperossido può essere estratto dalla miscela di reazione o ottenuto tramite cristallizzazione e successivamente scisso per produrre idrochinone e acetone mediante un riarrangiamento di Hock catalizzato da acido. Questo processo comporta il trattamento della soluzione di diidroperossido con catalizzatore di acido solforico (0,2-1,0%) a 60-80 °C. L’idrochinone viene quindi isolato e cristallizzato.
La resa complessiva di idrochinone, basata sul p-DIPB, è di circa l’80%.
1.2. Produzione di idrochinone mediante idrossilazione del fenolo
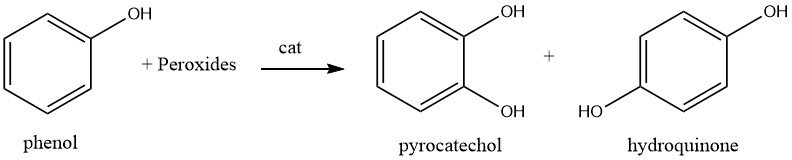
L’idrossilazione del fenolo mediante perossido di idrogeno a una temperatura di circa 80 °C e un catalizzatore come un acido minerale forte, ferro (II) o sale di cobalto (II), produce una miscela di idrochinone e catecolo. Il rapporto tra catecolo e idrochinone può variare da 3:1 a 0,1:1, con un rapporto tipico di 1,5:1 in cui il catecolo è il prodotto principale.
Il meccanismo della reazione è di natura ionica, per cui il perossido di idrogeno viene polarizzato dal catalizzatore acido forte e il fenolo viene successivamente idrossilato. Gli isomeri risultanti vengono separati mediante una serie di estrazioni e operazioni di stripping con solvente.
Il rapporto tra prodotti di idrochinone e catecolo può essere influenzato dalla presenza di superacidi o zeoliti selettive per forma. Ad esempio, l’uso di un polimero di perfluorosolfonato di Nafion modificato con vanadio nell’ossidazione del fenolo ha portato a un rapporto idrochinone-catecolo di 12,5:1.
L’uso di una zeolite selettiva per forma nell’idrossilazione del fenolo ha portato a una selettività per l’idrochinone del 99%.
1.3. Produzione di idrochinone mediante ossidazione dell’anilina
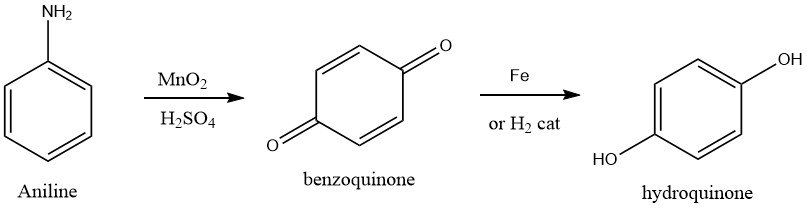
La produzione di idrochinone è stata storicamente realizzata tramite ossidazione dell’anilina, che è considerata il processo più antico conosciuto. Per ottenere questo risultato, l’anilina viene ossidata con un eccesso del 15-20% di biossido di manganese in una soluzione acquosa di acido solforico mantenuta a 0-5 °C.
Questa reazione produce p-benzochinone, che viene separato dalla miscela di reazione tramite strippaggio a vapore e raccolto. La reazione produce un sottoprodotto, il solfato di manganese, che può essere ottenuto dalla miscela di reazione impoverita e venduto per scopi agricoli.
L’idrochinone viene quindi ottenuto dall’intermedio p-benzochinone tramite riduzione con ferro a 55-65 °C o tramite idrogenazione catalitica. In genere, il prodotto di grado tecnico viene cristallizzato, isolato dal flusso acquoso tramite centrifugazione ed essiccato utilizzando un essiccatore sotto vuoto. La resa complessiva di idrochinone dall’anilina è di circa l’85%.
L’ossidazione dell’anilina è un processo discontinuo e, in quanto tale, richiede relativamente molta manodopera. Le condizioni di lavorazione sono anche altamente abrasive perché vengono utilizzati minerale di manganese macinato e ferro finemente suddiviso, che richiedono una manutenzione costante.
Lo smaltimento di sottoprodotti inorganici, che costituiscono circa l’85% del peso totale dei prodotti, pone un importante problema ambientale.
1.4. Altri processi
L’ossidazione Baeyer-Villiger di un chetone aromatico 4-idrossi-sostituito fornisce esteri carbossilati di dioli aromatici con elevata resa ed efficienza del 97%.
L’ossidazione microbiologica di benzene o fenolo è altamente selettiva e produce idrochinone con notevole selettività.
L’ossidazione dell’aria di fenolo in presenza di catalizzatore di rame fornisce p-benzochinone con selettività superiore al 90%. L’ossidazione del benzene a idrochinone può essere ottenuta utilizzando cloruro di rame (I) o titanio.
L’ossidazione del benzene indotta dall’ozono in un mezzo acquoso determina la formazione di idrochinone e p-benzochinone.
Ulteriori metodi di preparazione comportano l’idrolisi acida del nitrobenzene o p-nitrosofenolo, la carbonilazione dell’acetilene, l’ossidazione elettrochimica del benzene o del fenolo in acido solforico diluito seguita da riduzione e l’idrogenazione catalitica del nitrobenzene in soluzione acida.
Inoltre, il p-isopropenilfenolo può essere ottenuto tramite il cracking alcalino del bisfenolo A e quindi fatto reagire con perossido di idrogeno acquoso al 30% in condizioni acide per produrre idrochinone.
2. Reazioni chimiche dell’idrochinone
La maggior parte degli agenti ossidanti può facilmente convertire l’idrochinone in p-benzochinone. Anche le soluzioni acquose neutre di idrochinone si scuriscono se esposte all’aria.
La velocità di ossidazione dell’idrochinone da parte dell’aria è accelerata in una soluzione alcalina. Il prodotto di ossidazione può reagire con l’acqua per formare 1,2,4-benzentriolo, e un’ulteriore ossidazione può portare alla formazione di acidi umici.
Il potenziale redox E0 dell’idrochinone è 699 mV, con un potenziale di semionda E1/2 di 560 mV a pH 0 e 234 mV a pH 5-6. La perdita di un elettrone e l’eliminazione di un protone durante l’ossidazione dell’idrochinone danno origine a un radicale semibenzochinone relativamente stabile, che consente all’idrochinone di agire come antiossidante.
Un secondo trasferimento di un elettrone e l’eliminazione di protoni portano alla formazione di p-benzochinone. Il complesso equimolare di trasferimento di carica chinidrone è formato da idrochinone e p-benzochinone, con il complesso chinidrone che è tipicamente di colore nero-verdastro scuro e ha un punto di fusione di 171 °C.
L’idrochinone è un agente riducente con un potenziale di riduzione adatto per ridurre l’alogenuro d’argento. I granuli di alogenuro d’argento che sono stati esposti alla luce vengono ridotti molto più velocemente dei granuli non esposti o sottoesposti, a causa di cambiamenti nei cristalli di alogenuro d’argento esposti che riducono la barriera energetica per la reazione con l’idrochinone per formare argento elementare e p-benzochinone.
Il solfito di sodio viene aggiunto alla soluzione di sviluppo per prevenire la formazione di chinidrone convertendo il p-benzochinone in sodio 2,5-diidrossibenzenesolfonato, un agente di sviluppo più debole dell’idrochinone.
La reattività dell’idrochinone è generalmente simile a quella del fenolo, con uno o entrambi i gruppi idrossilici in grado di convertirsi in un etere o estere.
I derivati dell’ossigeno commercialmente importanti includono idrochinone monometil etere, idrochinone dimetil etere e idrochinone bis(2-idrossietil) etere. Gli esteri dell’idrochinone subiscono il riarrangiamento di Fries per dare idrochinoni acil-sostituiti.
L’idrochinone e i suoi eteri possono essere C-alchilati in condizioni di Friedel-Crafts per produrre una varietà di prodotti mono- e disostituiti, tra cui 2-terz-butilidrochinone, 2,5-bis[2-(2-metilbutil)]idrochinone e 2-terz-butil-4-metossifenolo (BHA).
L’idrochinone reagisce anche con alchilammine o arilammine per formare arilammine sostituite, tra cui p-N-metilamminofenolo (solitamente commercializzato come sale solfato) e N,N’-difenil-p-fenilendiammina.
L’idrochinone può essere clorurato con cloro o cloruro di solforile per fornire derivati che vanno da mono- a tetraclorurati.
La carbossilazione di Kolbe-Schmitt dell’idrochinone con anidride carbonica porta all’acido 2,5-diidrossibenzoico (acido gentisico), mentre la chinizarina (1,4-diidrossiantrachinone) può essere preparata dalla condensazione dell’idrochinone con anidride ftalica.
L’idrogenazione catalitica dell’idrochinone dà 1,4-cicloesandiolo.
La solfonazione dell’idrochinone determina la formazione di acido mono- o disolfonico di idrochinone, in genere isolato come il corrispondente sale di potassio.
3. Utilizzi dell’idrochinone
L’idrochinone e i suoi derivati sono utilizzati in vari campi, tra cui fotografia, industria della gomma, coloranti e pigmenti, antiossidanti, prodotti chimici agricoli e altre applicazioni specializzate.
Tra questi, la maggiore richiesta di idrochinone deriva dal suo utilizzo come sviluppatore fotografico, principalmente in pellicole in bianco e nero, litografia, lavorazione fotochimica, microfilm e pellicole radiografiche.
Molti derivati dell’idrochinone, come il sale solfato di p-N-metilamminofenolo e il 2,5-diidrossibenzenesolfonato di potassio, sono impiegati anche in applicazioni fotografiche.
L’industria della gomma è il secondo maggiore consumatore di idrochinone per la produzione di antiossidanti e antiozonanti. In particolare, diversi derivati dell’idrochinone, come N,N’-diaril-p-fenilendiammine, idrochinoni dialchilati, N-alchil-p-amminofenoli, dialchil-p-fenilendiammine e aralchil-p-fenilendiammine, sono utilizzati a questo scopo.
L’idrochinone, l’idrochinone monometil etere e il p-benzochinone sono ampiamente utilizzati nell’industria dei monomeri vinilici per inibire la polimerizzazione dei radicali liberi durante la lavorazione e lo stoccaggio.
Analogamente, l’idrochinone e diversi altri derivati, come 2-terz-butilidrochinone, 2-metilidrochinone e 2,5-di-terz-butilidrochinone, fungono da stabilizzanti per resine poliestere insature.
Inoltre, alcuni derivati dell’idrochinone, tra cui idrochinone dimetil etere, chinizarina, Chloroneb ed etofumesato, sono utilizzati nella produzione di coloranti, pigmenti, fungicidi ed erbicidi.
Il fluazifop-butile è un esempio di una nuova famiglia di erbicidi che utilizzano l’idrochinone come materiale di partenza.
L’idrochinone bis(2-idrossietil) etere, formato dalla reazione dell’idrochinone con l’ossido di etilene, agisce come estensore di catena nei polimeri uretanici termoindurenti.
L’idrochinone e diversi derivati, come quelli dell’idrochinone C-alchilato o C-arilato, sono monomeri utili per la preparazione di una varietà di polimeri, tra cui plastiche ad alte prestazioni, compositi e fibre.
I materiali preparati utilizzando monomeri di idrochinone presentano elevate resistenze alla trazione e all’impatto, buona resistenza agli agenti atmosferici, resistenza ai solventi, ritardo di fiamma, trasparenza alle radiazioni a microonde e mantenimento della resistenza a temperature elevate.
L’idrochinone (grado U.S.P.) e diversi derivati sono usati come agenti sbiancanti e depigmentanti per la pelle in formulazioni topiche.
Le applicazioni emergenti dell’idrochinone includono le sue proprietà di rimozione dell’ossigeno che possono essere sfruttate per l’uso nel trattamento dell’acqua della caldaia.
Riferimento
- Hydroquinone; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a13_499
