Phloroglucinol: Production, Réactions et Utilisations
Phloroglucinol, 1,3,5-trihydroxybenzène
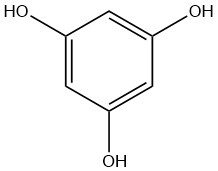
En 1855, HLASIWETZ a trouvé du phloroglucinol dans les produits d’hydrolyse de la phlorétine, qui a été obtenue à partir de l’écorce des arbres fruitiers.
Le nom phloroglucinol vient du grec et signifie « écorce douce ». Ses dérivés (par exemple, les flavones, les anthocyanures et les xanthines) sont largement distribués dans le règne végétal.
Table des matières
1. Production de phloroglucinol
Le phloroglucinol peut être préparé par divers procédés.
Le 2,4,6-trinitrotoluène est oxydé avec du dichromate de sodium pour donner de l’acide 2,4,6-trinitrobenzoïque, qui est ensuite décarboxylé. Les groupes nitro sont ensuite réduits avec du fer – acide chlorhydrique pour former du 1,3,5-triaminobenzène.
La substitution nucléophile ultérieure des groupes amino par des groupes hydroxyle produit du phloroglucinol. Cependant, l’élimination des filtrats acides qui contiennent du chrome et du fer pose un problème.

Dans les années 1980, un procédé a été développé pour produire du phloroglucinol à partir de 1,3,5-triisopropylbenzène via le trihydroperoxyde correspondant.
Le rendement est augmenté par addition de peroxyde d’hydrogène au mélange réactionnel dans l’étape d’acidolyse.

Une autre méthode de production de phloroglucinol est le réarrangement de Beckmann du trioxime de triacétylbenzène suivi d’une hydrolyse.
D’autres procédés comprennent le réarrangement d’Hofmann du triamide d’acide benzène-1,3,5-tricarboxylique; réaction du 1,3,5-tribromobenzène ou de l’hexachlorobenzène avec un alcoxyde suivie d’une acidolyse; et hydrolyse du 4-chlororésorcinol avec de l’hydroxyde de potassium.
2. Réactions chimiques du phloroglucinol
En raison de la tautomérie céto-énol, le phloroglucinol réagit pour former des dérivés de triphénol et des dérivés de tricétone.
Le phloroglucinol se comporte comme une tricétone, par exemple vis-à-vis de l’hydroxylamine pour former le trioxime, et ajoute du bisulfite de sodium pour donner les produits mono-, di- et tri-substitués correspondants.
Le comportement des triphénols est montré dans l’éthérification et l’estérification qui forment des phénols mono-, di- et trisubstitués. La réaction de Friedel-Crafts et la nitration ont également lieu.
Le phloroglucinol est également un agent réducteur. La solution aqueuse alcaline absorbe l’oxygène gazeux. L’absorption d’oxygène par le phloroglucinol est plus lente que par le pyrogallol.
Le phloroglucinol réduit la solution de Fehling et les ions de métaux précieux (par exemple, Au2þ, Agþ et Pt2þ).
La réaction avec l’iodure de méthyle provoque une méthylation du cycle dans des conditions basiques.
La réaction avec l’ammoniac aqueux produit du 5-aminorésorcinol ou du 3,5-diaminophénol.
Le phloroglucinol forme du phloroglucide lors du chauffage. L’hydrogénation donne le 1,3,5-trihydroxycyclohexane. Le couplage avec les sels de diazonium se fait facilement.
3. Utilisations du phloroglucinol
Le phloroglucinol est utilisé comme coupleur dans le diazotypage.
Le phloroglucinol et le composé diazoïque réagissent l’un avec l’autre pour former une grosse molécule de couleur noire.
Dans le processus de séchage, les composés diazo et hydroxy sont tous deux contenus dans le revêtement. Le phloroglucinol est également utilisé pour la photocopie.
En medecine, il est utilisé dans le traitement des spasmes douloureux d’origines digestive (colites spasmodiques), biliaire (coliques hépatiques), urologique (coliques néphrétiques) et gynécologique (règles douloureuses et contractions de l’utérus pendant la grossesse)
Références
- Phenol Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a19_313
- https://www.vidal.fr/medicaments/gammes/phloroglucinol-arrow-31619.html
