Floroglucinol: producción, reacciones y usos
Floroglucinol, 1,3,5-trihidroxibenceno
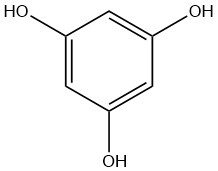
HLASIWETZ identificó por primera vez el floroglucinol en los productos de hidrólisis de la floretina, que se deriva de la corteza de los árboles frutales, en 1855.
El término floroglucinol se deriva del idioma griego y significa «corteza dulce». Sus derivados, como las flavonas, los antocianuros y las xantinas, se encuentran habitualmente en las plantas.
Tabla de contenido
1. Producción de floroglucinol
Existen varios métodos para la preparación de floroglucinol.
Un método implica la oxidación de 2,4,6-trinitrotolueno con dicromato de sodio para producir ácido 2,4,6-trinitrobenzoico que luego se descarboxila.
El producto resultante se reduce usando hierro y ácido clorhídrico para formar 1,3,5-triaminobenceno.
El floroglucinol se obtiene entonces mediante sustitución nucleófila posterior de los grupos amino por grupos hidroxilo. Sin embargo, la eliminación de los filtrados ácidos que contienen cromo y hierro es un desafío.

Durante la década de 1980, se desarrolló un nuevo método para la síntesis de floroglucinol a partir de 1,3,5-triisopropilbenceno mediante la formación del correspondiente trihidroperóxido intermedio.
Se encontró que la adición de peróxido de hidrógeno a la mezcla de reacción durante la etapa de acidólisis mejora el rendimiento de la reacción.

El floroglucinol se puede sintetizar mediante la transposición de Beckmann de la triacetilbencenotrioxima, seguida de hidrólisis.
En otro método, la triamida del ácido benceno-1,3,5-tricarboxílico se somete a un reordenamiento de Hofmann.
Además, el floroglucinol se puede obtener mediante la reacción de 1,3,5-tribromobenceno o hexaclorobenceno con un alcóxido, seguida de acidólisis. Otra alternativa implica la hidrólisis de 4-clororesorcinol con hidróxido de potasio.
2. Reacciones químicas del floroglucinol
Debido a su tautomerismo ceto-enol, el floroglucinol es capaz de reaccionar para formar derivados de trifenol y tricetona. La molécula muestra un comportamiento de tricetona en reacciones como con hidroxilamina para formar la trioxima correspondiente y con bisulfito de sodio para producir productos mono, di y trisustituidos.
Por el contrario, el comportamiento de los trifenoles se demuestra en reacciones como la eterificación y esterificación, que conducen a la formación de fenoles mono, di y trisustituidos.
El floroglucinol también puede sufrir reacciones de alquilación y acilación de Friedel-Crafts y nitración.
Además, se sabe que el floroglucinol actúa como agente reductor. Cuando está presente en una solución acuosa alcalina, puede absorber oxígeno gaseoso, aunque esto ocurre a un ritmo más lento que con el pirogalol.
El floroglucinol puede reducir la solución de Fehling, así como varios iones de metales preciosos, incluidos Au2+, Ag+ y Pt2+. Cuando se somete a condiciones básicas y se trata con yoduro de metilo, el floroglucinol sufre una metilación del anillo.
Otras reacciones del floroglucinol incluyen su reacción con amoníaco acuoso para formar 5-aminoresorcinol o 3,5-diaminofenol. Al calentarse, el floroglucinol forma floroglucida.
La hidrogenación del floroglucinol produce 1,3,5-trihidroxiciclohexano. El acoplamiento con sales de diazonio también es una reacción fácilmente realizable.
3. Usos del floroglucinol
El floroglucinol sirve como acoplador en el diazotipado, donde reacciona con un compuesto diazo para formar una molécula de alto peso molecular que tiene un color negro.
Tanto los compuestos diazo como los hidroxi están presentes en el recubrimiento durante el proceso de secado.
Además, el floroglucinol se utiliza en procesos de fotocopiado.
En medicina, se utiliza en el tratamiento de espasmos dolorosos de origen digestivo (colitis espástica), biliar (cólico hepático), urológico (cólico renal) y ginecológico (menstruaciones dolorosas y contracciones del útero durante el embarazo).
Referencia
- Phenol Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a19_313
- https://www.vidal.fr/medicaments/gammes/phloroglucinol-arrow-31619.html
