Condensation du benzaldéhyde
Points clés à retenir
- La condensation du benzaldéhyde est une réaction chimique polyvalente qui peut être utilisée pour synthétiser une large gamme de composés organiques.
- La réaction est généralement catalysée par une base forte, telle que l’hydroxyde de sodium ou l’hydroxyde de potassium.
- Le mécanisme de condensation du benzaldéhyde implique la formation d’un anion énolate, qui réagit ensuite avec un autre aldéhyde ou cétone pour former un aldéhyde ou une cétone α-ouβ-hydroxy.
- La condensation du benzaldéhyde peut être utilisée pour synthétiser une variété de composés importants, tels que le benjoin, l’acide cinnamique, le cinnamaldéhyde et des composés hétérocycliques.
- La réaction a un large éventail d’applications dans les industries pharmaceutique, alimentaire et chimique.
Table des matières
1. Qu’est-ce que la condensation du benzaldéhyde ?
La condensation du benzaldéhyde est une réaction chimique entre le benzaldéhyde et des molécules d’aldéhyde ou de cétone avec un α-hydrogène pour former un β-hydroxy aldéhyde ou cétone. La réaction est généralement catalysée par une base forte, telle que l’hydroxyde de sodium ou l’hydroxyde de potassium.
Il existe deux principaux types de condensation du benzaldéhyde :
- Condensation du benzoïne: Ce type de réaction de condensation se produit entre deux molécules d’aldéhyde en présence d’un catalyseur ionique cyanure. Le produit de la condensation du benjoin est une α-hydroxycétone.
- Condensation aldolique : Ce type de réaction de condensation se produit entre un aldéhyde et une cétone, ou entre deux aldéhydes, en présence d’un catalyseur basique. Le produit de la condensation aldolique est un β-hydroxy aldéhyde ou cétone.
L’équation générale de la condensation du benzaldéhyde est la suivante :

2. Histoire de la condensation du benzaldéhyde
La condensation du benzaldéhyde a été découverte pour la première fois en 1832 par Justus von Liebig et Friedrich Wöhler. Ils ont observé que la réaction du benzaldéhyde avec le cyanure de potassium produisait un nouveau composé, qu’ils appelèrent benzoine.
À la fin des années 1830, Nikolaï Zinine développa une version catalytique de la condensation du benjoin utilisant du cyanure de sodium. Cela a rendu la réaction plus pratique et accessible aux chimistes.
Depuis lors, la condensation du benzaldéhyde est devenue l’une des réactions de formation de liaisons carbone-carbone les plus importantes et les plus largement utilisées en chimie organique.
3. Mécanisme de condensation du benzaldéhyde
Le mécanisme de condensation du benzaldéhyde implique les étapes suivantes :
- Déprotonation : le catalyseur basique déprotonne le carbone α de la molécule d’aldéhyde, formant un anion énolate.
- Addition : L’anion énolate attaque le carbone carbonyle d’une autre molécule d’aldéhyde ou de cétone, formant un intermédiaire tétraédrique.
- Élimination : Un proton est transféré de l’intermédiaire tétraédrique au catalyseur basique, formant le produit α-ou β-hydroxy cétone.

4. Facteurs affectant le rendement de condensation du benzaldéhyde
Un certain nombre de facteurs peuvent affecter le rendement de condensation du benzaldéhyde, notamment :
- Nature de l’aldéhyde : Les aldéhydes aromatiques réagissent généralement plus facilement lors de la condensation du benzaldéhyde que les aldéhydes aliphatiques.
- Force du catalyseur basique : Les bases fortes, telles que l’alcoolate, l’hydroxyde de sodium et l’hydroxyde de potassium, sont des catalyseurs plus efficaces pour la condensation du benzaldéhyde que les bases faibles.
- Température de réaction : La vitesse de réaction de condensation du benzaldéhyde augmente avec la température. Cependant, les températures élevées peuvent également entraîner des réactions secondaires et une dégradation du produit.
- Temps de réaction : La condensation du benzaldéhyde nécessite généralement plusieurs heures. Cependant, le temps de réaction peut être réduit en utilisant un catalyseur basique plus concentré ou en augmentant la température de réaction.
5. Exemples de réactions de condensation du benzaldéhyde
La condensation du benzaldéhyde peut être utilisée pour synthétiser une large gamme de composés organiques, notamment : le benzoine, l’acide cinnamique, le cinnamaldéhyde et la benzalacétone,
5.1. Condensation de Benzoine

Le benzoine est une α-hydroxycétone symétrique produite par la condensation de benzoine de deux molécules de benzaldéhyde. Le benzoine est utilisé comme intermédiaire dans la synthèse d’un certain nombre d’autres composés, tels que l’hydrobenzoïne, l’isoxazole de benzoine et l’éther éthylique de benzoine.
La condensation du benzoine a été signalée pour la première fois par Justus von Liebig et Friedrich Wöhler en 1832. Ils ont découvert que lorsque le benzaldéhyde était traité avec du cyanure de potassium, un nouveau composé se formait, qu’ils appelèrent « benzoinen ».
Plus tard, Nikolaï Zinine a développé une version catalytique de cette réaction. Il a découvert qu’en utilisant une petite quantité de cyanure, la réaction pouvait être réalisée plus efficacement. Cela a marqué une avancée significative dans le domaine de la chimie organique.
5.1.1. Mécanisme de réaction
Le mécanisme de condensation du benzaldéhyde comporte plusieurs étapes. Premièrement, un nucléophile, tel que le cyanure ou le carbène N-hétérocyclique, attaque le carbone carbonyle du benzaldéhyde. Cela forme un complexe intermédiaire, qui subit ensuite un transfert de protons pour former le benzoine.
Dans la condensation du benzaldéhyde, les nucléophiles jouent un rôle important. Ils attaquent le carbone carbonyle du benzaldéhyde, déclenchant la réaction. Les nucléophiles courants utilisés dans cette réaction comprennent le cyanure et le carbène N-hétérocyclique.
5.2. Condensation du benzaldéhyde avec l’acétaldéhyde

La condensation du benzaldéhyde avec l’acétaldéhyde est une réaction chimique qui produit du cinnamaldéhyde, un composé parfumé utilisé dans les parfums et les arômes alimentaires. La réaction est également utilisée pour synthétiser d’autres produits chimiques importants, tels que l’acide cinnamique et les dérivés du cinnamaldéhyde.
5.2.1. Mécanisme de la réaction
Cette réaction est un exemple classique de condensation aldolique croisée, dans laquelle deux aldéhydes différents réagissent pour former une nouvelle liaison carbone-carbone. La réaction se déroule selon les étapes suivantes :
- Déprotonation de l’acétaldéhyde : une base forte, telle que l’hydroxyde de sodium, déprotonne l’acétaldéhyde pour former l’ion énolate.
- Attaque du carbone carbonyle du benzaldéhyde : l’ion énolate attaque le carbone carbonyle du benzaldéhyde, formant une nouvelle liaison carbone-carbone.
- Déshydratation : l’ion alcoxyde résultant est protoné puis se déshydrate pour former du cinnamaldéhyde.
5.2.2. Conditions de la réaction
La réaction est généralement réalisée dans un solvant tel que l’éthanol ou l’eau, en présence d’une base forte telle que l’hydroxyde de sodium. La température de réaction peut aller de la température ambiante au reflux, en fonction du rendement souhaité et de la pureté du produit.
Une réaction secondaire potentielle de la réaction est l’auto-condensation de l’acétaldéhyde pour former de l’aldol. Pour minimiser cette réaction secondaire, il est important d’ajouter lentement l’acétaldéhyde au mélange réactionnel et de maintenir la température de réaction basse.
5.3. Condensation du benzaldéhyde avec l’anhydride acétique (condensation de Perkin)

La condensation du benzaldéhyde avec l’anhydride acétique pour former de l’acide cinnamique est une réaction de synthèse organique classique connue sous le nom de condensation de Perkin. Il s’agit d’une méthode polyvalente et efficace pour préparer des acides carboxyliques α,β-insaturés, qui sont des intermédiaires importants dans la synthèse de nombreux produits naturels et synthétiques.
5.3.1. Mécanisme de réaction
La condensation de Perkin est une réaction catalysée par une base. Le catalyseur à l’acétate de sodium déprotonne le carbone α de la molécule d’anhydride acétique, formant un carbanion. Ce carbanion attaque ensuite le carbone carbonyle de la molécule de benzaldéhyde, formant un intermédiaire tétraédrique. L’intermédiaire s’effondre alors, éliminant l’acide acétique et formant de l’acide cinnamique.
La condensation Perkin est généralement réalisée à des températures de 160 à 180°C. La réaction peut être catalysée par diverses bases, notamment l’acétate de sodium, l’hydroxyde de sodium et la pyridine.
5.4. Condensation du benzaldéhyde avec de l’acétone
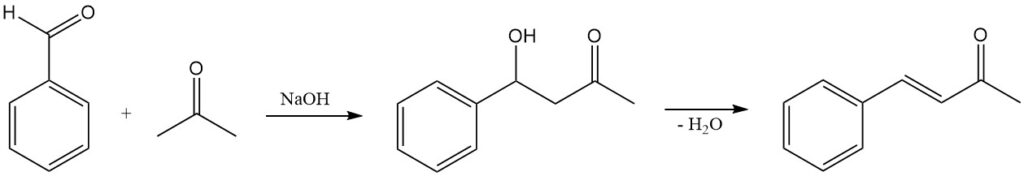
La condensation du benzaldéhyde avec l’acétone est une réaction organique courante utilisée pour synthétiser la benzalacétone, un intermédiaire précieux dans la production de produits pharmaceutiques, de colorants et d’autres produits chimiques.
La réaction est généralement catalysée par une base, telle que l’hydroxyde de sodium ou l’hydroxyde de potassium, et se déroule selon un mécanisme classique de condensation aldolique.
5.4.1. Mécanisme
La première étape de la réaction est la déprotonation de l’acétone par la base pour former l’ion énolate. L’ion énolate est un nucléophile puissant et attaque le carbone carbonyle électrophile du benzaldéhyde. L’intermédiaire tétraédrique résultant s’effondre, expulsant l’ion hydroxyde et formant une nouvelle liaison carbone-carbone.
La deuxième étape de la réaction est la déshydratation du produit aldol pour former la cétone α,β-insaturée benzalacétone. L’étape de déshydratation peut être favorisée en chauffant le mélange réactionnel ou en ajoutant un catalyseur acide.
5.4.2. Processus de production
La condensation aldolique du benzaldéhyde et de l’acétone peut être réalisée dans divers solvants, mais l’eau est le plus courant. La réaction est généralement chauffée au reflux (environ 100 °C) pour favoriser l’étape de déshydratation.
La quantité de base utilisée dépend du rendement souhaité et de la pureté du produit. Pour un rendement élevé en benzalacétone pure, il est important d’utiliser un léger excès de base.
Une fois la réaction terminée, le produit peut être isolé en refroidissant le mélange réactionnel et en l’extrayant avec un solvant organique, tel que le dichlorométhane ou l’éther diéthylique. L’extrait organique peut ensuite être lavé à l’eau et séché sur sulfate de sodium ou sulfate de magnésium.
Le produit brut peut être purifié par recristallisation dans l’éthanol ou les hexanes.
6. Applications de la condensation du benzaldéhyde
La condensation du benzaldéhyde a un large éventail d’applications dans les industries pharmaceutique, alimentaire et des matériaux. Voici quelques exemples spécifiques :
- Produits pharmaceutiques : la condensation du benzaldéhyde est utilisée pour synthétiser une variété de produits pharmaceutiques importants, tels que la phénytoïne (médicament anti-épileptique).
- Alimentation : la condensation du benzaldéhyde est utilisée pour synthétiser un certain nombre d’additifs alimentaires, tels que le cinnamaldéhyde et la coumarine (agents aromatisants et parfumants), l’acide cinnamique (conservateur alimentaire)
- Intermédiaires organiques : la condensation du benzaldéhyde est utilisée pour synthétiser une variété de matières premières pour la synthèse organique comme la benzalacétone, le benzil.
Références
- Benzoin Condensation: Definition, Mechanism and Applications – https://testbook.com/chemistry/benzoin-condensation
- Carbonyl Condensation Reactions (Summary) – https://www.organicchemistrytutor.com/topic/benzoin-condensation/
- Benzoin Condensation – an overview. – https://www.sciencedirect.com/topics/chemistry/benzaldehyde
- https://ntp.niehs.nih.gov/sites/default/files/ntp/htdocs/chem_background/exsumpdf/cinnamaldehyde_508.pdf
- SYNTHESIS OF CINNAMIC ACID BASED ON PERKIN REACTION USING SONOCHEMICAL METHOD AND ITS POTENTIAL AS PHOTOPROTECTIVE AGENT
- https://www.researchgate.net/publication/43656185_Synthesis_of_Hydroxyl_Radical_Scavengers_from_Benzalacetone_and_its_Derivatives
FAQ
Les deux principaux types de condensation du benzaldéhyde sont la condensation du benzoine et la condensation de l’aldol.
Le mécanisme de condensation du benzaldéhyde implique la déprotonation du carbone α de la molécule d’aldéhyde, suivie d’une réaction d’addition avec une autre molécule d’aldéhyde et d’une réaction d’élimination finale pour former le produit cétone α,β-insaturé.
Lorsque le benzaldéhyde est condensé avec de l’acétone, une formation de liaison (-C=C-) se produit. Cette réaction est un exemple de réaction de condensation aldolique mixte, qui aboutit à la formation de benzalacétone.
