Peróxido de metiletilcetona: producción y usos
Peróxido de metiletilcetona
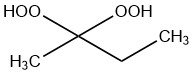
El peróxido de metiletilcetona es un compuesto químico líquido de la familia de los peróxidos de cetona que se utiliza para iniciar la polimerización de resinas de poliéster y éster vinílico insaturado a diferentes temperaturas de curado.
Es el producto de condensación de la reacción del peróxido de hidrógeno y 2-butanona y está disponible como estructura cíclica y de cadena abierta.
Tabla de contenido
1. Propiedades físicas Peróxido de metiletilcetona
El peróxido de metiletilcetona puro es un producto líquido con una energía de disociación de ca. 100 kJ/mol. Es un peróxido soluble en agua.
- La formulación comercial es una solución de ≈ 30 % en diisobutirato de 1-isopropil-2,2-dimetiltrimetileno.
- Densidad = 1,01
- Índice de refracción (20 °C) = 1,437
- Contenido de oxígeno activo = 9,3%
2. Reacciones químicas del peróxido de metiletilcetona
La termólisis del peróxido de metiletilcetona da una mezcla compleja de productos, entre ellos cetona, agua, dióxido de carbono, ácidos, alcohol y alcano.
La descomposición del peróxido de metiletilcetona en ácido carboxílico se acelera mediante catálisis ácida. Además, estos peróxidos son sensibles a los metales. La descomposición es inducida por promotores de metales de transición, como los iones de cobalto.
En presencia de sales de hierro o cobre, el peróxido de metiletilcetona cíclica sufre una reacción de apertura de anillo con ácidos carboxílicos.
La reacción del peróxido de hidrógeno con metiletilcetona da como resultado la formación de hidroperóxidos de α-hidroxialquilo, que reaccionan fácilmente con otros productos de condensación. Así, los peróxidos de cetonas siempre se obtienen como una mezcla de diferentes especies peroxídicas.
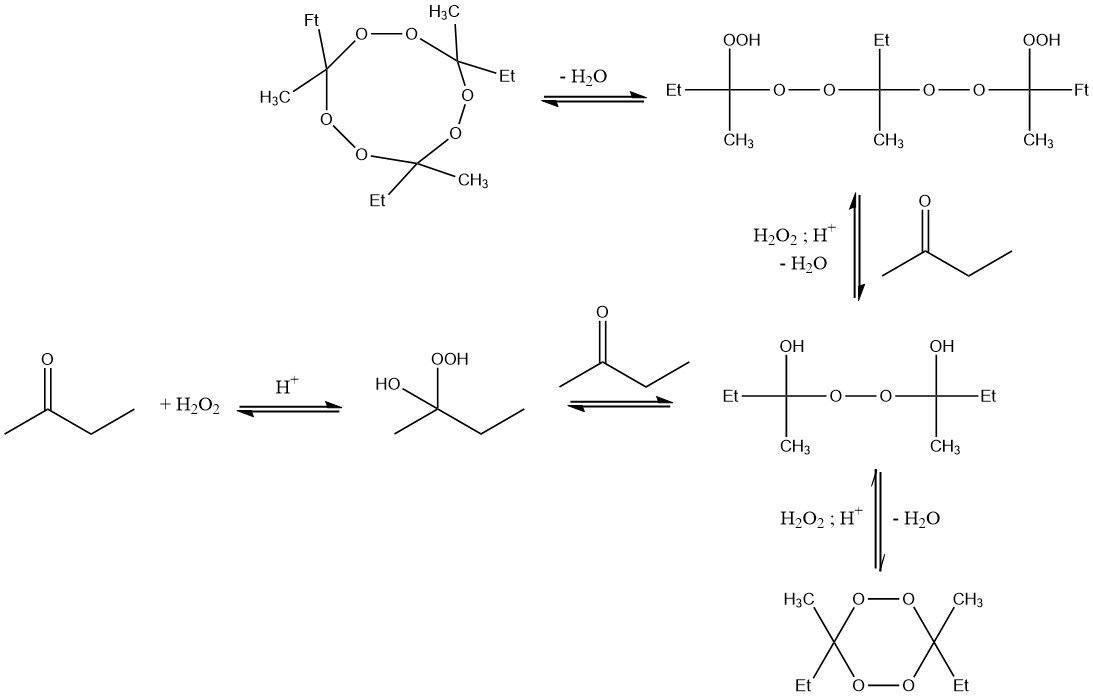
El grado de condensación depende de las condiciones de reacción, en particular de la concentración de peróxido de hidrógeno y 2-butanona, la temperatura de reacción, el tiempo y la cantidad de ácido.
Los compuestos más estables y frecuentes son las especies monoméricas y diméricas. Los derivados altamente condensados suelen constituir una pequeña fracción.
Además, durante la reacción se pueden formar productos de condensación cíclicos triméricos. Estos compuestos son sensibles a la temperatura y potencialmente explosivos cuando están en estado sólido.
Para garantizar la estabilidad, las formulaciones comerciales de peróxido de metiletilcetona pueden incluir bases de amina para ajustar el pH, evitando eficazmente la condensación en sustancias potencialmente peligrosas.
3. Producción de peróxido de metiletilcetona
El peróxido de metiletilcetona se puede preparar mediante reacción de peróxido de hidrógeno con metiletilcetona o mediante autooxidación.
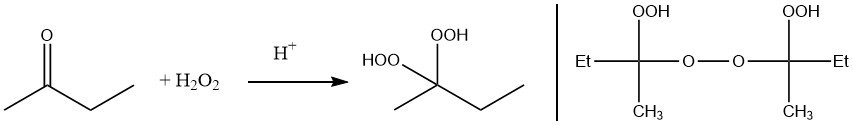
Según datos de 2016, la utilización de peróxidos de cetonas en el sector del plástico alcanzó aproximadamente 60.000 toneladas en todo el mundo. Esto implica que los peróxidos de cetonas representaron el 25% del consumo total de peróxidos dentro de la industria del plástico a escala global.
Es de destacar que estos peróxidos particulares encuentran una aplicación casi exclusiva en el proceso de curado de materiales de poliéster insaturado (UP).
Debido a sus características potencialmente detonables, el peróxido de metiletilcetona sólo está disponible como soluciones altamente flegmatizadas con aproximadamente un 30% de contenido de peróxido.
El proceso industrial consiste en la adición de peróxido de hidrógeno al 70% a una solución que contiene ftalato de dibutilo, metiletilcetona y 65% de HNO3 a una temperatura de 30°C durante 1 hora. La solución de reacción se agita adicionalmente durante 30 minutos más a la misma temperatura.
Después del paso de separación de fases, la materia prima resultante se combina con diacetona alcohol, colidina y peróxido de hidrógeno al 70%.
El proceso sintético tradicional para producir peróxido de cetona cíclica trimérica de butanona implica la pirólisis de peróxidos de tricicloalquilideno. En este método, la 2-butanona, el peróxido de hidrógeno y el ácido reaccionan para formar peróxido de 1-hidroxiperoxi-1´-hidroxi-dicicloalquilideno, que luego se condensa en presencia de un ácido fuerte, produciendo un compuesto cíclico con un rendimiento aproximado de 60 %.
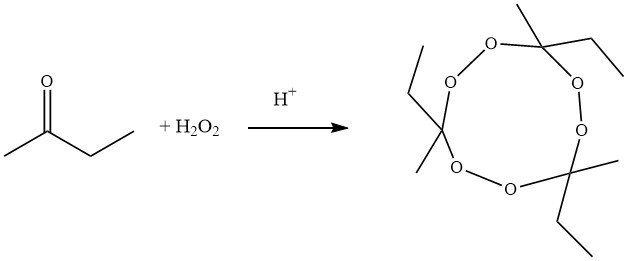
Los métodos modernos, por otra parte, emplean la conversión de 2-butanona con peróxido de hidrógeno en presencia de ácido nítrico, isoalcanos y ácido acético como agente solubilizante.
Después de la síntesis, el peróxido de hidrógeno y los hidroperóxidos restantes se reducen utilizando sulfito de sodio. El peróxido de cetona trimérico se obtiene con un rendimiento del 90% y la proporción de trímero a dímero es de aproximadamente 94:6.
4. Usos del peróxido de metiletilcetona
En el año 2016, se produjo una cantidad estimada de aproximadamente 250-260 millones de toneladas métricas de plástico, de las cuales alrededor del 75% del volumen entró en contacto con peróxidos orgánicos durante el proceso de fabricación. Las aplicaciones del peróxido de metiletilcetona se pueden clasificar en tres segmentos: fabricación de polímeros, modificación de polímeros y aplicaciones no poliméricas.
La fabricación de polímeros implica la utilización de peróxidos orgánicos en diversos procesos de polimerización industrial, como en masa, suspensión y solución. Los polímeros clave en esta categoría incluyen PVC, LDPE, PS, PP y PMMA. El consumo total de peróxidos para la fabricación de polímeros se estimó en unas 100.000 toneladas métricas.
4.1. Fabricación de polímeros
El PVC, que se utiliza ampliamente en la construcción, es un polímero termoplástico importante. Se emplean diferentes técnicas de polimerización para la producción de PVC, incluyendo suspensión (S-PVC), microsuspensión (MS-PVC), masa (M-PVC) y emulsión (E-PVC). El peróxido de metiletilcetona sirve como iniciador en todos estos procesos excepto en el E-PVC, con un factor de entrada que oscila aproximadamente entre el 0,05% y el 0,1%.
El LDPE, otro termoplástico importante, requiere peróxido orgánico para la polimerización radicalaria del gas etileno. El proceso se produce de forma continua a presiones de hasta 3000 bar, lo que da como resultado tasas de conversión entre el 10% y el 30%.
El polipropileno, el segundo termoplástico más grande a nivel mundial, sufre una degradación de la cadena polimérica durante el proceso final de extrusión/granulación cuando se agrega MEKP. Este proceso, conocido como PP de reología controlada (cr-PP), conduce a índices de flujo de fusión (MFI) más altos debido a una reducción en la masa molecular.
El poliestireno (PS) presenta versatilidad y puede copolimerizarse fácilmente con otros monómeros. Los peróxidos orgánicos se utilizan comúnmente como iniciadores en la mayoría de los grados de PS, mientras que los procesos iniciados térmicamente o con oxígeno son menos frecuentes.
Los poli(met)acrilatos (PMMA) y otros ésteres de ácido (met)acrílico encuentran aplicaciones en industrias como la optoelectrónica, la automoción y la construcción. Los peróxidos de cetona se utilizan en procesos de polimerización en masa y en solución, y normalmente oscilan entre el 0,03% y el 0,3% de la composición total.
4.2. Procesamiento de polímeros
El procesamiento de polímeros representa más del 50% del consumo mundial de peróxido orgánico e implica actividades como el curado de resinas de poliéster insaturado (UP) y polímeros reticulantes (XL).
4.2.1. ARRIBA Curado
Los poliésteres insaturados utilizan ácidos dicarboxílicos insaturados, como el ácido fumárico y maleico, durante la etapa de policondensación. El peróxido de metiletilcetona genera radicales que copolimerizan estos poliésteres insaturados con monómeros reactivos como el estireno o el metacrilato de metilo.
El curado en frío, donde se añaden aceleradores (sistemas redox) a la resina, permite la descomposición del peróxido a temperatura ambiente. Dos combinaciones comunes de peróxido orgánico/acelerador son sales de MEKP/Co2+ y peróxido de dibenzoilo/aminas aromáticas (dimetilanilina), con factores de entrada que oscilan entre el 2% y el 4%.
4.2.2. Reticulación de Polímeros (XL)
La reticulación de polímeros es la segunda aplicación más importante después del curado UP y representa aproximadamente el 40% de los peróxidos orgánicos utilizados en el procesamiento de polímeros. Este proceso encuentra aplicaciones en la fabricación de elastómeros (cauchos) y reticulación de polietileno (PE).
Los peróxidos orgánicos, con sus radicales altamente energéticos, son adecuados tanto para polímeros saturados como para elastómeros insaturados.
4.3. Aplicaciones sin polímeros
Además de los usos relacionados con polímeros, aproximadamente entre el 5% y el 6% del peróxido de metiletilcetona se emplea en diversas aplicaciones no poliméricas, incluidos cosméticos, síntesis química (producción de catecol), reacciones de epoxidación, saborizantes y fragancias.
5. Peligros para la seguridad del peróxido de metiletilcetona
El peróxido de metiletilcetona posee el potencial de descomposición espontánea y explosiva cuando se expone a estrés térmico o mecánico. Factores como golpes, impactos, fricción y la presencia de impurezas como metales pesados o aceleradores pueden catalizar este proceso de descomposición. En consecuencia, peróxido de metiletilcetona entra dentro del marco regulatorio para sustancias explosivas.
Es importante tener en cuenta que peróxido de metiletilcetona es sensible a la temperatura y puede sufrir una descomposición exotérmica. En ausencia de mecanismos de enfriamiento eficaces, la temperatura puede aumentar, acelerando así la reacción de descomposición.
A temperaturas elevadas, la descomposición del peróxido de metiletilcetona puede ocurrir espontáneamente y generar peligro de incendio. Además, si el proceso de descomposición tiene lugar dentro de un espacio confinado, el gas resultante puede provocar un aumento de presión, lo que podría provocar explosiones dentro de reactores, recipientes u otros contenedores.
Además, los productos volátiles de la descomposición del peróxido de metiletilcetona pueden contribuir a la formación de explosiones en fase de vapor. Para garantizar un almacenamiento seguro, es fundamental limitar la temperatura máxima de almacenamiento a menos de 30 °C.
Referencias
- Peroxy Compounds, Organic, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a19_199.pub2
- Production of salt-free and low-water-content methyl ethyl ketone peroxide. – https://patents.google.com/patent/EP0788477B1/en
