Methylethylketonperoxid (MEKP): Herstellung und Verwendung
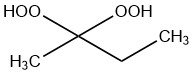
Methylethylketonperoxid (MEKP) ist eine flüssige chemische Verbindung aus der Familie der Ketonperoxide, die zur Initiierung der Polymerisation ungesättigter Polyester- und Vinylesterharze bei unterschiedlichen Härtungstemperaturen eingesetzt wird.
Es ist das Kondensationsprodukt aus der Reaktion von Wasserstoffperoxid und 2-Butanon und liegt als offenkettige und zyklische Struktur vor.
Inhaltsverzeichnis
1. Physikalische Eigenschaften Methylethylketonperoxid (MEKP)
Reines Methylethylketonperoxid ist ein flüssiges Produkt mit einer Dissoziationsenergie von ca. 100 kJ/mol. Es ist ein wasserlösliches Peroxid.
Handelsübliche Formulierung ist eine ≈ 30 %ige Lösung in 1-Isopropyl-2,2-Dimethyltrimethylendiisobutyrat.
- Dichte = 1,01
- Brechungsindex (20 °C) = 1,437
- Aktivsauerstoffgehalt = 9,3 %
2. Chemische Reaktionen von Methylethylketonperoxid (MEKP)
Bei der Thermolyse von Methylethylketonperoxid entsteht ein komplexes Produktgemisch, darunter Keton, Wasser, Kohlendioxid, Säuren, Alkohol und Alkan.
Die Zersetzung von Methylethylketonperoxid zu Carbonsäure wird durch Säurekatalyse beschleunigt. Darüber hinaus sind diese Peroxide empfindlich gegenüber Metallen. Die Zersetzung wird durch Übergangsmetallpromotoren wie Kobaltionen induziert.
In Gegenwart von Eisen- oder Kupfersalzen reagiert zyklisches Methylethylketonperoxid unter Ringöffnung zu Carbonsäuren.
Die Reaktion von Wasserstoffperoxid mit Methylethylketon führt zur Bildung von α-Hydroxyalkylhydroperoxiden, die leicht zu weiteren Kondensationsprodukten reagieren. Somit fallen Ketonperoxide immer als Gemisch verschiedener peroxidischer Spezies an.
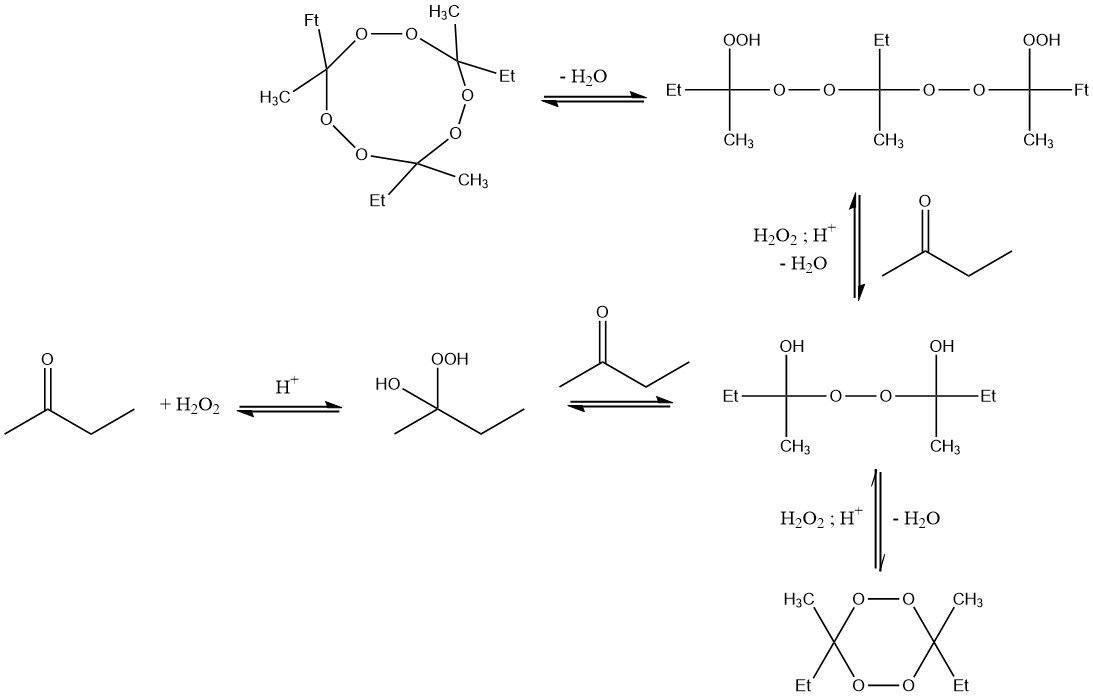
Der Grad der Kondensation hängt von den Reaktionsbedingungen ab, insbesondere von der Konzentration von Wasserstoffperoxid und 2-Butanon, der Reaktionstemperatur, der Reaktionszeit und der Säuremenge.
Die stabilsten und am weitesten verbreiteten Verbindungen sind Monomere und Dimere. Hochkondensierte Derivate machen typischerweise einen kleinen Anteil aus.
Darüber hinaus können während der Reaktion trimere cyclische Kondensationsprodukte entstehen. Diese Verbindungen sind temperaturempfindlich und im festen Zustand potenziell explosiv.
Um die Stabilität zu gewährleisten, können kommerzielle Formulierungen von Methylethylketonperoxid Aminbasen zur pH-Einstellung enthalten, wodurch die Kondensation potenziell gefährlicher Substanzen wirksam verhindert wird.
3. Herstellung von Methylethylketonperoxid (MEKP)
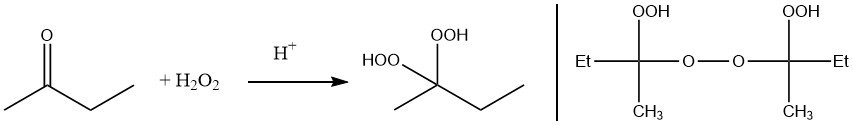
Methylethylketonperoxid kann entweder durch Reaktion von Wasserstoffperoxid mit Methylethylketon oder durch Autoxidation hergestellt werden.
Laut Daten aus dem Jahr 2016 belief sich der Einsatz von Ketonperoxiden im Kunststoffbereich weltweit auf etwa 60.000 Tonnen. Dies bedeutet, dass Ketonperoxide weltweit 25 % des gesamten Peroxidverbrauchs in der Kunststoffindustrie ausmachen.
Bemerkenswert ist, dass diese speziellen Peroxide fast ausschließlich im Härtungsprozess von Materialien aus ungesättigtem Polyester (UP) Anwendung finden.
Aufgrund seiner potenziell detonierbaren Eigenschaften ist MEKP nur als stark phlegmatisierte Lösungen mit etwa 30 % Peroxidgehalt erhältlich.
Der industrielle Prozess beinhaltet die Zugabe von 70 % Wasserstoffperoxid zu einer Lösung, die Dibutylphthalat, Methylethylketon und 65 % HNO3 enthält, bei einer Temperatur von 30 °C für eine Dauer von 1 Stunde. Die Reaktionslösung wird weitere 30 Minuten bei der gleichen Temperatur weitergerührt.
Nach dem Phasentrennungsschritt wird das resultierende Rohmaterial mit Diacetonalkohol, Collidin und 70 % Wasserstoffperoxid kombiniert.
Traditionelle Syntheseverfahren zur Herstellung des trimeren zyklischen Ketonperoxids von Butanon umfassen die Pyrolyse von Tricycloalkylidenperoxiden. Bei dieser Methode reagieren 2-Butanon, Wasserstoffperoxid und Säure unter Bildung von 1-Hydroxyperoxy-1´-hydroxy-dicycloalkylidenperoxid, das dann in Gegenwart einer starken Säure kondensiert und eine zyklische Verbindung mit einer Ausbeute von etwa 60 ergibt %.
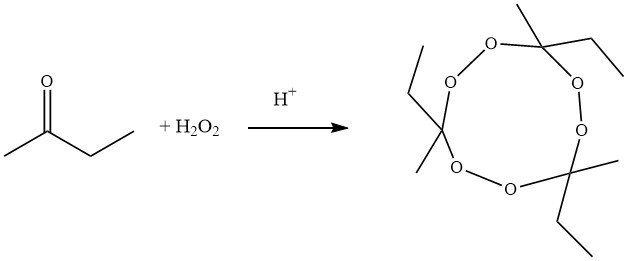
Moderne Methoden hingegen nutzen die Umwandlung von 2-Butanon mit Wasserstoffperoxid in Gegenwart von Salpetersäure, Isoalkanen und Essigsäure als Lösungsvermittler. Nach der Synthese werden verbleibendes Wasserstoffperoxid und Hydroperoxide mit Natriumsulfit reduziert. Das trimere Ketonperoxid wird mit einer Ausbeute von 90 % erhalten, das Verhältnis von Trimer zu Dimer beträgt etwa 94:6.
4. Verwendung von Methylethylketonperoxid (MEKP)
Im Jahr 2016 wurde eine geschätzte Menge von etwa 250–260 Millionen Tonnen Kunststoffen produziert, von denen etwa 75 % der Menge während des Herstellungsprozesses mit organischen Peroxiden in Kontakt kamen. Die Anwendungen von Methylethylketonperoxid können in drei Segmente eingeteilt werden: Polymerherstellung, Polymermodifikation und Nichtpolymeranwendungen.
Bei der Polymerherstellung werden organische Peroxide in verschiedenen industriellen Polymerisationsprozessen wie Masse-, Suspensions- und Lösungspolymerisation eingesetzt. Zu den wichtigsten Polymeren in dieser Kategorie gehören PVC, LDPE, PS, PP und PMMA. Der Gesamtverbrauch an Peroxiden für die Polymerherstellung wurde auf rund 100.000 Tonnen geschätzt.
4.1. Polymerherstellung
PVC, das im Bauwesen häufig verwendet wird, ist ein bedeutendes thermoplastisches Polymer. Für die PVC-Herstellung werden verschiedene Polymerisationstechniken eingesetzt, darunter Suspension (S-PVC), Mikrosuspension (MS-PVC), Masse (M-PVC) und Emulsion (E-PVC). Methylethylketonperoxid dient in allen diesen Prozessen mit Ausnahme von E-PVC als Initiator, wobei der Einsatzfaktor zwischen etwa 0,05 % und 0,1 % liegt.
LDPE, ein weiterer wichtiger Thermoplast, benötigt organisches Peroxid für die radikalische Polymerisation von Ethylengas. Der Prozess erfolgt kontinuierlich bei Drücken bis zu 3000 bar, was zu Umwandlungsraten zwischen 10 % und 30 % führt.
Bei Polypropylen, dem zweitgrößten Thermoplasten weltweit, kommt es beim abschließenden Extrusions-/Granulierungsprozess durch die Zugabe von MEKP zu einem Abbau der Polymerkette. Dieser als Controlled-Rheology-PP (cr-PP) bezeichnete Prozess führt aufgrund einer Verringerung der Molekularmasse zu höheren Schmelzflussindizes (MFI).
Polystyrol (PS) ist vielseitig einsetzbar und kann problemlos mit anderen Monomeren copolymerisiert werden. Organische Peroxide werden in den meisten PS-Qualitäten üblicherweise als Initiatoren verwendet, während thermische oder sauerstoffinitiierte Prozesse seltener sind.
Poly(meth)acrylate (PMMA) und andere (Meth)acrylsäureester finden Anwendung in Branchen wie der Optoelektronik, der Automobilindustrie und dem Bauwesen. Ketonperoxide werden in Massen- und Lösungspolymerisationsprozessen verwendet und liegen typischerweise im Bereich von 0,03 % bis 0,3 % der Gesamtzusammensetzung.
4.2. Polymerverarbeitung
Die Polymerverarbeitung macht über 50 % des weltweiten Verbrauchs organischer Peroxide aus und umfasst Aktivitäten wie das Aushärten ungesättigter Polyesterharze (UP) und vernetzender Polymere (XL).
4.2.1. UP-Härtung
Ungesättigte Polyester nutzen während des Polykondensationsschritts ungesättigte Dicarbonsäuren wie Fumarsäure und Maleinsäure. Methylethylketonperoxid erzeugt Radikale, die diese ungesättigten Polyester mit reaktiven Monomeren wie Styrol oder Methylmethacrylat copolymerisieren.
Die Kalthärtung, bei der dem Harz Beschleuniger (Redoxsysteme) zugesetzt werden, ermöglicht die Peroxidzersetzung bei Umgebungstemperaturen. Zwei gängige Kombinationen aus organischem Peroxid/Beschleuniger sind MEKP/Co2+-Salze und Dibenzoylperoxid/aromatische Amine (Dimethylanilin), wobei die Einsatzfaktoren zwischen 2 % und 4 % liegen.
4.2.2. Vernetzung von Polymeren (XL)
Die Vernetzung von Polymeren ist nach der UP-Härtung die zweitwichtigste Anwendung und macht etwa 40 % der bei der Polymerverarbeitung verwendeten organischen Peroxide aus. Dieses Verfahren findet Anwendung bei der Herstellung von Elastomeren (Kautschuken) und der Vernetzung von Polyethylen (PE). Organische Peroxide eignen sich mit ihren hochenergetischen Radikalen sowohl für gesättigte Polymere als auch für ungesättigte Elastomere.
4.3. Nichtpolymere Anwendungen
Zusätzlich zu polymerbezogenen Anwendungen werden etwa 5–6 % Methylethylketonperoxid in verschiedenen nichtpolymeren Anwendungen eingesetzt, darunter Kosmetika, chemische Synthese (Herstellung von Brenzkatechin), Epoxidierungsreaktionen, Aromen und Duftstoffe.
5. Sicherheitsrisiken für Methylethylketonperoxid
Methylethylketonperoxid (MEKP) kann bei thermischer oder mechanischer Belastung spontan und explosionsartig zerfallen. Faktoren wie Stöße, Stöße, Reibung und das Vorhandensein von Verunreinigungen wie Schwermetallen oder Beschleunigern können diesen Zersetzungsprozess katalysieren. Folglich fällt MEKP unter den Regulierungsrahmen für explosive Stoffe.
Es ist wichtig zu beachten, dass MEKP temperaturempfindlich ist und einer exothermen Zersetzung unterliegen kann. Ohne wirksame Kühlmechanismen kann die Temperatur ansteigen und dadurch die Zersetzungsreaktion beschleunigen.
Bei erhöhten Temperaturen kann die Zersetzung von MEKP spontan erfolgen und zu Brandgefahr führen. Wenn der Zersetzungsprozess außerdem in einem geschlossenen Raum stattfindet, kann das entstehende Gas zu einem Druckanstieg führen, der möglicherweise zu Explosionen in Reaktoren, Behältern oder anderen Behältern führt.
Darüber hinaus können die flüchtigen Zersetzungsprodukte von MEKP zur Entstehung von Dampfphasenexplosionen beitragen. Um eine sichere Lagerung zu gewährleisten, ist es unbedingt erforderlich, die maximale Lagertemperatur auf unter 30 °C zu begrenzen.
Verweise
- Peroxy Compounds, Organic, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a19_199.pub2
- Production of salt-free and low-water-content methyl ethyl ketone peroxide. – https://patents.google.com/patent/EP0788477B1/en
