4-Nitrofenol: Producción, Reacciones y Usos
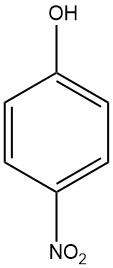
El 4-nitrofenol (también conocido como p-nitrofenol o 4-hidroxinitrobenceno) es un compuesto aromático con la fórmula química C6H5NO3. Es un nitrofenol, lo que significa que contiene un grupo nitro (-NO2) y un grupo hidroxilo (-OH) unidos a un anillo de benceno.
El 4-nitrofenol es un sólido cristalino de color amarillo a incoloro con un olor fenólico dulce. Es soluble en agua, etanol y otros disolventes orgánicos.
Tabla de contenido
1. Propiedades físicas del 4-nitrofenol
El p-nitrofenol tiene una forma α metaestable que se puede observar en forma cristalina cuando el tolueno se calienta por encima de 63 °C. La forma β más estable se obtiene cuando el tolueno se enfría por debajo de 63°C. El p-nitrofenol no es fácilmente volátil con el vapor, pero es más soluble en agua que su ortoisómero.
Algunas de las propiedades físicas del 4-nitrofenol se presentan en la siguiente tabla:
| Propiedad | Valor |
|---|---|
| Fórmula química | C6H5NO3 |
| Masa molar | 139,11 g/mol |
| Apariencia | Sólido cristalino amarillo, parecido a una aguja |
| Punto de fusión | 114 °C |
| Punto de ebullición | 216 °C |
| Solubilidad en agua (100°C) | 30% |
| Solubilidad en agua (25°C) | 16 g/L |
| Densidad | 1,48 g/cm³ |
| pKa | 7.15 |
| Punto de inflamación | 105°C |
| Temperatura de descomposición de la sal de sodio | 156°C |
2. Reacciones químicas del 4-nitrofenol
El 4-nitrofenol es un compuesto relativamente estable. A su reactividad contribuye la presencia de grupos nitro e hidroxilo en el anillo aromático, por lo que puede sufrir una variedad de reacciones químicas, como las siguientes:
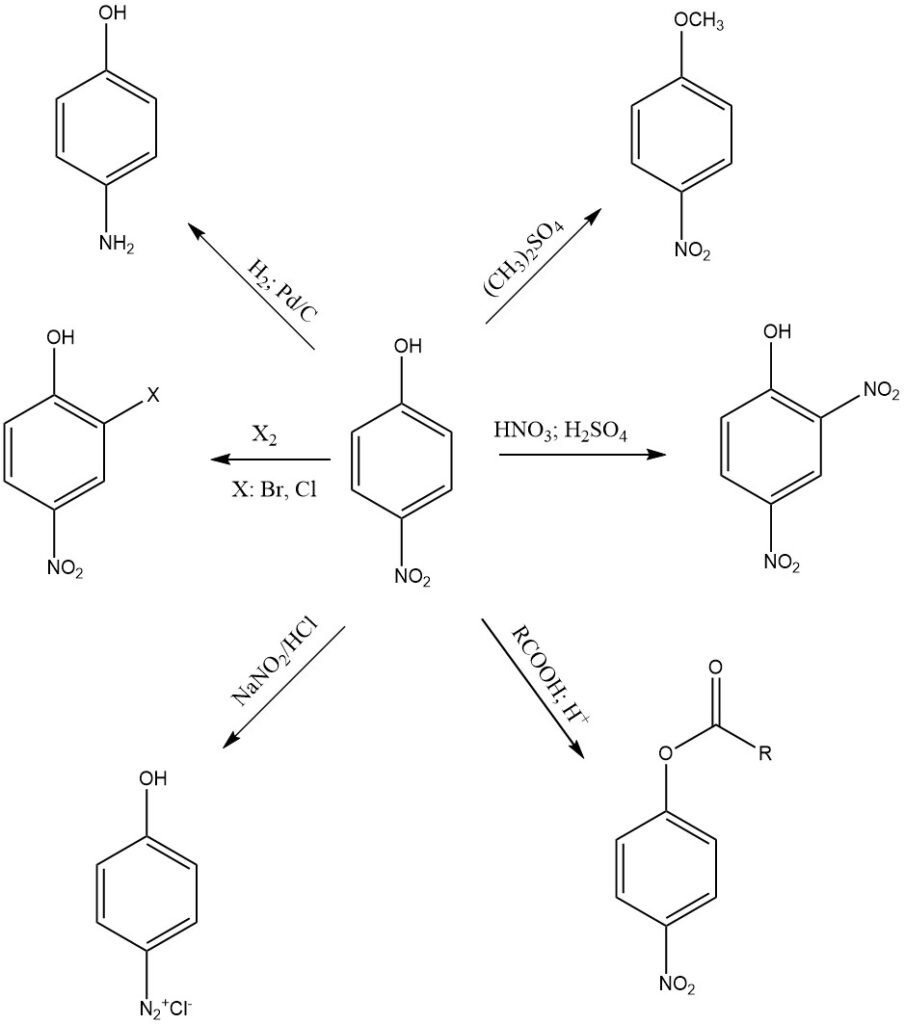
Reducción
Una de las reacciones más comunes del 4-nitrofenol es la reducción del grupo nitro a amina. El 4-nitrofenol se puede reducir a 4-aminofenol en diversas condiciones. Los agentes reductores comunes incluyen ditionito de sodio, zinc y hierro en HCl concentrado o gas hidrógeno.
El 4-nitrofenol se puede alquilar para formar una variedad de derivados. Los agentes alquilantes comunes incluyen sulfato de dimetilo y yoduro de metilo. Los derivados alquilados de 4-nitrofenol se utilizan a menudo como intermediarios en la síntesis de otros compuestos orgánicos.
Esterificación
El 4-nitrofenol puede sufrir esterificación, donde reacciona con ácidos carboxílicos para formar ésteres. Esta reacción suele estar catalizada por un ácido, como el ácido sulfúrico (H2SO4).
El 4-nitrofenol se nitra en presencia de ácido nítrico y ácido sulfúrico para formar 2,4-dinitrofenol. Una nitración adicional produce ácido pícrico, que es un explosivo más potente que el 2,4-dinitrofenol y se utiliza en una variedad de aplicaciones industriales y militares.
diazotización
El 4-nitrofenol también puede participar en reacciones de diazotización, proceso que convierte el grupo amino (-NH2) del 4-aminofenol en una sal de diazonio (-N2+X-). Esta reacción se utiliza en la síntesis de diversos tintes y compuestos aromáticos con grupos diazo.
Reacciones ácido-base
El 4-nitrofenol es ácido debido a su grupo hidroxilo. Reacciona con bases fuertes como el hidróxido de sodio para formar iones de 4-nitrofenolato.
El 4-nitrofenol también sufre reacciones de anillos aromáticos como halogenación, sulfonación, acilación y alquilación, particularmente en la posición orto del grupo (-OH).
3. Producción de 4-Nitrofenol
3.1. Hidrólisis de 4-cloronitrobenceno
Se calienta 4-cloronitrobenceno en un autoclave con una solución de hidróxido de sodio al 8,5%. La reacción exotérmica alcanza los 170°C y se mantiene durante 8 horas. Luego la solución se enfría y se acidifica para producir 4-nitrofenol con un rendimiento del 95%.

El proceso produce 4-nitrofenol de alta pureza e incluye los siguientes pasos:
- Hidrólisis básica del 4-cloronitrobenceno.
- Concentración del medio de reacción.
- Acidificación para obtener el compuesto 4-nitrofenol a partir de su sal.
- Decantación líquido/líquido para eliminar la fase acuosa obtenida tras la acidificación
- Cristalización del compuesto 4-nitrofenol.
- Separación del producto
El paso de concentración elimina las impurezas volátiles y el paso de decantación elimina las impurezas solubles en agua. El paso de cristalización purifica aún más el 4-nitrofenol eliminando las impurezas restantes.
Este proceso produce un 4-nitrofenol con un bajo contenido de impurezas liposolubles (como el 4-cloronitrobenceno) e impurezas solubles en agua (como el cloruro de sodio y el sulfato de sodio). El 4-nitrofenol tampoco contiene impurezas sulfurosas, lo que resulta ventajoso para reacciones de hidrogenación catalítica posteriores.
3.2. Nitración de fenol
El fenol se hace reaccionar con ácido nítrico en presencia de ácido sulfúrico para producir una mezcla de 2-nitrofenol y 4-nitrofenol. Luego se destila la mezcla para separar los dos isómeros. El 4-nitrofenol obtenido de la etapa de destilación se purifica adicionalmente mediante cristalización o recristalización.

Un proceso más eficiente para producir 4-nitrofenol a partir de fenol en un medio de ácido nítrico es un método que consta de dos pasos: nitrosación y nitración. En la etapa de nitrosación, el fenol se hace reaccionar con ácido nitroso para producir p-nitrosofenol.
En el paso de nitración, el p-nitrosofenol se hace reaccionar con ácido nítrico para producir 4-nitrofenol. El proceso se lleva a cabo en un medio de ácido nítrico de concentración en el rango de 5 a 30% en peso, y la temperatura se mantiene en el rango de 0-10°C durante la nitrosación y 15-30°C durante la nitración.
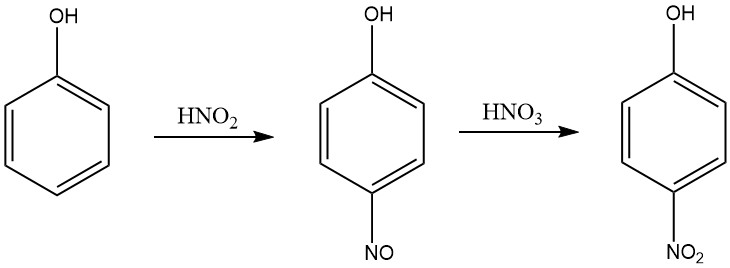
El ácido nitroso se produce en ácido nítrico acuoso mediante adición de óxidos de nitrógeno, como óxido nítrico, tetróxido de nitrógeno o trióxido de nitrógeno. El 4-nitrofenol se separa de la mezcla de reacción mediante cristalización.
Este proceso es ventajoso porque produce 4-nitrofenol con un bajo contenido de isómero orto.
4. Usos del 4-nitrofenol
La reducción de 4-nitrofenol a 4-aminofenol se utiliza menos porque los procesos para reducir directamente el nitrobenceno son más comunes.
El 4-nitrofenol reacciona con cloruros dialquiltiofosfóricos a 125°C en clorobenceno para formar un grupo de insecticidas que incluye el paratión. Pero este compuesto ha sido reemplazado por alternativas menos tóxicas como el metilparatión y sustancias relacionadas.
El 4-nitrofenol reacciona con el 4-cloro-3-nitrobenzotrifluoruro para formar fluorodifeno, que está relacionado con el nitrofeno. Este herbicida se utiliza para tratar cultivos de arroz sembrados.
El 4-nitrofenol se utiliza en otras aplicaciones que incluyen:
- Productos farmacéuticos: el 4-nitrofenol se utiliza como intermediario en la síntesis de paracetamol (también conocido como acetaminofén), un analgésico y antifebril común de venta libre.
- Fungicidas: el 4-nitrofenol es un precursor de algunos fungicidas, como dinocap y binapacryl.
- Tintes: el 4-nitrofenol se utiliza para producir una variedad de tintes, incluidos tintes amarillos, naranjas y rojos.
- Curtido del cuero: El 4-nitrofenol se utiliza para oscurecer el cuero.
5. Toxicología del 4-nitrofenol
| Exposición | LD50 |
|---|---|
| Dérmica, cobaya | >1 g/kg |
| Oral, ratón | 282 mg/kg |
| Oral, rata | 202 mg/kg |
| Piel, rata | 1024 mg/kg |
| Inhalación, rata | > 4,7 mg/l/4H |
| Sensibilización de la piel, cobaya | Ninguno sensibilizado |
- Efectos agudos: La inhalación o ingestión de 4-nitrofenol puede provocar dolores de cabeza, somnolencia, náuseas y cianosis (color azul en labios, orejas y uñas). El contacto con los ojos puede causar irritación.
- Efectos crónicos: No hay información disponible sobre los efectos crónicos del 4-nitrofenol en humanos o animales por inhalación o exposición oral.
- Efectos reproductivos/de desarrollo: No hay información disponible sobre los efectos reproductivos o de desarrollo del 4-nitrofenol en humanos.
- Riesgo de cáncer: No hay información disponible sobre los efectos cancerígenos del 4-nitrofenol en humanos. No hubo evidencia de actividad cancerígena en ratones expuestos dérmicamente al 4-nitrofenol durante 18 meses en un estudio del Programa Nacional de Toxicología (NTP).
Referencias
- Nitro Compounds, Aromatic, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a17_411
- Process for preparation of a nitrophenol. – https://patents.google.com/patent/US20080045756A1/en
- Preparation of p-nitrophenols. – https://patents.google.com/patent/US3510527A/en
- https://www.epa.gov/sites/default/files/2016-09/documents/4-nitrophenol.pdf
- https://fscimage.fishersci.com/msds/96371.htm
