Industrielle Produktion von Caprolactam
Caprolactam, der Hauptbestandteil von Nylon-6, kann auf verschiedenen Wegen hergestellt werden. Die gebräuchlichste Methode ist die Umwandlung von Cyclohexanon in Cyclohexanonoxim durch Ammoximation oder Wasserstoffperoxidverfahren. Dieses Oxim durchläuft dann eine Beckmann-Umlagerung zu Caprolactam.
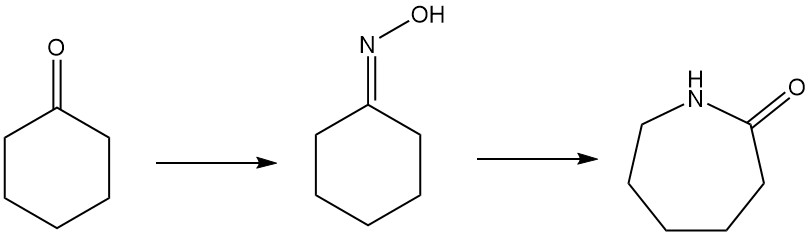
Andere Prozesse umfassen die Herstellung durch Photooximation und Toluol-basierte Verfahren oder werden aus Nylon-6-Abfällen gewonnen. Es entstehen innovative Prozesse, darunter die ALTAM-Route, die Butadien- oder Adipodinitril-basierte Methoden nutzt, die aus erneuerbaren Ressourcen wie Furfural oder Biomasse gewonnen werden.
Moderne Caprolactam-Anlagen sind komplexe, mehrstufige Betriebe, wobei die aktuellen Einzellinienkapazitäten für die weithin lizenzierte Fibrant HPO-Technologie beeindruckende 200.000 Tonnen pro Jahr erreichen.
Während Cyclohexanon als Ausgangsstoff dominiert (>98 %), können auch Cyclohexan und Toluol eingesetzt werden. Insbesondere werden die Phenolhydrierung und verschiedene Oxidationswege für Cyclohexan eingesetzt, um das Schlüsselzwischenprodukt zu erhalten. Der kombinierte Wirkungsgrad der Umwandlung von Cyclohexanon in Caprolactam beträgt etwa 98 %.
Inhaltsverzeichnis
1. Herstellung von Caprolactam über das Cyclohexanon-Verfahren
Die moderne Caprolactam-Produktion basiert auf Benzol, das aus BTX-Strömen als Hauptrohstoff gewonnen wird. Alle kommerziellen Verfahren außer einem verwenden Cyclohexanonoxim als Zwischenprodukt. Dieses Oxim entsteht durch die Reaktion von Cyclohexanon mit Hydroxylamin, das durch verschiedene Methoden erzeugt wird, wie zum Beispiel:
- Raschig-Prozess
- NO Hydrierung im Schwefelsäureverfahren
- Fibrant HPO-Prozess
- Ammoximationsprozess
1.1. Cyclohexanonoxim nach dem Raschig-Verfahren
Bei diesem Verfahren wird das Cyclohexanonoxim durch die Reaktion von Cyclohexanon und Hydroxylaminsulfat hergestellt und Ammoniak zur Neutralisierung des Oximsalzes verwendet. Als Nebenprodukt dieser Reaktion entsteht Ammoniumsulfat.
Mehrere Verbesserungen, sogenannte Raschig-Prozesse, wurden implementiert, um die Ausbeute an Cyclohexanonoxim zu steigern und die Sulfatsalzproduktion zu minimieren. Modifizierte Raschig-Prozesse, die einzigen, die noch in Betrieb sind, erzeugen als Nebenprodukt ausschließlich Ammoniumsulfat.
Im modifizierten Raschig-Verfahren reagieren zunächst die Rohstoffe (Ammoniak, CO2, SO2, Wasser und Luft) über Gleichung (1) zu Hydroxylaminsulfat. Anschließend reagiert Hydroxylaminsulfat mit Cyclohexanon unter Bildung von Cyclohexanonoxim (Gleichung (2)).
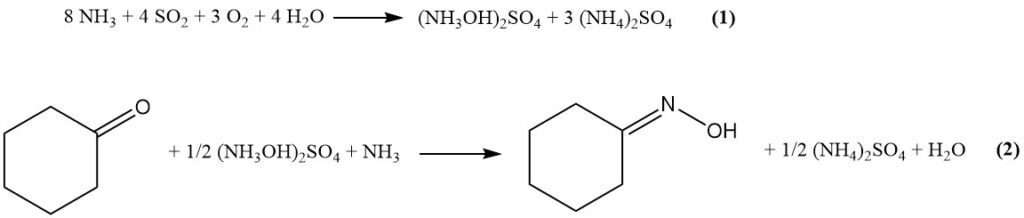
Die wichtigsten Prozessschritte sind unten aufgeführt:
Ammoniak absorbiert CO2 in Wasser und bildet eine Ammoniumcarbonat-/Bicarbonatlösung.
Ammoniak verbrennt mit Luft (Pt/Rh-Katalysatoren) bei ~850 °C, um NOx und Wasser zu erzeugen. Die heißen Gase werden gekühlt, wobei die exotherme Oxidationswärme zurückgewonnen und das Nebenprodukt verdünnte Salpetersäure kondensiert wird.
Lachgasgemisch und Ammoniumcarbonat/Bicarbonatlösung reagieren bei <10°C und pH 15 zu Ammoniumnitrit.
Bei der Schwefelverbrennung entsteht SO2 (10–20 Vol.-%), mit Wärmerückgewinnung zur Dampferzeugung.
- SO2 reagiert mit einer wässrigen Mischung aus Ammoniumnitrit und Ammoniumhydroxid unter Bildung von Hydroxyimidodischwefelsäure. Temperatur und das NH4OH/NH4NO2-Verhältnis sind wichtige Parameter zur Minimierung von Nebenprodukten.
Hydroxyimidodischwefelsäure wird hydrolysiert und neutralisiert, um über Ammonium-N-hydroxysulfamat Hydroxylaminsulfat zu bilden.
Oximation von Cyclohexanon mit Hydroxylaminsulfat bei pH 4,5 und 50–100 °C ergibt Cyclohexanonoxim.
Wässriges Ammoniak neutralisiert freigesetzte Schwefelsäure und gleichzeitig produziertes Ammoniumsulfat wird durch Verdampfungskristallisation zurückgewonnen.
Weitere Nebenprodukte des Raschig-Prozesses sind nitrose Gase in Abgasen der Nitritbildung, Stickstoffgas aus der Ammoniumnitritzersetzung und N2O-Gas aus verschiedenen Zersetzungsreaktionen.
1.2. NO Hydrierung im Schwefelsäureprozess
Um die Koproduktion von Ammoniumsulfat zu minimieren, BASF, Cyclopol und Inventa entwickelte Verfahren zur katalytischen NO-Reduktion mit Wasserstoff zu Hydroxylaminsulfat in verdünnter Schwefelsäure. NO selbst wird durch katalytische Ammoniakoxidation mit reinem Sauerstoff und Wasserdampf erzeugt.
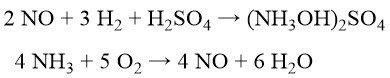
Die anschließende Oximproduktion ähnelt dem Raschig-Verfahren (Gleichung (2)). Dieser Weg erzeugt mit der Neutralisierung von überschüssigem H2SO4 immer noch etwa 0,7 kg Ammoniumsulfat pro kg Cyclohexanonoxim.
Explosionsrisiken werden durch die kontrollierte Gaszusammensetzung während der Hydroxylaminsulfat-Synthese gemindert. Umfangreiche Rohstoffreinigungen und aufwändige Katalysatoraufarbeitungen sind erforderlich.
Ein ca. 14 %iges Ammoniak, ein O2/NH3-Verhältnis von ca. 1,34 und ein Dampfgemisch strömen bei ca. 850 °C über einen Pt/Rh-Katalysator, um hauptsächlich NO und andere Stickoxide zu bilden. Das heiße Gas kühlt in einem Abhitzekessel (der Dampf erzeugt) ab und kühlt dann weiter ab, um Wasser zu kondensieren und Salpetersäure zu verdünnen.
Das verbleibende NO2 wird in aufeinanderfolgenden Türmen mit verdünnter Salpetersäure und Natronlauge ausgewaschen, wodurch eine Reinheit von ~95 % erreicht wird.
Die Hydroxylamin-Synthese umfasst mehrere Linien von 5–7 gut gerührten Reaktoren mit jeweils 20 m3, die kontinuierlich betrieben werden. Jeder Reaktor erhält eine 20 Gew.-%ige gereinigte Schwefelsäurelösung mit ca. 35 g/l fein dispergiertem Pt-Graphit-Katalysator (ca. 0,5 Gew.-%). Alle Reaktoren erhalten gereinigtes NO und überschüssigen Wasserstoff. Die Reaktionstemperatur beträgt ~45°C.
Während atmosphärischer Druck verwendet wird, kann erhöhter Druck vorteilhaft sein. Eine den Katalysator enthaltende Hydroxylaminsulfatlösung mit ca. 25 Gew.-% verlässt den letzten Reaktor und wird filtriert. Die konzentrierte Katalysatoraufschlämmung wird in den ersten Reaktor zurückgeführt.
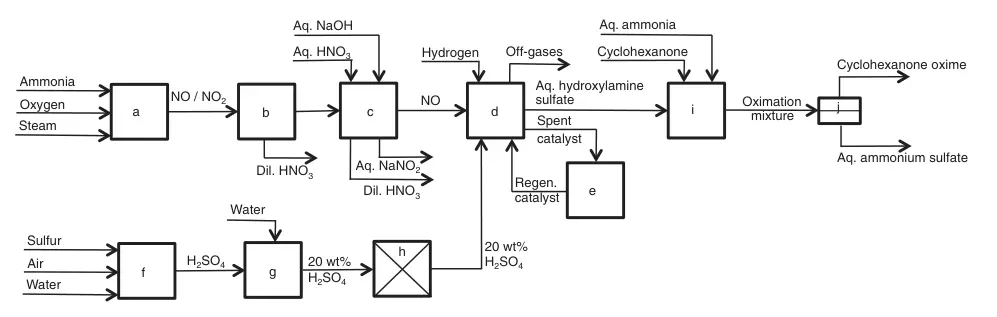
a) Ammoniakverbrennung; b) Kondensation; c) KEIN Waschen; d) NO-Reduktion; e) Katalysatorregeneration; f) Schwefelverbrennung; g) Verdünnung; h) Reinigung; i) Cyclohexanonoximierung; j) Trennung von Cyclohexanonoxim und wässrigem Ammoniumsulfat
Extrem korrosive Reaktionsmischungen und Katalysatorempfindlichkeit erfordern eine sorgfältige Materialauswahl. Inventa schlug Gummi-/Kunstharz-Auskleidungen vor, und BASF schlug spezielle kupferfreie Stahlsorten vor.
Die erzeugte Hydroxylaminsulfatlösung reagiert mit Cyclohexanon bei einer Temperatur (85–90 °C), die über dem Schmelzpunkt des wässrigen Cyclohexanonoxims liegt. Die resultierende wässrige Ammoniumsulfatphase trennt sich von der etwa 7 Gew.-% wasserhaltigen organischen Phase und beide werden getrennt verarbeitet.
Cyclohexanonoxim wird mit Cyclohexanon aus der Ammoniumsulfatphase extrahiert und später durch Destillation zurückgewonnen. Die Verdampfungskristallisation der verbleibenden Lösung ergibt etwa 0,7 kg kristallines Ammoniumsulfat pro kg Cyclohexanonoxim. Nach teilweiser Trocknung ist das wasserhaltige Oxim bereit für die Beckmann-Umlagerung zur Herstellung von Caprolactam.
1.3. Fibrant HPO® Prozess
Das in den 1960er Jahren von Fibrant entwickelte HPO-Verfahren (Hydroxylaminphosphatoxim) bietet einen einzigartigen Ansatz zur Herstellung von Cyclohexanonoxim auf der Grundlage selektiver Nitrat Ionen-/Stickoxid-Hydrierung.
Diese kombinierte Hydroxylamin- und Oxim-Syntheseroute eliminiert das Nebenprodukt Ammoniumsulfat. Das HPO-Verfahren ermöglicht einen geschlossenen Kreislauf zwischen Hydroxylamin- und Oximsynthesen, indem es die Freisetzung von Schwefelsäure während der Oximbildung vermeidet.
Es dreht sich um das Recycling zweier Ströme: eines wässrigen Phosphorsäurepuffers und einer organischen Prozessphase. In diesem System finden mehrere Schlüsselreaktionen und Vorgänge statt.
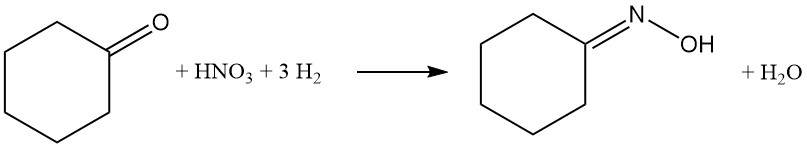
Durch die selektive katalytische Hydrierung von Nitrationen mit Wasserstoffgas in der Phosphorsäurepufferlösung entsteht Hydroxylamin. Bei einem pH-Wert der Reaktion von etwa 2 wird das resultierende Hydroxylamin protoniert und bildet Hydroxylammoniumphosphat. Als Katalysator wird Pd/Pt auf Kohlenstoff oder Aluminiumoxid verwendet.
Ein einzigartiges Dreiphasen-Blasensäulenreaktorsystem kombiniert optimalen Gas-Flüssigkeit-Feststoff-Kontakt mit effizienter Wärmeabfuhr. Nicht umgesetzter Wasserstoff wird nach der Abtrennung von der Katalysatorsuspension recycelt. Die Hydroxylammoniumphosphorsäure-Pufferlösung gelangt in den Oximierungsabschnitt.
Der wässrige Hydroxylamin-Phosphorsäure-Puffer wird mit einer organischen Toluol-Cyclohexanon-Phase umgesetzt, wandelt Cyclohexanon in Cyclohexanonoxim um und setzt Phosphorsäure frei. Dieser Oximierungsschritt erfolgt bei einem pH-Wert von etwa 2 und erzielt nahezu quantitative Umwandlungen sowohl von Hydroxylamin als auch Cyclohexanon.
Die gebildete organische Phase (Cyclohexanonoxim-Toluol) wird vom wässrigen Puffer abgetrennt, mit Wasser gewaschen und anschließend wird Toluol destilliert. Trockenes Oxim wird in die Beckmann-Umlagerungssektion geleitet, während destilliertes Toluol zurück zum Oximierungsreaktor zurückgeführt wird.
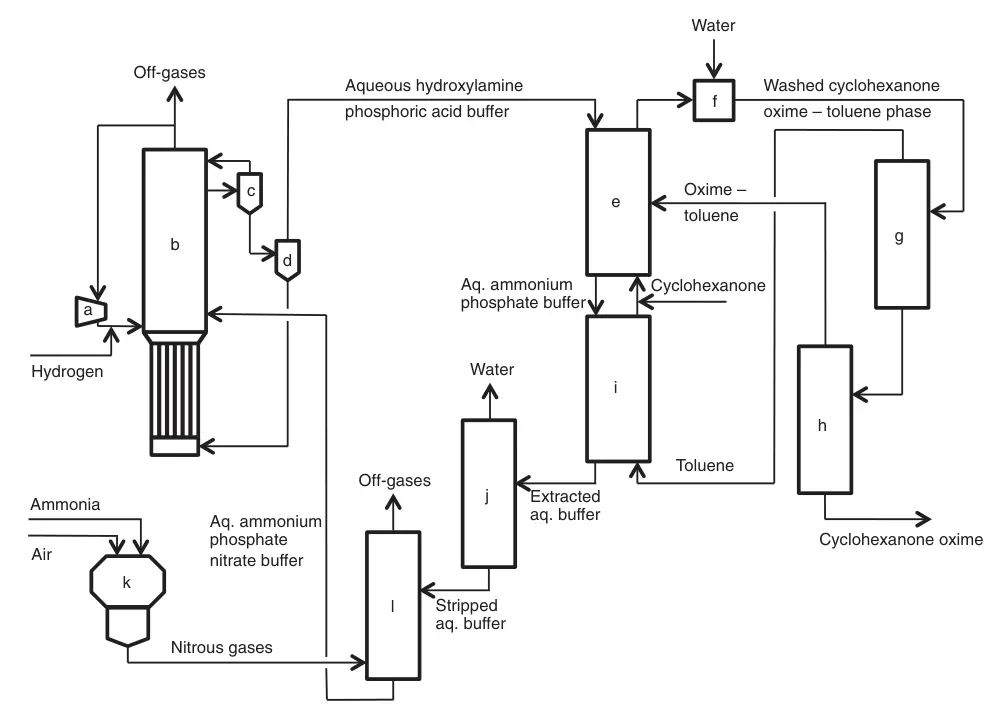
a) Kompressor; b) Nitrathydrierungsreaktor; c) Gas-Flüssigkeits-Abscheider; d) Katalysatorfiltration; e) Oximierung; f) Waschen; g) Toluol-Destillation; h) Cyclohexanonoxim-Reinigung; i) Extraktion; j) Dampfstrippung; k) Ammoniakverbrennung; l) Ammoniakzersetzung und Absorption nitroser Gase
Die kontinuierliche Weiterentwicklung des HPO-Prozesses führte zum intensivierten HPOplus-Prozess, der sich durch konzentrierte Prozessabläufe, einen reduzierten Rohstoff-/Energieverbrauch und eine deutlich erhöhte Einlinien-Oximkapazität (>200.000 t/a) auszeichnet.
1.4. Ammoximationsprozess
Die Cyclohexanon-Reaktion mit Ammoniak und Wasserstoffperoxid bietet einen alternativen Weg zur Cyclohexanonoxim-Synthese in der Flüssigphase, ohne dass Ammoniumsulfat als Nebenprodukt entsteht.
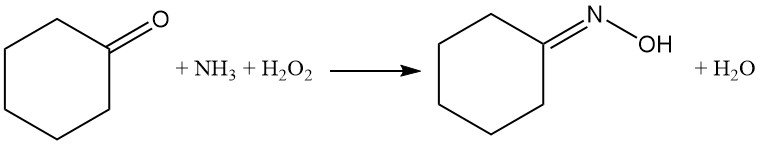
Der erste Erfolg dieses Ansatzes kam 1960 mit der Verwendung von Wolfram- und Zinnkatalysatoren in wässrigem Ammoniak bei 10–30 °C, wodurch hohe Oximausbeuten (>90 %) erzielt wurden. Allerdings behinderten Herausforderungen bei der Extraktion und Katalysatorrückgewinnung die Kommerzialisierung.
Ende der 1970er Jahre wurde ein poröser Kunststoff (Titansilikalit (TS-1)) entwickelt, der zu neuen katalytischen Oxidationsprozessen führte. Im Jahr 1987 implementierte Montedipe TS-1 für die Cyclohexanon-Ammoximierung, gefolgt von ähnlichen Verfahren von Sinopec.
Ammoniak reagiert mit Wasserstoffperoxid an den Titanzentren des Katalysators und bildet das Zwischenprodukt Hydroxylamin, das anschließend mit Cyclohexanon zum gewünschten Oxim reagiert.
Das molare Zufuhrverhältnis von H2O2/Cyclohexanon beträgt 1,0–1,1 und als Lösungsmittel wird ein stabiler tertiärer Alkohol (z. B. tert.-Butylalkohol) mit dem 2–4-fachen des Cyclohexanongewichts verwendet.
Die Reaktion wird bei einer Temperatur von ~85 °C und einem Druck von >0,25 MPa etwa 1,5 Stunden lang durchgeführt, um eine Umwandlung von Cyclohexanon zu Oxim von bis zu 98 % zu erreichen.
Die erste kommerzielle Anlage auf Basis dieser Technologie wurde 2003 von Sumitomo Chemical gebaut. Mehrere chinesische Caprolactam-Anlagen nutzen diese Technologie, teilweise mit TS-1-Varianten.
Eine vereinfachte Prozessbeschreibung ist in Abbildung 3 dargestellt:
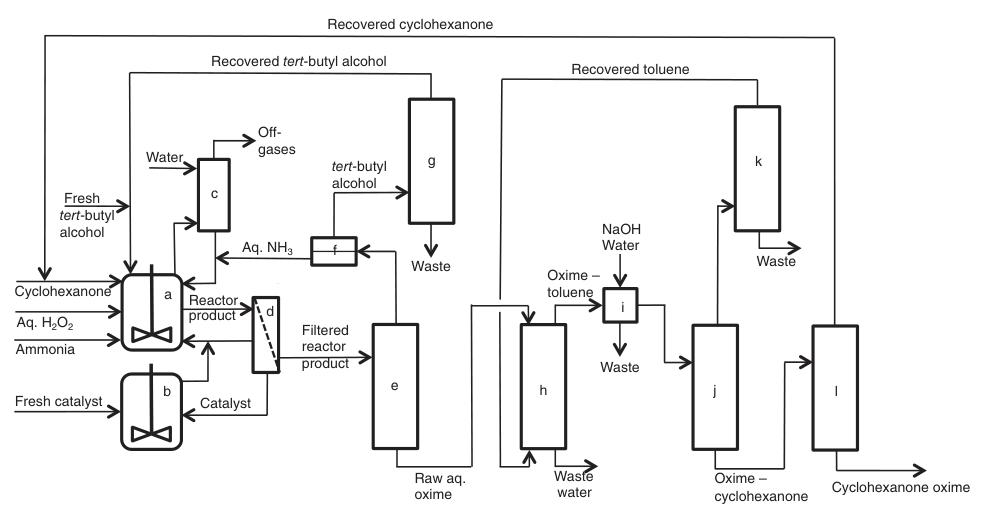
a) Ammoximationsreaktoren; b) Katalysatorvorbereitung/-reinigung; c) Abgaswäsche; d) Filtration; e) Ammoniak/tert-Butylalkohol-Rückgewinnung; f) L/L-Trennung; g) Tert-Butylalkohol-Destillation; h) Extraktion; i) Waschen; j) Lösungsmittelrückgewinnung; k) Lösungsmitteldestillation; l) Cyclohexanon-Rückgewinnung
Der Prozess beginnt damit, dass ein kontinuierlicher Ausgangsmaterialstrom, der verdünntes Wasserstoffperoxid, Cyclohexanon, Ammoniak, tert-Butylalkohol (sowohl frisch als auch recycelt) und Katalysator (entweder frisch oder recycelt) enthält, in gerührte Ammoximierungsreaktoren gelangt.
Die bei diesem Schritt entstehenden Abgase, die nicht umgesetztes Ammoniak enthalten, werden mit Wasser gewaschen, um das Ammoniak zurückzugewinnen und zu recyceln.
Das resultierende Produktgemisch wird dann filtriert und zur Trennung und Reinigung in eine Rückgewinnungskolonne geleitet. In dieser Phase können zwei alternative Wege genutzt werden:
1. Toluol-Extraktion:
Nicht umgesetztes Ammoniak und wasserhaltiger tert-Butylalkohol werden zurückgewonnen und zur Wiederverwendung gereinigt. Cyclohexanonoxim und nicht umgesetztes Cyclohexanon werden mit Toluol extrahiert, anschließend mit Wasser gewaschen und weiter durch Destillation getrennt.
2. Gegenstrom-Reextraktion:
In einem kontinuierlichen Gegenstrom-Reextraktionsschritt wird entmineralisiertes Wasser verwendet, um getrennte wässrige Oxim- und Cyclohexanonphasen zu bilden. Anschließend werden diese Phasen einer weiteren Reinigung durch Destillation unterzogen.
1.5. Beckmann-Umlagerung von Cyclohexanonoxim zu Caprolactam
Caprolactam, ein wichtiger Vorläufer für Nylon-6, wird hauptsächlich aus Cyclohexanonoxim über die Beckmann-Umlagerung hergestellt. Diese stark exotherme Reaktion findet sowohl in der Flüssig- als auch in der Gasphase statt.
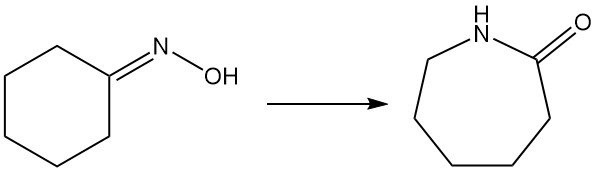
Die Umwandlung von Oxim in Caprolactam umfasst die traditionelle Beckmann-Umlagerung in der flüssigen Phase mit rauchender Schwefelsäure, wodurch Ammoniumsulfat als Nebenprodukt. Sumitomo Chemical verwendet jedoch ein einzigartiges Beckmann-Umlagerungsverfahren in der Dampfphase.
Ein niedriger Preis für Ammoniumsulfat macht dessen Koproduktion unerwünscht, was die Entwicklung von Prozessen zur Minimierung oder Eliminierung dieser Ammoniumsulfate motiviert. Allerdings kann Ammoniumsulfat auch die Caprolactam-Produktion fördern, wenn es als Dünger unter bestimmten Bodenbedingungen verwendet wird und für eine Stickstoff-, Schwefel- und pH-Anpassung sorgt.
1.5.1. Beckmann-Umlagerung in flüssiger Phase
Die vorherrschende industrielle Methode nutzt rauchende Schwefelsäure oder Oleum als Katalysator und Lösungsmittel. Es erreicht eine hohe Oximumwandlung und die Caprolactam-Ausbeute beträgt nahezu 100 %, es entsteht jedoch Ammoniumsulfat als Nebenprodukt.
Die Reaktionsparameter wie Temperatur, Säurekonzentration und Mischen haben einen erheblichen Einfluss auf die Reinheit und Farbe des Produkts. Eine mehrstufige Umlagerung mit verteilter Oleumzufuhr reduziert die Ammoniumsulfatproduktion.
Die abschließende Caprolactam-Reinigung umfasst Lösungsmittelextraktion, Destillation und Waschen.
1.5.2. Gasphasenumlagerung (heterogene katalytische Umlagerung)
Die Gasphasenumlagerung wurde entwickelt, um die mit Flüssigphasenmethoden verbundene Ammoniumsulfatbildung zu vermeiden. Frühe Versuche mit wassereliminierenden Katalysatoren hatten mit geringer Selektivität und Katalysatordeaktivierung zu kämpfen.
Sumitomo Chemical erzielte industriellen Erfolg mit Zeolithen mit hohem Siliciumdioxidgehalt in Gegenwart von Wasser und Methanol.
Bei diesem Verfahren wird eine feuchte Oxim/Methanol-Mischung eingedampft. Das Oxim wird dann über einem MFI-Zeolithkatalysator bei 350–380 °C in Caprolactam umgewandelt. Der Katalysator wird in einem Wirbelschichtsystem kontinuierlich mit Luft bei 500 °C regeneriert.
Die Verunreinigungen aus dem entstehenden Caprolactam werden durch Destillation entfernt. Die weitere Reinigung von Caprolactam durch Kristallisation aus einem gemischten Lösungsmittel sowie durch Hydrierung und mehrstufige Destillation ergibt ein hochreines Produkt.
Sumitomo Chemical ist der einzige kommerzielle Hersteller, der die Gasphasenumlagerung ohne Erzeugung von Ammoniumsulfat nutzt.
2. Herstellung von Caprolactam durch Photooximation
In den 1950er Jahren entwickelte Toray ein einzigartiges photochemisches Verfahren zur Herstellung von Caprolactam. Diese als Photonitrosierung (PNC) bezeichnete Methode umgeht die herkömmliche Oximsynthese durch direkte Umwandlung von Cyclohexan in Cyclohexanonoxim-Dihydrochlorid, gefolgt von der anschließenden Beckmann-Umlagerung zu Caprolactam.
Das Cyclohexan wird mit Nitrosylchlorid umgesetzt, um Cyclohexanonoximhydrochlorid zu ergeben, wobei die folgenden Reaktionen folgen:
1. Bildung von Nitrosylschwefelsäure: Lachgase, die bei der Ammoniakverbrennung entstehen, werden mit Schwefelsäure zu Nitrosylschwefelsäure (NOHSO4) umgesetzt.
2 H2SO4 + NO + NO2 → 2 NOHSO4 + H2O
2. NOCl-Produktion: NOHSO4 reagiert mit Chlorwasserstoff (HCl) zur Produktion von NOCl bei gleichzeitiger Regenerierung von Schwefelsäure.
NOHSO4 + HCl → NOCl + H2SO4
3. Photochemische Umwandlung:
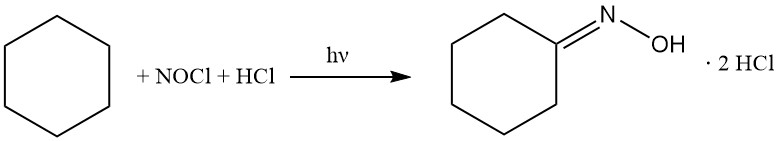
Das PNC-Verfahren basiert auf der photochemischen Reaktion von Cyclohexan mit NOCl in Gegenwart von überschüssigem HCl. Diese Umwandlung wird durch Hochleistungs-LED-Lampen, die aktinisches Licht aussenden, erleichtert und führt zur selektiven Bildung von Cyclohexanonoxim-Dihydrochlorid als ölige Unterschicht.
Insbesondere bieten LED-Lampen im Vergleich zu früheren Quecksilberlampenalternativen eine überlegene Energieeffizienz (0,4 kg Oxim pro kWh) und molare Selektivität (86 %).
Das gewonnene Oximdihydrochlorid wird einer Beckmann-Umlagerung mit Oleum unterzogen, wodurch Caprolactam entsteht. Nicht umgesetztes Cyclohexan wird recycelt, während freigesetzter Chlorwasserstoff durch einen wässrigen Absorptions- und Konzentrationsprozess zurückgewonnen wird.
Die Rohcaprolactamlösung wird mit Ammoniak neutralisiert und einer weiteren Reinigung durch chemische Behandlung, Trocknung und Destillation unterzogen. Bei diesem Prozess entstehen pro Tonne Caprolactam 1,55 Tonnen Ammoniumsulfat.
3. Rückgewinnung von Caprolactam aus Nylon-6-Abfällen
Nylon-6-Abfälle, die während des gesamten Lebenszyklus von der Produktion bis zur Endproduktentsorgung entstehen, bieten eine Möglichkeit zur Ressourcenrückgewinnung. Durch Depolymerisationsverfahren wird wertvolles Caprolactam aus diesen Abfallströmen zurückgewonnen, was sowohl ökologische als auch wirtschaftliche Vorteile bietet.
Feste Nylon-6-Abfälle werden in einem Hochdruckkesselreaktor unter Verwendung von überhitztem Dampf und einem Crackkatalysator (typischerweise Phosphorsäure) zu Caprolactam depolymerisiert. Diese Umwandlung kann auch ohne Katalysator unter erhöhtem Dampfdruck erfolgen.
Das resultierende Dampf-Caprolactam-Gemisch wird teilweise kondensiert und konzentriert. Anschließend reinigt ein Oxidationsmittel das Konzentrat, gefolgt von der abschließenden Reinigung des Caprolactams durch Destillation.
Waschwasser aus der Nylon-6-Chip-Produktion enthält neben dem Monomer auch Caprolactam-Oligomere. Der Depolymerisation geht eine Vorkonzentration durch Dünnschichtverdampfung voraus, wobei die gleiche Methode wie bei festen Abfällen angewendet wird.
Die resultierende wässrige Caprolactam-Lösung wird einer chemischen Reinigung und Destillation unterzogen, um Wasser, niedrigsiedende Fraktionen und das gewünschte Caprolactam-Produkt zu ergeben.
Alternative Methoden befassen sich auch mit der Depolymerisation von Oligomeren. Ein Ansatz besteht darin, das Waschwasser zu konzentrieren, um die Löslichkeit des Oligomers aufrechtzuerhalten, und die Caprolactam-Oligomer-Lösung in einen Festbett- oder Wirbelschichtreaktor einzuspeisen.
Ein spezieller Aluminiumoxidkatalysator spaltet die Oligomere bei 275–350 °C und erreicht dabei eine Ausbeute von 95 % im Verhältnis zum Einsatzmaterial. Konventionelle Reinigungsmethoden gewinnen anschließend das Caprolactam zurück.
Mehrere etablierte Technologien befassen sich mit Post-Consumer-Nylon-6-Abfällen, insbesondere weggeworfenen Teppichen. Diese Prozesse erfordern eine Sammlung, Sortierung und mechanische Zerkleinerung vor der Depolymerisierung zu Caprolactam in Neuqualität.
Bemerkenswerte Beispiele sind das „6ix Again“-Programm der BASF, das einen halbkontinuierlichen Reaktor mit Phosphorsäure und überhitztem Dampf für die Hochtemperatur-Depolymerisation (250–300 °C) verwendet. Durch anschließende Reinigung mit einem Oxidationsmittel und Vakuumdestillation wird Caprolactam aus dem Destillat zurückgewonnen.
Ein weiteres Verfahren ist Evergreen Nylon Recycling, eine zweistufige, nicht katalysierte Depolymerisationsmethode, bei der ein Hochdruckreaktorsystem und überhitzter Dampf zur Hydrolyse von zerkleinertem Material eingesetzt werden. Es gewinnt 90–95 % des ursprünglichen Nylon-6 als Caprolactam zurück, das für die Teppichproduktion geeignet ist.
4. Toluolbasierter Prozess
Dieses 1960 von Snia Viscosa entwickelte und bis Anfang der 1990er Jahre in Italien eingesetzte Verfahren auf Toluolbasis bietet einen alternativen Weg zur Caprolactam-Produktion. Der Prozess umfasst drei wesentliche Schritte:
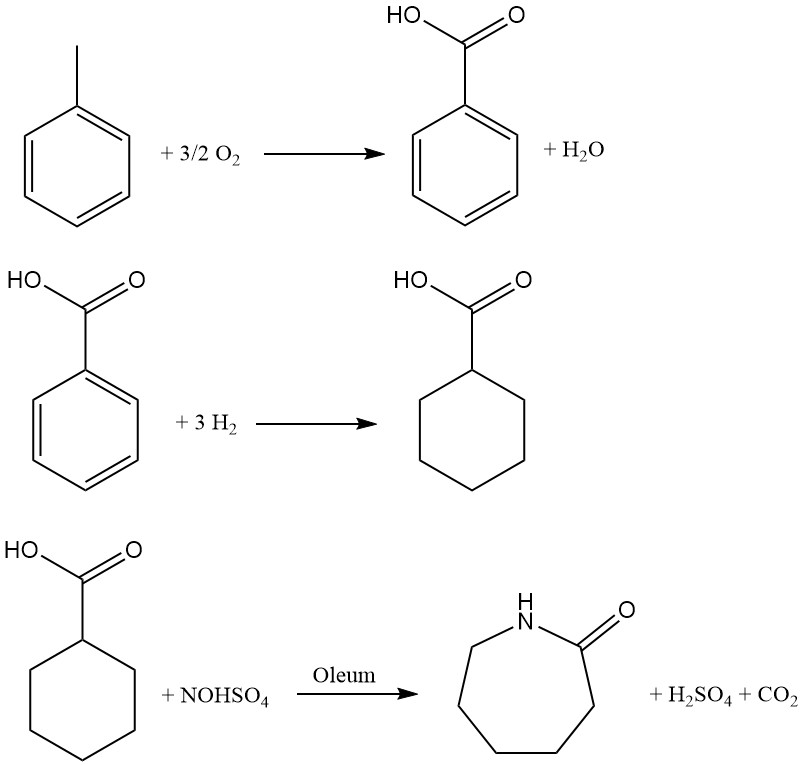
1. Katalytische Oxidation: Toluol wird in der flüssigen Phase mit einem Kobaltkatalysator bei 160–170 °C und einem Druck von 0,8–1 MPa an der Luft oxidiert. Die Rückgewinnung von nicht umgesetztem Toluol durch Kühlung gewährleistet eine optimale Ausbeute.
Das resultierende flüssige Produkt, das neben Zwischen- und Nebenprodukten etwa 30 % Benzoesäure enthält, erfordert zur Reinigung eine mehrstufige Destillation.
2. Hydrierung: Benzoesäure wird durch Hydrierung in der flüssigen Phase unter Verwendung eines Pd/C-Katalysators in Cyclohexancarbonsäure umgewandelt. Eine Reihe von Rührreaktoren, die bei etwa 170 °C und einem Druck von 1–1,7 MPa betrieben werden, ermöglichen eine effiziente Umwandlung. Eine anschließende Destillation unter vermindertem Druck reinigt die entstehende Säure.
3. Nitrosodecarboxylierung und Umlagerung: Dieser entscheidende Schritt kombiniert die Nitrosierung von Cyclohexancarbonsäure mit der Beckmann-Umlagerung, um direkt Caprolactam zu erzeugen. Bei der Reaktion in einem mehrstufigen Reaktor wird eine 73 %ige Nitrosylschwefelsäurelösung in Schwefelsäure verwendet, die durch konventionelle NO-Absorption in Oleum hergestellt wird.
Um die Umwandlungsrate auf etwa 50 % zu halten, muss der Prozess in siedendem Cyclohexan unter Atmosphärendruck stattfinden. Als unvermeidliche Nebenprodukte entstehen Sulfonsäuren.
Nach der kombinierten Nitrosierung-Umlagerung wird der Produktstrom bei niedrigen Temperaturen mit Wasser hydrolysiert. Durch die Extraktion nicht umgesetzter Cyclohexancarbonsäure kann diese wieder in den Prozess zurückgeführt werden.
Die saure Caprolactamlösung, die überschüssige Schwefelsäure enthält, gelangt dann in die Neutralisationsstufe. Durch Kristallisation unter reduziertem Druck mit Ammoniak entstehen zwei unterschiedliche Flüssigkeitsschichten: eine Ammoniumsulfatlösung und eine wässrige Caprolactamlösung. Eine weitere Reinigung umfasst:
- Toluol-Extraktion trennt Caprolactam von wasserlöslichen Nebenprodukten.
- Gegenstromextraktion mit Wasser gewinnt Caprolactam aus der Toluollösung zurück.
- Die Destillation liefert aus der konzentrierten wässrigen Lösung reines Caprolactam.
5. Alternative Prozesse
Über den herkömmlichen Cyclohexanon-Ammoximationsprozess hinaus sind mehrere alternative Wege zu Caprolactam entstanden:
5.1. Wasserstoffperoxid-Prozesse
- Inventa-Prozess: Cyclohexylamin-Oxidation mit Wasserstoffperoxid erzeugt Cyclohexanonoxim.
- 1,1´-Peroxydicyclohexylamin-Verfahren: Cyclohexanon und Wasserstoffperoxid reagieren zu einem Peroxid, das sich dann in Caprolactam umwandelt und Cyclohexanon regeneriert.
5.2. Oxidation von Cyclohexylamin mit elementarem Sauerstoff:
Direkte Oxidation von Cyclohexylamin mit Sauerstoff erzeugt Cyclohexanonoxim.
5.3. Direkte Oximierung von Cyclohexanon:
Ammoniak, Luft und Cyclohexanon reagieren direkt an verschiedenen Katalysatoren zu Cyclohexanonoxim.
5.4. Bis(nitrosocyclohexan)-Verfahren:
Elektrische Entladung löst die Reaktion von Cyclohexan mit Stickoxid oder verwandten Verbindungen aus und bildet Bis(nitrosocyclohexan), das sich zu Cyclohexanonoxim umlagert.
5.5. ε-Hydroxycapronsäure/ε-Caprolacton-Verfahren:
Durch die Oxidation von Cyclohexanon mit Luft entstehen ε-Hydroxycapronsäure und Adipinsäure (Nebenprodukt). Beide können auf unterschiedlichen Wegen in Caprolactam umgewandelt werden.
5.6. 2-Nitrocyclohexanon-Verfahren:
Eine einzigartige Reaktionsfolge mit Acetylierung, Nitrierung, Ringspaltung, Hydrierung und Cyclisierung wandelt Cyclohexanon ohne Nebenprodukte in Caprolactam um .
5.7. 3,3-Pentamethylenoxaziridin-Verfahren:
Hypochlorit reagiert mit Cyclohexanon in wässrigem Ammoniak unter Bildung von Cyclohexanon-Isoxim, das sich dann unter Hitze zu Caprolactam umlagert.
5.8. Katalytische Deacetylierung von N-Acetylcaprolactam:
O-Acetylcyclohexanonoxim wird an Katalysatoren deacetyliert, um Caprolactam zu ergeben.
5.9. Butadienbasierte Prozesse:
- ALTAM-Prozess: Dieser von DSM und anderen entwickelte mehrstufige Prozess nutzt Butadien, um letztendlich Caprolactam mit hoher Selektivität herzustellen.
- Adiponitril-basierte Prozesse: BASF und Rhone-Poulenc entwickelten unabhängige Prozesse für die Caprolactam-Produktion aus Adiponitril, das auf verschiedenen Wegen, einschließlich Butadien, gewonnen wird.
5.10. Bioregenerative Routen:
Angesichts zunehmender Nachhaltigkeitsbedenken gewinnen biobasierte Ressourcen als Rohstoffe für die Caprolactam-Produktion an Bedeutung. Mehrere vielversprechende Routen sind in der Entwicklung, mit Schwerpunkt auf:
- Drop-in-Chemikalien: Biologisch gewonnenes Benzol, Phenol, Acrylnitril oder HMF können problemlos in bestehende Caprolactam-Prozesse integriert werden.
- Chemische Wege: Lavulinsäure oder Furfural, aus Biomasse gewonnen, kann in Zwischenprodukte umgewandelt werden, die zu Caprolactam führen.
- (Teilweise) fermentative Wege: Mikrobielle Synthese von Lysin oder direkt Fermentation von Kohlenhydraten bieten potenzielle Wege zu Caprolactam-Vorläufern.
Obwohl bioerneuerbare Verfahren derzeit wirtschaftlich nicht mit herkömmlichen Methoden konkurrenzfähig sind, sind sie vielversprechend für eine zukünftige nachhaltige Caprolactam-Produktion.
Referenz
- Caprolactam; Ullmanns Enzyklopädie der industriellen Chemie. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a05_031.pub3
