Apfelsäure: Eigenschaften, Herstellung und Verwendung
Was ist Apfelsäure?
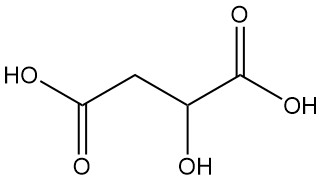
Apfelsäure, auch bekannt als Hydroxybernsteinsäure oder Hydroxybutandisäure, ist eine Dicarbonsäure mit der chemischen Formel C4H6O5. Es ist eine natürlich vorkommende organische Verbindung, die sich durch einen säuerlichen Geschmack auszeichnet.
Sie wurde erstmals von Sheele beschrieben, der diese Säure 1785 aus unreifen Äpfeln isolierte. Der Name Apfelsäure leitet sich vom lateinischen Wort für Apfel, malum, ab.
Apfelsäure ist ein Bestandteil verschiedener Früchte, insbesondere Äpfel. In biologischen Systemen dient Apfelsäure in ihrer ionisierten Form, Malat, als Zwischenprodukt im Tricarbonsäurezyklus. Dieser Stoffwechselweg ist für die Energieproduktion von entscheidender Bedeutung.
Das L-Isomer der Apfelsäure ist die in der Natur vorherrschende Form und besitzt biologische Aktivität. Obwohl sie in erster Linie für ihre Rolle als Lebensmittelaroma bekannt ist, deuten neuere Erkenntnisse auf potenzielle Vorteile für die menschliche Gesundheit hin.
Apfelsäure ist am Energiestoffwechsel beteiligt, insbesondere bei Hypoxie. Studien weisen auf ihr Potenzial hin, die körperliche Leistungsfähigkeit zu steigern und Symptome im Zusammenhang mit Fibromyalgie zu lindern.
Der Apfelsäurestoffwechsel wird durch Enzyme wie das Apfelsäureenzym beeinflusst. Dieses Enzym katalysiert die oxidative Decarboxylierung von Malat zu Pyruvat. Das erzeugte Pyruvat kann weitere Stoffwechselumwandlungen durchlaufen, einschließlich der Umwandlung in Glucose oder Oxalacetat.
Apfelsäure hat antimikrobielle Eigenschaften. Ihre saure Natur trägt zur Konservierung von Lebensmitteln bei, indem sie mikrobielles Wachstum hemmt. Ihre Wirksamkeit wird jedoch von Faktoren wie dem pH-Wert und bestimmten mikrobiellen Arten beeinflusst.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Apfelsäure
Apfelsäure ist ein weißes, geruchloses, kristallines Pulver mit saurem Geschmack. Sie ist gut löslich in Wasser, Methanol, Ethanol, Aceton, Ether und anderen polaren Lösungsmitteln.
Einige physikalische Eigenschaften von Apfelsäure sind in der folgenden Tabelle zusammengefasst.
| Eigenschaft | Wert |
|---|---|
| CAS-Nummer | [617-48-1] |
| Chemische Formel | C4H6O5 |
| Molekularmasse | 134,09 g/mol |
| Schmelzpunkt | 131 °C |
| Dichte | 1,60 g/cm3 |
| Viskosität einer 50%igen wässrigen Lösung bei 25 °C | 6,5 mPa.s |
| Verbrennungswärme bei 20 °C | -1,340 MJ/mol |
| pKa1 bei 20 °C | 3,51 |
| pKa2 bei 20 °C | 5,03 |
| Eigenschaft | Wert |
|---|---|
| CAS-Nummer | [97-67-6] |
| Schmelzpunkt | 100 °C |
| Dichte bei 20 °C | 1,595 g/cm3 |
| Spezifische Drehung bei 18 °C (7 Gew.-% in H2O) | -2,3° |
| Löslichkeit in Wasser bei 20 °C | 36,4 g/100 g |
2. Chemische Reaktionen der Apfelsäure
Da Apfelsäure Carbonsäure- und Hydroxylgruppen enthält, kann sie eine Vielzahl chemischer Reaktionen eingehen.
Als Carbonsäure reagiert Apfelsäure mit Basen und bildet Salze wie Natriummalat oder Kaliummalat.
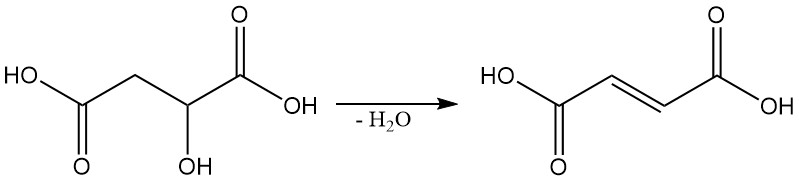
Unter bestimmten Bedingungen kann Apfelsäure dehydriert werden, um Fumarsäure zu produzieren.
Durch Decarboxylierung von Apfelsäure entsteht Brenztraubensäure.
Apfelsäure kann mit Alkoholen reagieren und Ester bilden, die häufig als Geschmacksstoffe verwendet werden.
Apfelsäure kann oxidiert werden und je nach Bedingungen verschiedene Produkte wie Oxalessigsäure, Oxalsäure und Kohlendioxid erzeugen.
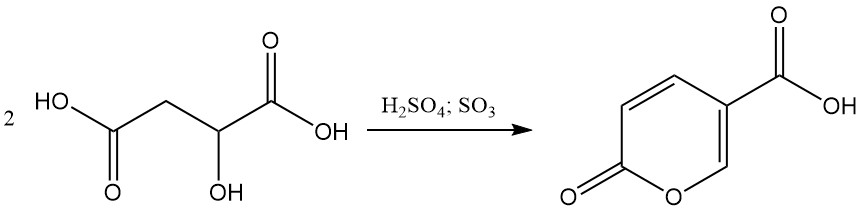
In Gegenwart von 20–30 % rauchender Schwefelsäure kondensiert Apfelsäure selbst und bildet Cumalsäure.
Apfelsäure kann Komplexe mit Metallionen wie Kalzium und Magnesium bilden.
Die malolaktische Gärung ist ein üblicher Prozess bei der Weinherstellung, bei dem Apfelsäure durch Bakterien in Milchsäure umgewandelt wird. Sie ist auch ein Zwischenprodukt im Krebs-Zyklus, in dem sie zu Oxalessigsäure oxidiert wird.
3. Herstellung von Apfelsäure
3.1. Chemische Herstellung von Apfelsäure
Die Apfelsäuresynthese beruht hauptsächlich auf chemischen Prozessen und ergibt racemische D,L-Apfelsäure. Der Vorläufer, Maleinsäureanhydrid, wird aus fossilen Kohlenwasserstoffen, hauptsächlich n-Butan, gewonnen. Benzol, ein ehemaliger Rohstoff, wird weiterhin verwendet, insbesondere in asiatischen Ländern.
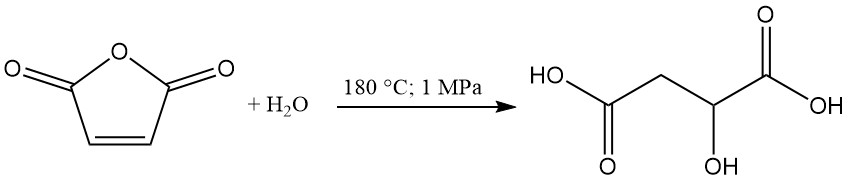
(R,S)-Äpfelsäure wird in den USA und Kanada industriell durch Hydratisierung von Maleinsäureanhydrid hergestellt. Alberta Gas ist der einzige US-Hersteller mit einer Produktionskapazität von etwa 5000 Tonnen pro Jahr.
Bei diesem Verfahren wird Maleinsäureanhydrid bei 180 °C unter 1 MPa Druck erhitzt, um als Hauptprodukt Äpfelsäure zu bilden. Maleinsäure und Fumarsäure entstehen als Nebenprodukte. Fumarsäure kann aufgrund ihrer geringen Wasserlöslichkeit durch Filtration abgetrennt und recycelt werden.
Durch anschließende Konzentration des Filtrats erhält man Äpfelsäure. Die Rohsäure wird durch wiederholtes Waschen, Eindampfen und Umkristallisieren gereinigt, um die Verunreinigungen durch Fumarsäure und Maleinsäure auf 7,5 bzw. <500 ppm zu reduzieren.
Um Äpfelsäure in pharmazeutischer Qualität zu erhalten, sind zusätzliche Reinigungsschritte erforderlich.
3.2. Enzymatische Produktion von L-Äpfelsäure
Enantiomerenreine L-Äpfelsäure, die für Pharmazeutika und Polymere bevorzugt wird, ist durch racemische D,L-Äpfelsäure-Trennung schwierig zu erhalten. Die enzymatische Synthese bietet eine selektive und mildere Alternative.
Die Fumarase-katalysierte Hydratisierung von Fumarsäure zu L-Äpfelsäure ist der wichtigste enzymatische Prozess. Dies kann durch die Verwendung gereinigter Enzyme, permeabilisierter oder lyophilisierter Zellen oder ganzer Zellen erreicht werden.
Mikroorganismen wie Saccharomyces cerevisiae, Brevibacterium flavus, Brevibacterium ammoniagenes und Rhizopus oryzae zeigen hohe Umwandlungsraten zwischen 80 % und ≈100 % bei der Ganzzellkatalyse. Die Immobilisierung macht den Prozess wirtschaftlicher, da der Katalysator wiederverwendbar ist.
3.3. Biosynthese von Apfelsäure durch Mikroorganismen
Die mikrobielle Apfelsäureproduktion bietet Vorteile gegenüber der chemischen Synthese, darunter die ausschließliche Bildung von L-Apfelsäure und die Verwendung vielfältiger, erneuerbarer Substrate.
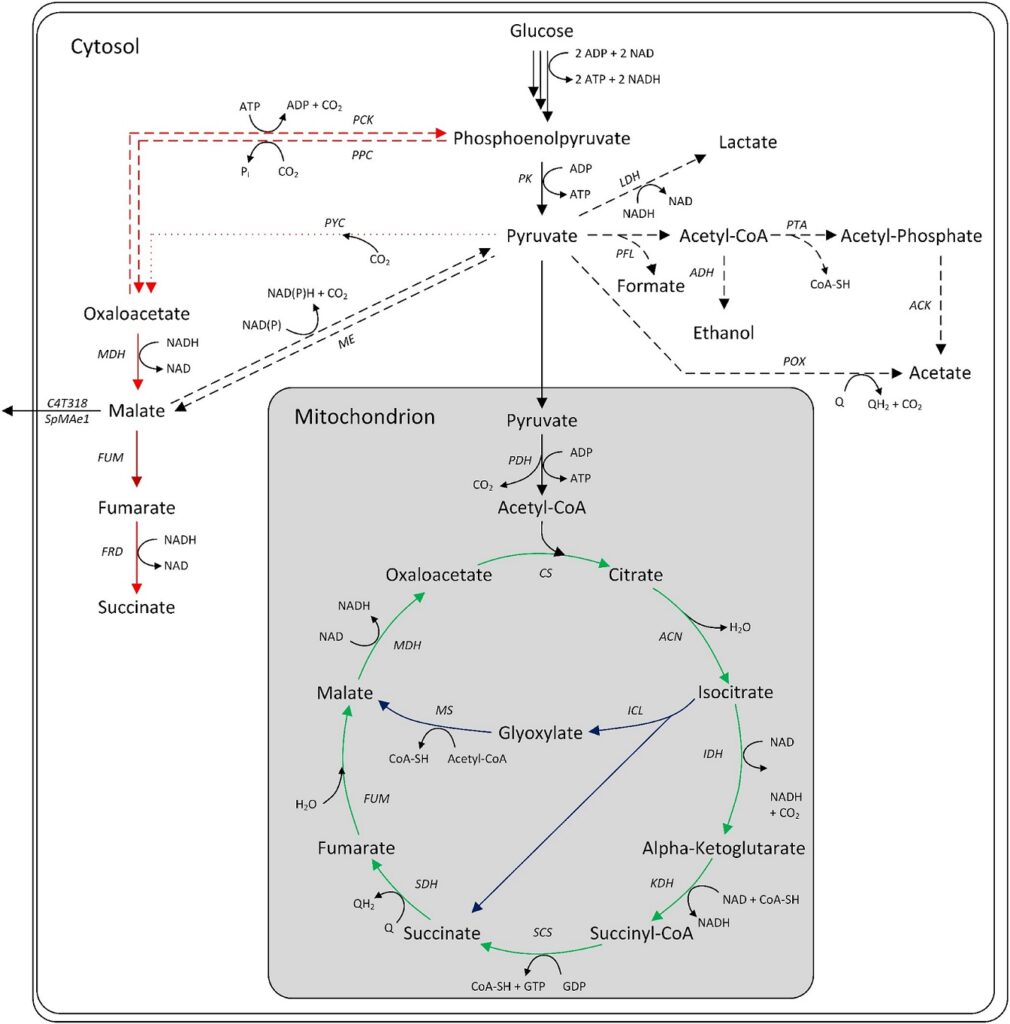
Es gibt drei primäre intrazelluläre Wege für die mikrobielle Apfelsäureproduktion: den oxidativen Tricarbonsäurezyklus (TCA), den reduktiven TCA-Zyklus (rTCA) und den Glyoxylatzyklus. Der oxidative TCA-Zyklus, der sich im Mitochondrium befindet, wandelt Acetyl-CoA in Citrat um, das anschließend unter Verlust von Kohlendioxid zu L-Malat oxidiert wird.
Die maximale theoretische Ausbeute beträgt 1 mol/mol. Einige Aspergillus-Arten besitzen zytosolische TCA-Isoformen, die einen reduktiven TCA-Weg ermöglichen. Dieser ATP-neutrale Weg carboxyliert Pyruvat zu Oxalacetat, das durch Malatdehydrogenase in L-Malat umgewandelt wird. Eine theoretische Ausbeute von 2 mol/mol Glucose ist möglich.
Der Glyoxylatzyklus wandelt Citrat in Succinat und Glyoxylat um, mit anschließender Kondensation zu L-Malat. Die maximale Ausbeute beträgt 1 mol/mol, kann aber auf 1,33 mol/mol ansteigen, wenn das verbrauchte Oxalacetat durch die Carboxylierung von Pyruvat wieder aufgefüllt wird.
Zu den bei der Herstellung von L-Äpfelsäure verwendeten Mikroorganismen zählen natürliche Mikroorganismen (wie Aspergillus flavus, Aspergillus oryzae, Ustilago trichophora und Rhizopus delemar) sowie gentechnisch veränderte Pilze und Bakterien.
4. Verwendung von Äpfelsäure
(R,S)-Apfelsäure hat dieselben physikochemischen Eigenschaften wie Zitronensäure und Weinsäure, besitzt aber ein milderes Geschmacksprofil. Diese Eigenschaft begünstigt ihre Anwendung in Lebensmitteln, bei denen der Säuregehalt der Zitronensäure unerwünscht ist. Beispiele hierfür sind Lebensmittelverpackungen und Backwaren.
In der Lebensmittelindustrie wird Apfelsäure häufig (etwa 85–90 %) als Säuerungsmittel und Säureregulator verwendet. Ihr Geschmack unterscheidet sich von dem der Zitronensäure und bietet eine weniger intensive, aber länger anhaltende Säure. Diese Eigenschaft hilft dabei, den Nachgeschmack künstlicher Süßstoffe zu überdecken und ausgewogene Geschmacksprofile in Getränken zu erzeugen.
Synergistische Wechselwirkungen zwischen Apfelsäure und Süßstoffen ermöglichen eine Süßstoffreduzierung von bis zu 20 % und potenzielle Kosteneinsparungen. Die Verwendung von wasserfreiem Apfelsäurepulver bietet zusätzliche wirtschaftliche Vorteile.
Zu den Hauptanwendungen gehören Süßwaren, Marmeladen, Gelees sowie Obst- und Gemüsekonserven. Die Vorschriften für Lebensmittelzusatzstoffe in den meisten Ländern erlauben ihre Verwendung.
Enantiomere Apfelsäuren, (R)-(+)-Apfelsäure und (S)-(-)-Apfelsäure, können durch (R,S)-Apfelsäurespaltung oder durch mikrobielle Fermentation von Fumarsäure gewonnen werden.
Außerhalb der Lebensmittelindustrie wird Apfelsäure als Puffer und Chelatbildner in Körperpflege- und Reinigungsprodukten verwendet. Zu den pharmazeutischen Anwendungen gehört die Verwendung als Arzneimittelbestandteil, während sie in der Halbleiterherstellung in Polier- und Reinigungsprozessen eingesetzt wird.
Darüber hinaus wird Apfelsäure in Tierfutter und als Bestandteil in Mischungen mit niedriger Übergangstemperatur eingesetzt.
Apfelsäure ist eine Dicarbonsäure, was ihre Verwendung als Polymerbaustein ermöglicht. Copolymere und Homopolymere der Apfelsäure weisen Eigenschaften wie Hydrophilie, Biokompatibilität und biologische Abbaubarkeit auf und finden potenzielle Anwendungen in Bereichen wie Arzneimittelverabreichung und Materialwissenschaft.
Zu den wichtigsten Herstellern von Apfelsäure zählen Bartek (Kanada), die japanischen Unternehmen Fuso Chemical und Mitsubishi Corporation Life Sciences, Isegen (Südafrika), Polynt (Italien), Thirumalai Chemicals (Indien), die chinesischen Unternehmen Changmao Biochemical Engineering Company, Anhui Sealong Biotechnology und Jinhu Lile Biotechnology Industry sowie Tate & Lyle (Großbritannien) und Yongsan Chemicals (Korea).
5. Toxikologie von Apfelsäure
Apfelsäure zeigt in Tierversuchen eine geringe akute Toxizität. Die oralen LD50-Werte liegen bei allen Spezies zwischen 1,6 und 5 g/kg. Die intravenösen und intraperitonealen LD50-Werte sind deutlich niedriger.
Chronische orale Studien an Ratten und Hunden ergaben nur minimale Nebenwirkungen, vor allem geringfügige Veränderungen des Körpergewichts und der Futteraufnahme. Studien zur Reproduktionstoxizität lieferten negative Ergebnisse.
Dermatologische Studien weisen auf mäßige Hautreizungen bei Kaninchen und schwere Augenreizungen bei Kaninchen hin. Apfelsäure ist ein starker Reizstoff für die Haut von Meerschweinchen.
Mutagenitätsbewertungen ergaben inkonsistente Ergebnisse. Apfelsäure selbst war in verschiedenen Tests nicht mutagen, aber ihre Pyrolysate und chlorierten Derivate zeigten mutagene Eigenschaften.
Hautreizungsstudien berichteten über dosisabhängige Effekte, wobei ein höherer pH-Wert mit einer stärkeren Reizung korrelierte. Prädiktive Tests bei Patienten mit atopischer Dermatitis zeigten eine mögliche Hautreaktivität gegenüber apfelsäurereicher Ernährung. Apfelsäure beeinflusste auch die Zellerneuerungsraten in Abhängigkeit vom pH-Wert.
Klinische Wirksamkeits- und Sicherheitsstudien berichteten von keiner Toxizität.
Chronische Toxizitätsstudien von Apfelsäure bei Ratten und Hunden ergaben No Observed Effect Levels (NOEL) von 5000 ppm bzw. 50000 ppm.
Daten zur chronischen Toxizität von Fumarsäure bei Ratten weisen auf einen No Observed Adverse Effect Level (NOAEL) von ungefähr 600 mg/kg Körpergewicht/Tag hin. Angesichts der metabolischen Umwandlung von Fumarsäure in Apfelsäure innerhalb des Krebs-Zyklus wird eine artenübergreifende Extrapolation als gültig angesehen.
Die Bewertung der Apfelsäureexposition anhand der Nahrungskonzentration in mg/kg/Tag ergab unsichere Ergebnisse. Die geschätzten Bereiche variierten zwischen 2–200 mg/kg/Tag und 25–2500 mg/kg/Tag. Durch die Anwendung von EFSA-Umrechnungsfaktoren wurde diese Unsicherheit ausgeglichen, was zu einem NOAEL von 260 mg/kg/Tag führte.
Referenzen
- Hydroxycarboxylic Acids, Aliphatic; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a13_507
- https://scijournals.onlinelibrary.wiley.com/doi/10.1002/jctb.6269
- https://pubmed.ncbi.nlm.nih.gov/11358110/
- https://onlinelibrary.wiley.com/doi/10.1002/0471743984.vse9535
- https://onlinelibrary.wiley.com/doi/10.1002/9780470995327.ch157
- https://echa.europa.eu/registration-dossier/-/registered-dossier/11511/7/6/1
- https://www.orgsyn.org/demo.aspx?prep=cv4p0201
