Diossano: proprietà, reazioni, produzione e usi
Il diossano, o 1,4-diossano, è un dietere eterociclico con formula C4H8O2. È un liquido infiammabile e incolore con un debole odore dolce simile all’etere dietilico. È noto con altri nomi come p-diossano, ossido di dietilene, biossido di dietilene, etere dietilene, 1,4-diossacicloesano, etere diossietilene e diossano.
Il diossano fu prodotto per la prima volta da A. V. Lourenço nel 1863 facendo reagire l’etilenglicole con 1,2-dibromoetano. Tuttavia, la produzione commerciale non ebbe luogo fino al 1929.
Sommario
1. Proprietà fisiche del diossano
Il diossano è un buon solvente con proprietà eccezionali. Scioglie facilmente un’ampia gamma di composti organici, tra cui idrocarburi alifatici e aromatici, eteri, alcoli, chetoni e idrocarburi clorurati, in particolare quelli con pesi molecolari inferiori.
Il 1,4-diossano è miscibile con acqua in tutte le proporzioni e dissolve anche vari composti ed elementi inorganici, tra cui cloruri di ferro, cloruro mercurico, acidi minerali (cloridrico, solforico e fosforico), alogeni (bromo, cloro e iodio), oli animali e vegetali, oli di paraffina e resine sintetiche e naturali.
A temperatura ambiente, il 1,4-diossano appare come un liquido limpido con un odore etereo. La sua stabilità chimica è paragonabile a quella di altri eteri alifatici. Similmente a questi eteri, il diossano forma perossidi se esposto all’aria.
Le proprietà fisiche più importanti del diossano sono elencate nella Tabella 1.
| Proprietà | Valore |
|---|---|
| Peso molecolare | 88,11 g/mol |
| Punto di ebollizione | 101,3 °C |
| Punto di congelamento | 11,8 °C |
| Densità | 1,0356 g/cm3 |
| Calore latente di Evaporazione | 413 kJ/kg |
| Calore di fusione | 141 kJ/kg |
| Calore specifico (20 °C) | 1,76 kJ kg-1 K-1 |
| Indice di rifrazione | 1,4224 |
| Pressione di vapore (20 °C) | 4,13 kPa (41,3 mbar) |
| Costante dielettrica (20 °C) | 2,23 |
| Tensione superficiale (20 °C) | 36,9 mN/m |
| Temperatura critica | 312 °C |
| Pressione critica | 5,14 MPa |
| Punto di infiammabilità (vaso chiuso) | 11 °C |
| Limiti di infiammabilità (in aria) |
Inferiore: 2 vol % Superiore: 22 vol % |
| Calore di Combustione | 27 600 kJ/kg |
| Temperatura di autoaccensione | 180 °C |
Il diossano forma miscele azeotropiche con molti solventi. Esempi comuni sono riportati nella Tabella 2.
| Componente | Punto di ebollizione del componente, °C | Diossano, % in peso | Punto di ebollizione azeotropico, °C |
|---|---|---|---|
| Acido formico | 100,7 | 57 | 113,35 |
| Nitrometano | 100,8 | 43,5 | 100,55 |
| Acido acetico | 117,9 | 20,5 – 23 | 119,4 |
| Etanolo | 78,5 | 9,3 | 78,1 |
| 3-Iodo-1-propene | 103 | 44 | 98,5 |
| 1-Propanolo | 97,4 | 45 | 95,3 |
| Alcool terz-amilico | 102,5* | 20 | 100,65 |
| Cicloesano | 80,7 | 24,6 | 79,5 |
| Eptano | 98,4 | 44 | 91,85 |
| Acqua | 100 | 82 | 87,8 |
2. Reazioni chimiche del diossano
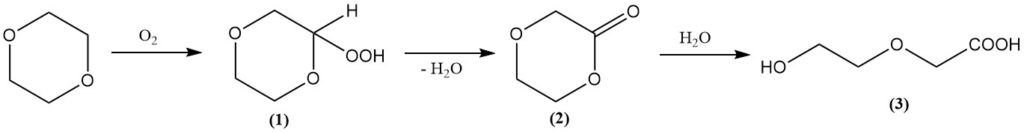
Similmente ad altri eteri, il diossano forma facilmente perossidi se esposto all’aria. Questi perossidi sono spesso altamente esplosivi e instabili. Il perossido primario formato è il 2-idroperossi-1,4-diossano (1), che si decompone per produrre dioxanone (2) e acqua.
La successiva idrolisi porta alla formazione di acido 2-(2-idrossietossi)acetico (3). Fortunatamente, il percorso di reazione favorisce la formazione del prodotto finale, limitando la concentrazione di perossido.
Nonostante ciò, la manipolazione del diossano richiede le stesse precauzioni degli altri eteri per prevenire la formazione di perossidi. Si raccomanda di effettuare il lavaggio con gas inerte, in genere con azoto. Inoltre, i perossidi non devono mai essere concentrati o distillati fino a secchezza.
I metodi consolidati per la loro rimozione prevedono agenti riducenti come cloruri di ferro (II) o stagno (II), bisolfito di sodio o materiali assorbenti come carbone attivo, allumina o resine a scambio anionico.
Il 1,4-diossano è in grado di dissolversi e formare complessi con vari alogeni (Cl2, Br2 e I2) e acidi alogeni. Questi complessi possono moderare la reattività degli alogeni o degli acidi alogenidrici durante le reazioni. Ad esempio, il complesso di diossano dibromuro può essere utilizzato per la bromurazione controllata di fenoli, aldeidi/ammine aromatiche e chetoni.
La clorurazione del diossano può produrre derivati clorurati contenenti da 1 a 8 atomi di cloro. La distribuzione specifica degli isomeri dipende dalle condizioni di reazione (temperatura, catalizzatori) impiegate.
I diossani con meno atomi di cloro vengono utilizzati come precursori per composti di addizione, come gruppi etossilici o etilici, utilizzando reagenti appropriati come NaOCH2CH3 o CH3CH2MgBr, rispettivamente.
Il 2,3-dicloro-1,4-diossano è altamente reattivo, condensandosi facilmente con altri gruppi funzionali come acidi carbossilici, alcoli e glicoli per formare i corrispondenti diesteri ed eteri.
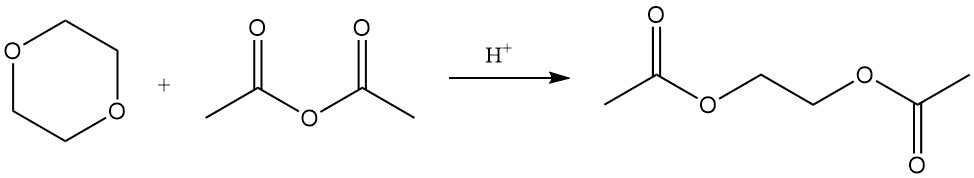
Mentre l’anello diossano è stabile, forte gli acidi a temperatura e pressione elevate possono scinderlo. In tali condizioni, le reazioni con anidride acetica producono diacetato di glicole etilenico e diacetato di glicole dietilene.
Il diossano può essere decomposto dal perossido di idrogeno a 25 °C usando FeSO4 come catalizzatore.
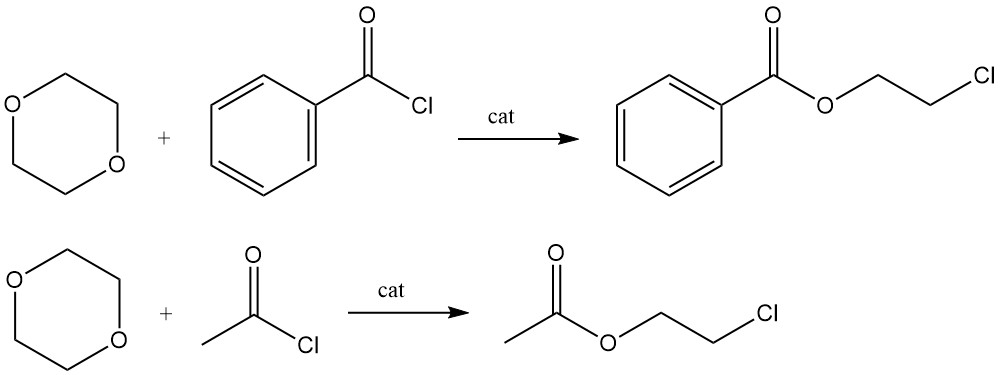
Le reazioni catalizzate dall’acido di Lewis del 1,4-diossano con cloruro di benzoile o cloruro di acetile producono rispettivamente gli esteri 2-cloroetilici dell’acido benzoico e dell’acido acetico.
Utilizzando il perossido di benzoile come catalizzatore, il diossano reagisce con le α-olefine a una temperatura di 80–140 °C per 5–10 ore per produrre una varietà di polimeri utilizzati come lubrificanti.
Reazioni simili possono verificarsi con il tetrafluoroetilene, dove reazioni catalizzate dal perossido ad alte temperature e pressioni producono polimeri analoghi.
Sono stati segnalati numerosi catalizzatori alternativi per queste polimerizzazioni, tra cui perossidi (organici e inorganici), basi (borace, fosfato disodico, idrazina) e acidi di Lewis (cloruro di zinco, acido fosforico).
Oltre agli alogeni, il 1,4-diossano forma complessi con vari gruppi funzionali, come come AlBr3, AlCl3, AuCl3, BBr3, BCl3, BF3, CuCl2, CoCl2, FeCl3, HgCl2, LiBr, LiCl, LiI, ZnCl2, PtCl4, HCl, H2SO4, H3PO4, SO2, SO3 e trinitrofenolo.
Questi complessi sono usati come catalizzatori, agenti moderatori in reazioni come la bromurazione o solfonazione, o come mezzo di reazione per sistemi di acido anidro.
3. Produzione di diossano
Il diossano è prodotto principalmente da un processo a ciclo chiuso che prevede la disidratazione e la successiva chiusura dell’anello del dietilenglicole. L’acido solforico concentrato (circa il 5%) è utilizzato come catalizzatore per questa reazione. Tuttavia, possono essere impiegati anche catalizzatori alternativi come acido fosforico, acido p-toluensolfonico e resine a scambio ionico fortemente acide.
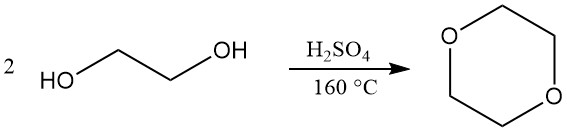
Le condizioni operative per questo processo possono variare. Le temperature di reazione variano in genere da 130 a 200 °C, mentre la pressione può variare da leggermente superiore alla pressione atmosferica a un vuoto parziale (25–110 kPa). Una temperatura di reazione di 160 °C è spesso considerata ottimale.
La configurazione della reazione consente una produzione continua, con il diossano formato vaporizzato direttamente dal recipiente di reazione. Questi vapori vengono quindi fatti passare attraverso una trappola acida e una serie di colonne di distillazione per rimuovere l’acqua e purificare il prodotto finale. Sono ottenibili rese di circa il 90%.
È importante notare che questo processo genera sottoprodotti indesiderati come 2-metil-1,3-diossolano, acetaldeide, crotonaldeide e poliglicole.
Sebbene la disidratazione del dietilenglicole sia la via commerciale dominante, esistono altri metodi per sintetizzare 1,4-diossano. Questi metodi meno comuni includono:
- Deidroalogenazione di 2-cloro-2′-idrossietil etere
- Reazione di glicole etilenico con 1,2-dibromoetano
- Dimerizzazione di ossido di etilene utilizzando catalizzatori come NaHSO4, SiF4 o BF3, o mediante reazioni ad alta temperatura con resine a scambio cationico acide
4. Utilizzi del diossano
L’applicazione industriale più importante del 1,4-diossano è la stabilizzazione del 1,1,1-tricloroetano contro la reazione con l’alluminio. Sulla superficie del metallo si forma una pellicola di ossido di alluminio, impedendo il contatto diretto con il 1,1,1-tricloroetano.
Tuttavia, quando questo strato protettivo viene disturbato, il 1,1,1-tricloroetano reagisce con l’alluminio esposto, estraendo cloro e formando cloruro di alluminio, che quindi promuove la deidroalogenazione del 1,1,1-tricloroetano per produrre acido cloridrico e cloruro di vinilidene.
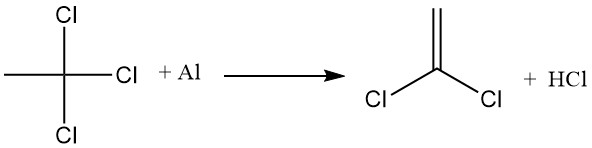
Il 1,4-diossano inibisce queste reazioni formando un complesso insolubile tra diossano e cloruro di alluminio. Questo complesso disattiva il catalizzatore AlCl3 e sigilla tutte le aperture nella pellicola di ossido di alluminio, impedendo il contatto diretto tra il metallo e il 1,1,1-tricloroetano.
Il diossano è impiegato come agente bagnante e disperdente nella lavorazione tessile, nei bagni di tintura, nella colorazione e nelle composizioni di stampa. Inoltre, aiuta nella preparazione di vetrini istologici.
Il diossano è utilizzato in altri settori, tra cui:
- Solventi: è utilizzato come solvente nella formulazione di inchiostri, rivestimenti, adesivi, contatori a scintillazione e per l’estrazione di oli animali e vegetali.
- Intermedio chimico: i prodotti derivati dal diossano sono preziosi come insetticidi, erbicidi, plastificanti e monomeri.
- Catalisi e Reagenti: i complessi di ossonio formati da diossano con sali, acidi minerali, alogeni e triossido di zolfo funzionano come catalizzatori e reagenti in reazioni di acido anidro, bromurazioni e solfonazioni.
- Applicazioni di laboratorio: nei laboratori, il 1,4-diossano è utilizzato come solvente crioscopico per determinare le masse molecolari e la sua stabilità lo rende un mezzo di reazione adatto per varie trasformazioni chimiche.
- Tradizionalmente, il diossano era utilizzato nella produzione di polimeri e come solvente per resine naturali e sintetiche, tra cui derivati della cellulosa, resine polivinilacetaliche e copolimeri acrilonitrile-metil vinil piridina.
5. Tossicologia del diossano
Il diossano ha una tossicità acuta relativamente bassa. I valori LD50 orale e dermico nei ratti e nei conigli, rispettivamente, sono 5170 mg/kg e 7600 mg/kg. L’esposizione per inalazione per 4 ore a 14.260 ppm (51.880 mg/m³) è letale per il 50% della popolazione di ratti esposta (LC50).
Limiti di esposizione professionale:
- Valore limite di soglia dell’American Conference of Governmental Industrial Hygienists (ACGIH) – Media ponderata nel tempo (TLV-TWA): 25 ppm (90 mg/m³) con una notazione “cutanea”.
- Amministrazione per la sicurezza e la salute sul lavoro degli Stati Uniti (OSHA): 100 ppm (360 mg/m³)
- Deutsche Forschungsgemeinschaft (MAK): >50 ppm (180 mg/m³) con notazione IIIB (sospetto cancerogeno)
Misure di controllo dell’esposizione
A causa del potenziale di irritazione della pelle e degli occhi e di danni all’apparato respiratorio ad alte concentrazioni, i luoghi di lavoro che utilizzano 1,4-diossano devono implementare misure di controllo per ridurre al minimo l’esposizione dei lavoratori. Questi includono controlli ingegneristici per ridurre al minimo i livelli di vapore nell’aria e l’uso di dispositivi di protezione individuale come guanti, occhiali protettivi e respiratori, quando necessario.
Carcinogenicità
I primi studi sugli animali che utilizzavano dosi orali elevate di diossano (7-18.000 mg/kg) hanno provocato tumori nasali ed epatici. Tuttavia, studi successivi a dosi inferiori (1.000 mg/kg e inferiori) non hanno mostrato alcuna formazione di tumori, suggerendo un possibile effetto soglia. Inoltre, i test di mutagenicità non hanno rivelato alcuna interazione diretta del diossano con il DNA.
Questi risultati suggeriscono che i tumori nei roditori possono derivare da ripetuti danni ai tessuti piuttosto che da genotossicità diretta.
Metabolismo ed eliminazione
Gli studi che utilizzano diossano radiomarcato indicano che basse dosi vengono rapidamente convertite ed eliminate nelle urine come acido 2-idrossietossiacetico. Questo processo di conversione diventa meno efficiente a dosi elevate, con conseguente eliminazione più lenta.
Esposizioni umane e valutazione del rischio di cancerogenicità
Gli incidenti di esposizione umana a concentrazioni stimate di 470 ppm di diossano hanno causato decessi. Tuttavia, studi epidemiologici su lavoratori esposti a livelli fino a 51 ppm non hanno mostrato effetti negativi sulla salute.
La potenziale cancerogenicità del 1,4-diossano ha spinto vari enti normativi internazionali a stabilire linee guida per la sua presenza nell’acqua potabile e nell’ambiente.
L’Agenzia Internazionale per la Ricerca sul Cancro (IARC) classifica il 1,4-diossano come cancerogeno di Gruppo 2B (probabilmente cancerogeno per l’uomo) sulla base di studi sugli animali che mostrano un’incidenza maggiore di carcinomi della cavità nasale, del fegato e della cistifellea rispettivamente nei ratti, nei topi e nelle cavie.
Linee guida sul diossano nell’acqua potabile
L’Organizzazione Mondiale della Sanità (OMS) raccomanda un valore guida di 50 μg/L per il 1,4-diossano nell’acqua potabile.
L’Agenzia per la Protezione Ambientale degli Stati Uniti (EPA) e il Centro Nazionale per la Valutazione Ambientale hanno proposto un livello di consulenza basato sulla salute di 3 μg/L nell’acqua potabile.
Il Sistema Integrato di Informazioni sui Rischi dell’EPA suggerisce un potenziale rischio di cancro di 1 su 1.000.000 a un’esposizione a vita di 0,35 μg/L. Di conseguenza, la norma sul monitoraggio dei contaminanti non regolamentati (UCMR3) stabilisce un livello minimo di segnalazione di 0,07 μg/L.
L’Agenzia federale tedesca per l’ambiente raccomanda un limite precauzionale di 0,1 μg/L per i cancerogeni non genotossici come il 1,4-diossano nell’acqua potabile.
Il Giappone ha stabilito uno standard ambientale di 50 μg/L per il 1,4-diossano.
Negli Stati Uniti, diversi stati hanno stabilito i propri livelli di consulenza per il 1,4-diossano nell’acqua potabile, riflettendo un mosaico di normative in tutto il paese.
Riferimenti
- Dioxane; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a08_545.pub2
- 1,4-Dioxane; https://onlinelibrary.wiley.com/doi/10.1002/9781119407621.ch4
