4-Nitrofenolo: Proprietà, Produzione e Usi
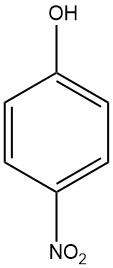
Il 4-nitrofenolo, noto anche come p-nitrofenolo o 4-idrossinitrobenzene, è un composto aromatico con formula chimica C6H5NO3. È un solido cristallino giallo-incolore con un odore dolce e fenolico. È solubile in acqua, etanolo e altri solventi organici.
Sommario
1. Proprietà fisiche del 4-nitrofenolo
Il P-nitrofenolo ha una forma α metastabile che può essere osservata in forma cristallina quando il toluene viene riscaldato a una temperatura superiore a 63 °C. La forma β più stabile si ottiene quando il toluene viene raffreddato a una temperatura inferiore a 63 °C. Il P-nitrofenolo non è facilmente volatile con il vapore, ma è più solubile in acqua rispetto al suo isomero orto.
Alcune delle proprietà fisiche del 4-nitrofenolo sono presentate nella seguente tabella:
| Proprietà | Valore |
|---|---|
| Formula chimica | C6H5NO3 |
| Massa molare | 139,11 g/mol |
| Aspetto | Solido cristallino giallo, aghiforme |
| Punto di fusione | 114 °C |
| Punto di ebollizione | 216 °C |
| Solubilità in acqua (100 °C) | 30% |
| Solubilità in acqua (25 °C) | 16 g/L |
| Densità | 1,48 g/cm³ |
| pKa | 7,15 |
| Punto di infiammabilità | 105 °C |
| Temperatura di decomposizione del sale di sodio | 156 °C |
2. Reazioni chimiche del 4-nitrofenolo
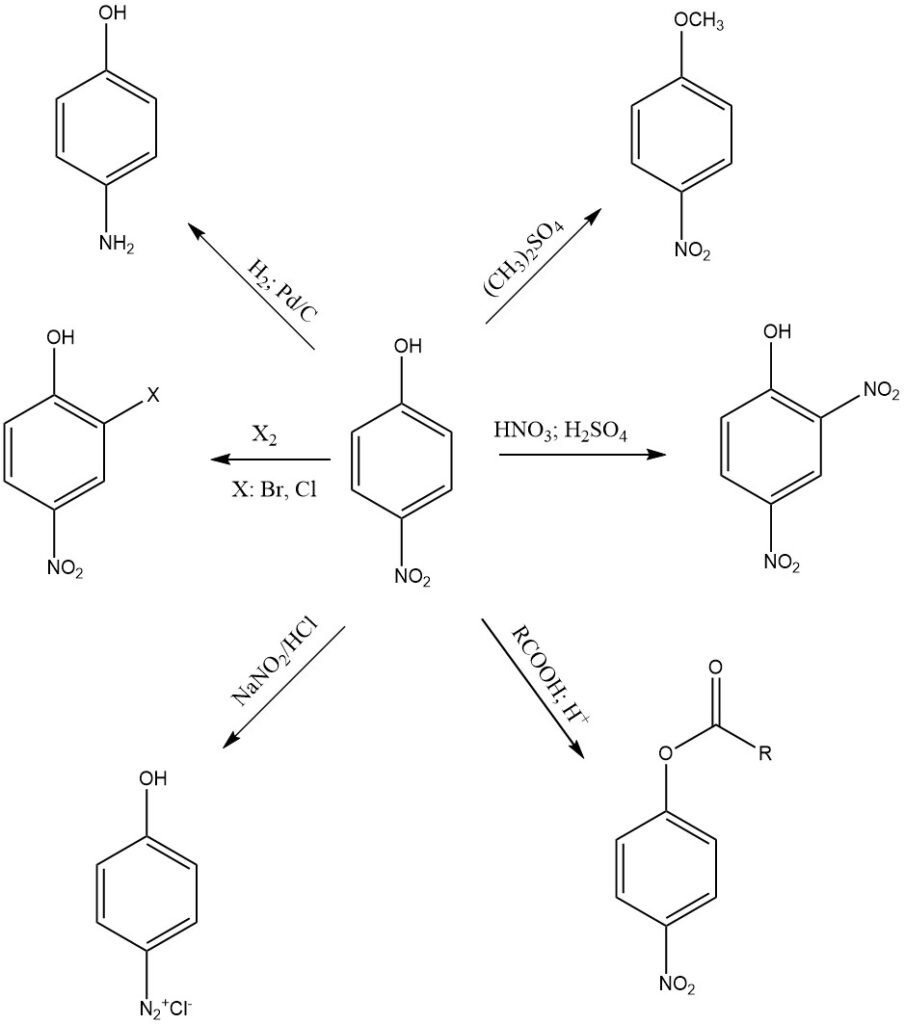
Il 4-nitrofenolo è un composto relativamente stabile. La sua reattività è dovuta alla presenza di gruppi nitro e idrossile sull’anello aromatico, quindi può subire una serie di reazioni chimiche, come segue:
Riduzione
Una delle reazioni più comuni del 4-nitrofenolo è la riduzione del gruppo nitro ad ammina. Il 4-nitrofenolo può essere ridotto a 4-amminofenolo in una serie di condizioni. Gli agenti riducenti comuni includono ditionito di sodio, zinco e ferro in HCl concentrato o gas idrogeno.
Alchilazione
Il 4-nitrofenolo può essere alchilato per formare una serie di derivati. Gli agenti alchilanti comuni includono dimetil solfato e ioduro di metile. I derivati del 4-nitrofenolo alchilati sono spesso usati come intermedi nella sintesi di altri composti organici.
Esterificazione
Il 4-nitrofenolo può subire esterificazione, dove reagisce con acidi carbossilici per formare esteri. Questa reazione è in genere catalizzata da un acido, come l’acido solforico.
Nitrazione
Il 4-nitrofenolo viene nitrato in presenza di acido nitrico e acido solforico per formare 2,4-dinitrofenolo. Un’ulteriore nitrazione produce acido picrico, che è un esplosivo più potente del 2,4-dinitrofenolo, ed è usato in una varietà di applicazioni industriali e militari.
Diazotazione
Il 4-nitrofenolo può anche partecipare alle reazioni di diazotazione, un processo che converte il gruppo amminico (-NH2) del 4-amminofenolo in un sale di diazonio (-N2+X–). Questa reazione è utilizzata nella sintesi di vari coloranti e composti aromatici con gruppi diazoici.
Reazioni acido-base
Il 4-nitrofenolo è acido a causa del suo gruppo idrossilico. Reagisce con basi forti come l’idrossido di sodio per formare ioni 4-nitrofenolato.
Il 4-nitrofenolo subisce anche reazioni dell’anello aromatico come alogenazione, solfonazione, acilazione e alchilazione, in particolare nella posizione orto del gruppo (-OH).
3. Produzione di 4-nitrofenolo
3.1. Idrolisi del 4-cloronitrobenzene
Il 4-cloronitrobenzene viene riscaldato in un’autoclave con una soluzione di idrossido di sodio all’8,5%. La reazione esotermica raggiunge i 170 °C e viene mantenuta per 8 ore. La soluzione viene quindi raffreddata e acidificata per produrre 4-nitrofenolo con una resa del 95%.

Il processo produce 4-nitrofenolo ad alta purezza e comprende i seguenti passaggi:
- Idrolisi basica del 4-cloronitrobenzene
- Concentrazione del mezzo di reazione
- Acidificazione per ottenere il composto 4-nitrofenolo dal suo sale
- Decantazione liquido/liquido per rimuovere la fase acquosa ottenuta dopo l’acidificazione
- Cristallizzazione del composto 4-nitrofenolo
- Separazione del prodotto
La fase di concentrazione rimuove i composti volatili impurità e la fase di decantazione rimuove le impurità solubili in acqua. La fase di cristallizzazione purifica ulteriormente il 4-nitrofenolo rimuovendo eventuali impurità rimanenti.
Questo processo produce un 4-nitrofenolo con un basso contenuto di impurità liposolubili (come il 4-cloronitrobenzene) e impurità solubili in acqua (come il cloruro di sodio e il solfato di sodio). Il 4-nitrofenolo è inoltre privo di impurità solforose, il che è vantaggioso per le successive reazioni di idrogenazione catalitica.
3.2. Nitrazione del fenolo
Il fenolo viene fatto reagire con acido nitrico in presenza di acido solforico per produrre una miscela di 2-nitrofenolo e 4-nitrofenolo. La miscela viene quindi distillata per separare i due isomeri. Il 4-nitrofenolo ottenuto dalla fase di distillazione viene ulteriormente purificato mediante cristallizzazione o ricristallizzazione.

Un processo più efficiente per produrre 4-nitrofenolo dal fenolo in un mezzo di acido nitrico è un metodo che prevede due fasi: nitrosazione e nitrazione. Nella fase di nitrosazione, il fenolo viene fatto reagire con acido nitroso per produrre p-nitrosofenolo.
Nella fase di nitrazione, il p-nitrosofenolo viene fatto reagire con acido nitrico per produrre 4-nitrofenolo. Il processo viene eseguito in un mezzo di acido nitrico con una concentrazione compresa tra il 5 e il 30% in peso e la temperatura viene mantenuta tra 0 e 10 °C durante la nitrosazione e tra 15 e 30 °C durante la nitrazione.
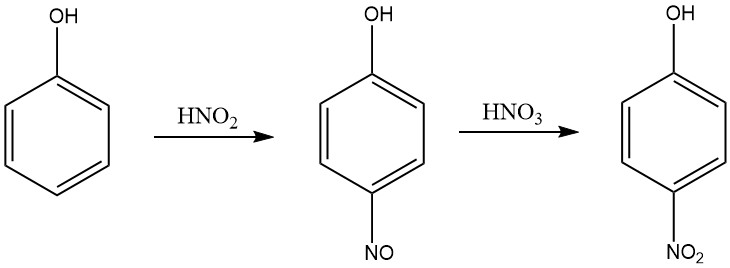
L’acido nitroso viene prodotto nell’acido nitrico acquoso mediante aggiunta di ossidi di azoto, come ossido nitrico, tetrossido di azoto o triossido di azoto. Il 4-nitrofenolo viene separato dalla miscela di reazione mediante cristallizzazione.
Questo processo è vantaggioso perché produce 4-nitrofenolo con un basso contenuto di isomeri orto.
4. Usi del 4-nitrofenolo
La riduzione del 4-nitrofenolo a 4-amminofenolo è meno utilizzata perché i processi per ridurre direttamente il nitrobenzene sono più comuni.
Il 4-nitrofenolo reagisce con i cloruri dialchiltiofosforici a 125 °C nel clorobenzene per formare un gruppo di insetticidi tra cui il paration. Ma questo composto è stato sostituito da alternative meno tossiche come il metilparathion e sostanze correlate.
Il 4-nitrofenolo reagisce con il 4-cloro-3-nitrobenzotrifluoruro per formare il fluorodifen, che è correlato al nitrofen. Questo erbicida è usato per trattare le colture di riso seminate.
Il 4-nitrofenolo è utilizzato in altre applicazioni, tra cui:
- Prodotti farmaceutici: il 4-nitrofenolo è utilizzato come intermedio nella sintesi del paracetamolo (noto anche come acetaminofene), un comune antidolorifico da banco e antipiretico.
- Fungicidi: il 4-nitrofenolo è un precursore di alcuni fungicidi, come dinocap e binapacryl.
- Coloranti: il 4-nitrofenolo è utilizzato per produrre una varietà di coloranti, tra cui coloranti gialli, arancioni e rossi.
- Concia della pelle: il 4-nitrofenolo viene utilizzato per scurire la pelle.
5. Tossicologia del 4-nitrofenolo
| Esposizione | LD50 |
|---|---|
| Cutanea, cavia | >1 gm/kg |
| Orale, topo | 282 mg/kg |
| Orale, ratto | 202 mg/kg |
| Pelle, ratto | 1024 mg/kg |
| Inalazione, ratto | > 4,7 mg/l/4H |
| Sensibilizzazione cutanea, cavia | Nessuno sensibilizzato |
- Effetti acuti: L’inalazione o l’ingestione di 4-nitrofenolo può causare mal di testa, sonnolenza, nausea e cianosi (colorazione bluastra di labbra, orecchie e unghie). Il contatto con gli occhi può causare irritazione.
- Effetti cronici: Non sono disponibili informazioni sugli effetti cronici del 4-nitrofenolo negli esseri umani o negli animali derivanti da inalazione o esposizione orale.
- Effetti riproduttivi/sviluppativi: Non sono disponibili informazioni sugli effetti riproduttivi o sullo sviluppo del 4-nitrofenolo negli esseri umani.
- Rischio di cancro: Non sono disponibili informazioni sugli effetti cancerogeni del 4-nitrofenolo negli esseri umani. Non vi è stata alcuna prova di attività cancerogena nei topi esposti per via cutanea al 4-nitrofenolo per 18 mesi in uno studio del National Toxicology Program (NTP).
Riferimenti
- Nitro Compounds, Aromatic, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a17_411
- Process for preparation of a nitrophenol. – https://patents.google.com/patent/US20080045756A1/en
- Preparation of p-nitrophenols. – https://patents.google.com/patent/US3510527A/en
- https://www.epa.gov/sites/default/files/2016-09/documents/4-nitrophenol.pdf
- https://fscimage.fishersci.com/msds/96371.htm
