Ciclohexilamina: propiedades, reacciones, producción y usos
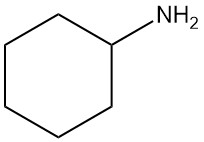
¿Qué es la ciclohexilamina?
La ciclohexilamina, también conocida como aminociclohexano, es una amina primaria alifática con la fórmula química C6H13N. Es un líquido incoloro miscible con agua y disolventes orgánicos comunes.
Tabla de contenido
1. Propiedades físicas de la ciclohexilamina
La ciclohexilamina es un líquido incoloro con olor a amoníaco o a pescado, muy soluble en etanol, éter, acetona y disolventes orgánicos comunes. Forma un azeótropo con agua que hierve a 96,4 °C y contiene un 44,2 % de ciclohexilamina.
Las propiedades físicas de la ciclohexilamina se enumeran en la siguiente tabla:
| Propiedad | Valor |
|---|---|
| Número CAS | [108-91-8] |
| Fórmula química | C6H13N |
| Peso molecular | 99,18 g/mol |
| Punto de fusión | -17,8 °C |
| Punto de ebullición | 134,5 °C |
| Densidad | 0,8647 g/cm3 |
| Índice de refracción | 1,4592 |
| Viscosidad a 20 °C | 2,10 Pa·s |
| pKa | 10,63 |
| Densidad de vapor | 3,42 |
| Presión de vapor | 1,4 kPa a 20 °C |
| Capacidad calorífica específica a 20 °C | 2,366 J g-1K-1 |
| Calor de vaporización | 399,86 J/g |
| Punto de inflamación (vasos cerrados) | 26,5 °C |
| Temperatura de ignición | 265 °C |
| Rango de ignición en el aire | 1,6–9,4 vol% |
2. Reacciones químicas de la ciclohexilamina
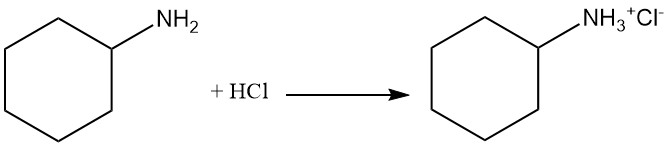
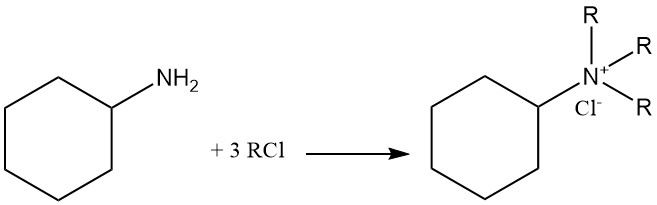
La ciclohexilamina es una base débil con un pKb de 3,4 que tiene una reactividad similar a la de las aminas alifáticas primarias. Forma sales con ácidos de Brønsted y Lewis. La alquilación exhaustiva conduce a la formación de un catión amonio cuaternario.
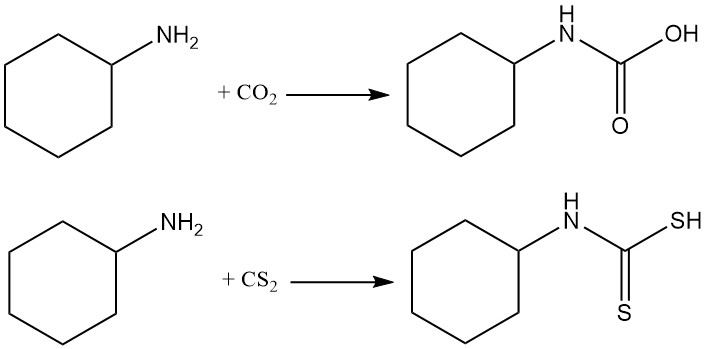
La ciclohexilamina reacciona con dióxido de carbono y disulfuro de carbono para producir carbamatos y tiocarbamatos, respectivamente.
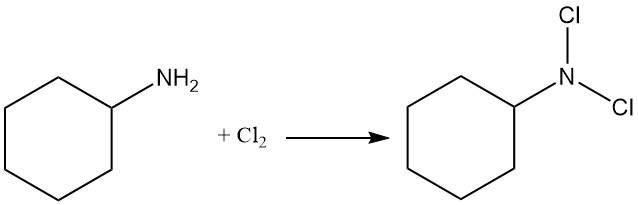
La reacción de ciclohexilamina con cloro produce N,N-diclorociclohexilamina.
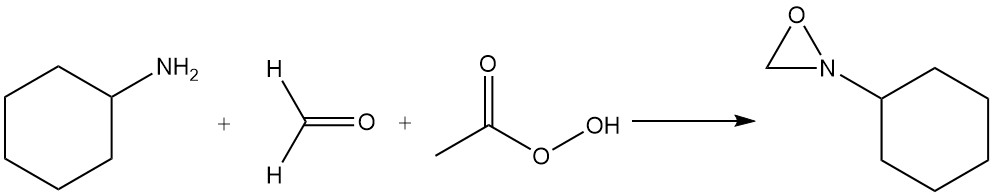
La 2-ciclohexiloxaziridina se prepara haciendo reaccionar una mezcla de ciclohexilamina, formaldehído y ácido peracético.
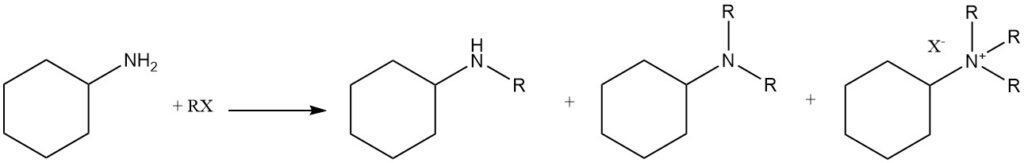
La N-alquilación de ciclohexilamina se puede lograr utilizando diversos agentes alquilantes, incluidos haluros de alquilo, sulfatos y fosfatos. Alternativamente, se pueden utilizar alcoholes como compuestos alquilantes en presencia de metales catalíticos (aluminio, cobre, níquel, cobalto o platino) o en condiciones de Leuckart-Wallach.
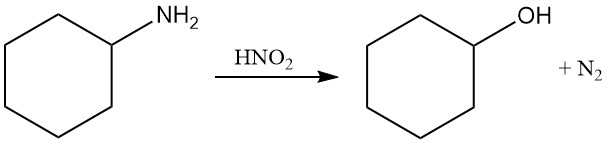
La ciclohexilamina sufre diazotación con ácido nitroso para formar gas nitrógeno y ciclohexanol.
Los cloruros de ácido reaccionan con ciclohexilamina en condiciones de Schotten-Baumann para formar ciclohexilamidas.
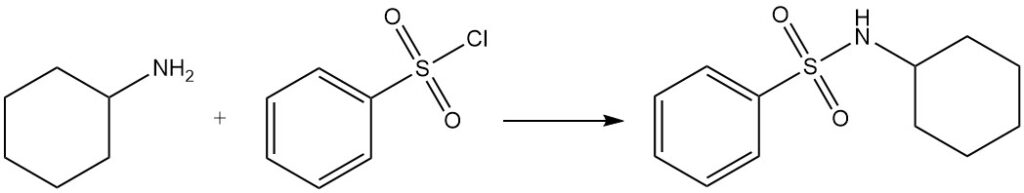
El cloruro de bencenosulfonilo reacciona con ciclohexilamina para producir N-ciclohexilbencenosulfonamida, que es soluble en soluciones alcalinas (prueba de Hinsberg).
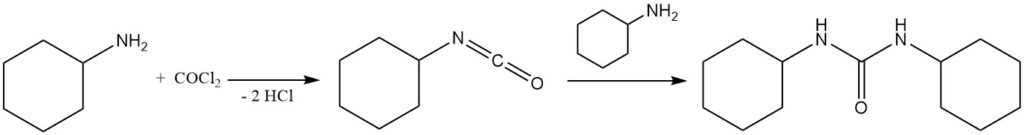
El fosgeno reacciona con ciclohexilamina para formar isocianatociclohexano, que a su vez reacciona con ciclohexilamina para formar 1,3-diciclohexilurea.
Debido al carácter nucleofílico de la ciclohexilamina, reacciona con epóxidos para producir derivados de hidroxialquilamina y dihidroxialquilamina.
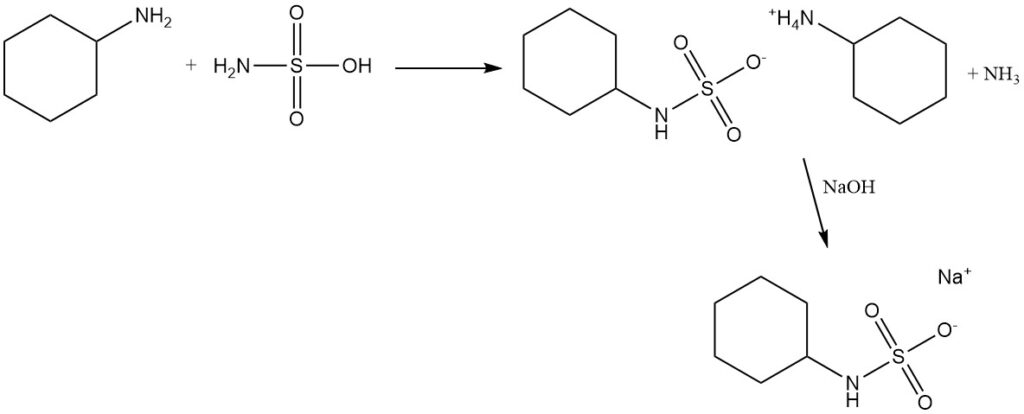
La ciclohexilamina de alta pureza reacciona con ácido sulfámico, seguido de un tratamiento con hidróxido de sodio o hidróxido de calcio, para formar ciclohexilsulfamato de sodio o ciclohexilsulfamato de calcio, que son edulcorantes artificiales utilizados en el pasado.
La reacción de condensación de ciclohexilamina con mercaptobenzotiazol produce N-ciclohexil-2-benzotiazolesulfenamida, que se utiliza como acelerador de caucho moderado.
3. Producción industrial de ciclohexilamina
La ciclohexilamina se produce comercialmente mediante la reacción de ciclohexanol con amoníaco e hidrógeno en fase de vapor utilizando catalizadores metálicos como Ni o Co.
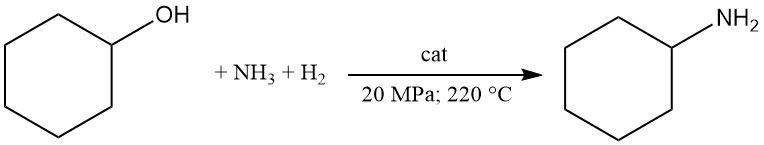
En este proceso, el ciclohexanol reacciona a 20 MPa y 220 °C con al menos 3 moles de amoníaco en presencia de hidrógeno circulante sobre un catalizador de lecho fijo.
Una mayor proporción de alimentación de amoníaco a ciclohexanol favorece la formación de ciclohexilamina y reduce la formación del subproducto diciclohexilamina.
La aminación reductora de ciclohexanona mediante un proceso continuo es otro método para producir ciclohexilamina. En este proceso, el hidrógeno y el amoníaco presurizados reaccionan con la ciclohexanona sobre catalizadores de níquel o cobalto a 0,1–20 MPa y altas temperaturas de hasta 275 °C.

Se ha afirmado que la relación amoniaco-ciclohexanona es de 3,3:1 y la relación hidrógeno-ciclohexanona de 6,5:1.
La ciclohexilamina se produce mediante hidrogenación en fase líquida de anilina sobre un catalizador de cobalto-alúmina a 25 MPa y 140 °C con un rendimiento del 80 %. Sin embargo, la hidrogenación en fase de vapor sobre níquel sobre piedra pómez favorece la formación de diciclohexilamina.
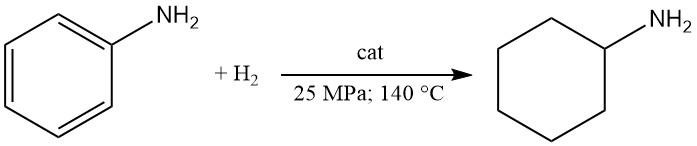
La elección de los catalizadores y las condiciones de reacción influyen en la selectividad de la reacción para la ciclohexilamina. Por ejemplo, si se hidrogena anilina a 160-200 °C en presencia de un catalizador de rutenio-paladio soportado sobre γ-alúmina, la mezcla de productos finales contiene solo un 19,3 % de ciclohexilamina y un 80,3 % de diciclohexilamina.
Se logra una alta selectividad para la ciclohexilamina añadiendo amoníaco durante la hidrogenación de anilina a 160-180 °C y 2-5 MPa utilizando un catalizador de rutenio sobre carbono.
La ciclohexilamina también se fabrica a escala comercial mediante la hidrogenación de nitrobenceno sin separación intermedia de anilina.
Se ha explorado la síntesis directa de ciclohexilamina a partir de fenol utilizando catalizadores de rodio o níquel, pero con una menor selectividad hacia la ciclohexilamina en comparación con la diciclohexilamina.
La ciclohexilamina se purifica a partir de subproductos mediante destilación a presión reducida.
4. Usos de la ciclohexilamina
La ciclohexilamina es un compuesto miscible en agua que forma un azeótropo con el agua. Se utiliza como inhibidor de la corrosión en sistemas de vapor de baja presión porque forma una película protectora y es un agente neutralizador de ácidos.
En 2000, aproximadamente el 55% de la producción de ciclohexilamina de EE. UU. se dedicó a esta aplicación. En comparación con la morfolina, la ciclohexilamina ofrece una estabilidad química superior en entornos de alta presión y no forma nitrosamina.
Se utiliza como inhibidor de la corrosión para soluciones de alcohol para radiadores y también en las industrias del papel y del revestimiento de metales para la protección contra la humedad y la oxidación.
Más allá de la inhibición de la corrosión, la ciclohexilamina se utiliza como acelerador de la vulcanización, aditivo anticorrosivo y precursor de varios compuestos, incluidos plastificantes, emulsionantes, coagulantes y endurecedores epóxicos.
Sus sales con ácidos grasos evitan la formación de espuma en los aceites minerales. La ciclohexilamina también se utiliza como terminador de cadena en la polimerización de poliamidas y como precursor de herbicidas como la hexazinona. También funciona como endurecedor de resinas epoxi y como catalizador de poliuretanos.
Históricamente, la ciclohexilamina se utilizaba en la producción de edulcorantes de ciclamato.
Los principales productores de ciclohexilamina incluyen US Amines, Air Products, BASF, Borsodchem, Jintian Enterprises y New Japan Chemical Co.
5. Toxicología de la ciclohexilamina
La ciclohexilamina es un líquido alcalino que se absorbe fácilmente por vía oral y respiratoria, aunque la absorción dérmica es más lenta. Se produce una excreción urinaria rápida con una alteración metabólica mínima. El compuesto posee un fuerte olor a pescado con un umbral de olor de alrededor de 2,5 ml/m³.
La exposición humana a la ciclohexilamina puede inducir efectos simpaticomiméticos en dosis diarias de 5 mg/kg. Se han realizado estudios toxicológicos exhaustivos debido a su asociación con el edulcorante sacarina.
Los estudios de alimentación a largo plazo en roedores no revelaron efectos carcinógenos, mutagénicos o teratogénicos en dosis de hasta aproximadamente 20 mg/kg por día. Los estudios de fertilidad en ratas no mostraron efectos adversos, a pesar de una atrofia testicular menor en dosis más altas.
Se han establecido límites de exposición ocupacional para proteger la salud humana. Un estudio de inhalación de 4 horas en humanos mostró irritación a 10 mL/m³, mientras que una concentración promedio ponderada en el tiempo de 2 mL/m³ fue bien tolerada.
En consecuencia, la concentración máxima en el lugar de trabajo (valor MAK) se estableció en 2 mL/m³ con una categoría de limitación máxima de I.
Los estudios de toxicidad aguda en animales indican una DL50 oral de 710 mg/kg en ratas y una DL50 dérmica de 320 mg/kg en conejos.
Referencias
- Amines, Aliphatic, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_001.pub2
- Amines, Cycloaliphatic. – https://onlinelibrary.wiley.com/doi/10.1002/0471238961.0325031203011905.a01.pub2
- Aniline and Its Derivatives. – https://onlinelibrary.wiley.com/doi/10.1002/0471238961.0114091201130914.a01.pub2
- Cyclohexylamine [MAK Value Documentation, 2017]. – https://onlinelibrary.wiley.com/doi/10.1002/3527600418.mb10891e6218
