Herstellung von Nitrobenzoesäuren
Inhaltsverzeichnis
2-Nitrobenzoesäure oder o-Nitrobenzoesäure

2-Nitrobenzoesäure ist Mononitrobenzoesäure, bei der sich die Nitrogruppe in ortho-Stellung zur Carboxylgruppe befindet. Es ist ein Feststoff, der in Wasser unlöslich und in Alkohol wie Methanol löslich ist.
Physikalische Eigenschaften von 2-Nitrobenzoesäure
Die physikalischen Eigenschaften der 2-Nitrobenzoesäure sind nachstehend aufgeführt:
- Molmasse = 167,12 g/mol
- Schmelzpunkt = 148 °C
- Dichte = 1,575
- Löslichkeit in Wasser = 0,75 g/100 ml (bei 25 °C)
- Löslichkeit in Methanol = 42,72 g/100 ml (bei 10 °C)
- Löslichkeit in Benzol = 0,294 g/100 ml (bei 10 °C)
- Dissoziationskonstante Ka (bei 18 °C) = 6,1 × 10-3
- Decarboxylierungstemperatur = 180 °C
Chemische Reaktionen von 2-Nitrobenzoesäure
2-Nitrobenzoesäure unterliegt der typischen Reaktion aromatischer Carbonsäuren und nitroaromatischer Verbindungen:
Anthranilsäure kann durch Reduktion der Nitrogruppe zu einem Amin hergestellt werden.
Die Carboxylgruppe bildet Ester mit Alkoholen und 2-Nitrobenzoylchlorid mit Chlorierungsmitteln.
Bei Temperaturen über 180 °C bildet 2-Nitrobenzoesäure durch Decarboxylierung Nitrobenzo.
Der aromatische Ring kann Substitutionsreaktionen eingehen, dies ist jedoch aufgrund des Vorhandenseins desaktivierender Gruppen schwierig.
Herstellung von 2-Nitrobenzoesäure
2-Nitrobenzoesäure wird durch Oxidation von 2-Nitrotoluol mit Salpetersäure hergestellt.

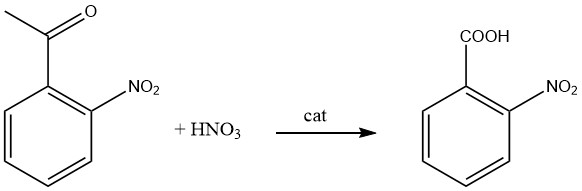
Monsanto Chemicals Ltd. hatte eine Produktionsmethode für 2-Nitrobenzoesäure durch Oxidation von 2-Nitroacetphenon mit wässriger Salpetersäure in Gegenwart von Ammoniummetavanadat als Katalysator unter Rückfluss entwickelt.
Um ein Mol 2-Nitroacetophenon bei einer Temperatur von 60 °C auf die Rückflusstemperatur der Mischung umzuwandeln, sind acht Mol Salpetersäure erforderlich.
Durch Abkühlen der Reaktionsmischung bilden sich die rohen 2-Nitrobenzoesäurekristalle, die daraus durch Filtration gewonnen und anschließend durch Umkristallisation aus Lösungsmitteln wie Benzol, Ethanol, Benzol-Ethanol-Mischungen, Hexan usw. gereinigt werden.
3-Nitrobenzoesäure oder m-Nitrobenzoesäure

3-Nitrobenzoesäure ist ein weißer Feststoff. Die Carbonsäure- und Nitrosubstituenten stehen in Metastellung zueinander, weshalb sie auch m-Nitrobenzoesäure genannt wird. Es ist ein wichtiger Vorläufer bei der Herstellung von Farbstoffen.
Physikalische Eigenschaften von 3-Nitrobenzoesäure
Die physikalischen Eigenschaften der 3-Nitrobenzoesäure sind nachstehend aufgeführt:
- Molmasse = 167,12 g/mol
- Schmelzpunkt = 142 °C
- Dichte = 1,494
- Löslichkeit in Wasser = 0,24 g/100 ml (bei 15 °C)
- Löslichkeit in Methanol = 47,34 g/100 ml (bei 10 °C)
- Löslichkeit in Benzol = 0,795 g/100 ml (bei 10 °C)
- Dissoziationskonstante Ka (bei 25 °C) = 3,48 × 10-4
- Decarboxylierungstemperatur = 238 °C
Chemische Reaktionen von 3-Nitrobenzoesäure
3-Nitrobenzoesäure unterliegt der typischen Reaktion aromatischer Carbonsäuren und nitroaromatischer Verbindungen:
3-Aminobenzoesäure kann durch Reduktion der Nitrogruppe zu einem Amin hergestellt werden.
Die Carboxylgruppe bildet Ester mit Alkoholen und 3-Nitrobenzoylchlorid mit Chlorierungsmitteln.
Bei Temperaturen über 238 °C bildet 3-Nitrobenzoesäure durch Decarboxylierung Nitrobenzoe.
Der aromatische Ring kann Substitutionsreaktionen eingehen, dies ist jedoch aufgrund des Vorhandenseins desaktivierender Gruppen schwierig.
Herstellung von 3-Nitrobenzoesäure
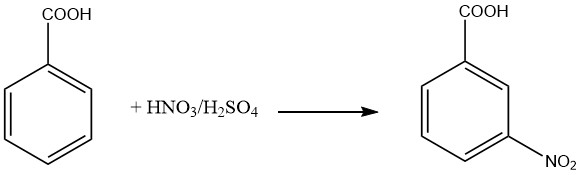
Die 3-Nitrobenzoesäure wird durch Nitrierung von Benzoesäure unter Niedrigtemperaturbedingungen hergestellt. Dabei entstehen neben der gewünschten 3-Nitrobenzoesäure etwa 20 % des 2-Nitro-Isomers und 1,5 % des 4-Nitro-Isomers. Um gereinigte 3-Nitrobenzoesäure zu erhalten, kann eine Umkristallisation des Natriumsalzes eingesetzt werden.
Durch die kontrollierte Oxidation von Benzaldehyd kann eine höhere Ausbeute an 3-Nitrobenzaldehyd, einem Vorläufer von 3-Nitrobenzoesäure, erzielt werden. 3-Nitrobenzoesäure dient als Zwischenprodukt bei der Synthese von 3-Aminobenzoesäure und Azofarbstoffen. Sein Derivat, die 4-Chlor-3-nitrobenzoesäure, fungiert als Zwischenprodukt bei der Herstellung von Farbstoffen.
4-Nitrobenzoesäure oder p-Nitrobenzoesäure
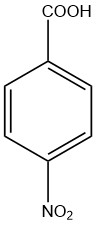
4-Nitrobenzoesäure ist eine Mononitrobenzoesäure, bei der sich die beiden Gruppen in para-Stellung zueinander befinden. Sie wird auch Parra-Nitrobenzoesäure genannt. Es ist ein hellgelber Feststoff, der in Wasser unlöslich und in Methanol schwer löslich ist.
Physikalische Eigenschaften von 4-Nitrobenzoesäure
Die physikalischen Eigenschaften der 4-Nitrobenzoesäure sind folgende:
- Molmasse = 167,12 g/mol
- Schmelzpunkt = 240 °C
- Dichte = 1,61
- Löslichkeit in Wasser = 0,02 g/100 ml (bei 15 °C)
- Löslichkeit in Methanol = 9,6 g/100 ml (bei 10 °C)
- Löslichkeit in Benzol = 0,017 g/100 ml (bei 12,5 °C)
- Dissoziationskonstante Ka (bei 25 °C) = 3,93 × 10-4
- Decarboxylierungstemperatur > 240 °C
Chemische Reaktionen von 4-Nitrobenzoesäure
4-Nitrobenzoesäure unterliegt der typischen Reaktion aromatischer Carbonsäuren und nitroaromatischer Verbindungen:
4-Aminobenzoesäure kann durch Reduktion der Nitrogruppe zu einem Amin hergestellt werden.
Die Carboxylgruppe bildet Ester mit Alkoholen und 4-Nitrobenzoylchlorid mit Chlorierungsmitteln, das ein Ausgangsmaterial für Procainhydrochlorid und Folsäure ist.
Bei Temperaturen über 240 °C bildet 4-Nitrobenzoesäure durch Decarboxylierung Nitrobenzoe.
Der aromatische Ring kann Substitutionsreaktionen eingehen, dies ist jedoch aufgrund des Vorhandenseins desaktivierender Gruppen schwierig.
Herstellung von 4-Nitrobenzoesäure
4-Nitrobenzoesäure wird kommerziell durch Oxidation von 4-Nitrotoluol mit molekularem Sauerstoff hergestellt. Durch Oxidation mit 15 %iger Salpetersäure bei 175 °C entsteht die Säure in einer Ausbeute von 88,5 %.

Monsanto Chemicals Ltd. hatte eine Produktionsmethode für 4-Nitrobenzoesäure durch Oxidation von 4-Nitroacetphenon mit wässriger Salpetersäure in Gegenwart von Ammoniummetavanadat als Katalysator unter Rückfluss entwickelt.
Um ein Mol 4-Nitroacetophenon bei einer Temperatur von 60 °C auf die Rückflusstemperatur der Mischung umzuwandeln, sind acht Mol Salpetersäure erforderlich.
Durch Abkühlen der Reaktionsmischung bilden sich die rohen 4-Nitrobenzoesäurekristalle, die daraus durch Filtration gewonnen und dann durch Umkristallisation aus Lösungsmitteln wie Benzol, Ethanol, Benzol-Ethanol-Mischungen, Hexan usw. gereinigt werden.

Eine interessante Methode ist die Nitrierung und anschließende Oxidation von Polystyrol. Diese Methode nutzt die sterische Hinderung der Polymerkette, um das para-zu-ortho-Verhältnis des Produkts zu verbessern.
Verweise
- Benzoic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a03_555
Preparation of 2-and 4-nitrobenzoic acid. – https://patents.google.com/patent/US2695311A/en
