Fumarsäure: Eigenschaften, Herstellung und Verwendung
Was ist Fumarsäure?
Fumarsäure, auch bekannt als Trans-Butendisäure, ist eine Dicarbonsäure mit der Formel C4H4O4. Sie ist in der Natur weit verbreitet und erscheint als weißer, kristalliner Feststoff mit fruchtartigem Geschmack.
Fumarsäure wurde erstmals 1832 von Winckler aus Erdrauch (Fumaria officinalis) isoliert. Sie wurde später unter verschiedenen Namen identifiziert, darunter Boletinsäure, Glauciniumsäure, Flechtensäure und Paramaleinsäure.
Fumarsäure wird heute industriell hergestellt, ist jedoch im Vergleich zu Maleinsäureanhydrid weniger wichtig.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Fumarsäure
Fumarsäure kristallisiert in Form monokliner Prismen. Sie ist löslich in Ethanol und konzentrierter Schwefelsäure, schwach löslich in Ethylether und Aceton und unlöslich in Chloroform und Benzol. Eine 0,05%ige wässrige Lösung von Fumarsäure bei 25 °C hat einen pH-Wert von 3,0-3,2.
Die wichtigen physikalischen Eigenschaften von Fumarsäure sind in der folgenden Tabelle zusammengefasst.
| Eigenschaft | Wert |
|---|---|
| CAS-Nummer | [110-17-8] |
| Chemische Formel | C4H4O4 |
| Molekulargewicht | 116,07 g/mol |
| Schmelzpunkt | 286–287 °C (geschlossen Röhrchen) |
| Sublimationstemperatur | 200 °C |
| Dichte (fest) | 1,635 g/cm3 |
| Sublimationswärme (92 °C) | 136,1 kJ/mol |
| pKa1 | 3,02 |
| pKa2 | 4,38 |
| Löslichkeit in 100 g Wasser | 0,428 g (bei 15,5 °C) |
| 9,97 g (bei 100 °C) | |
| Flammpunkt | 273 °C (offener Tiegel) 230 °C (geschlossener Tiegel) |
| Selbstentzündungstemperatur | 375 °C (Pulver) |
2. Chemische Eigenschaften von Fumarsäure
Fumarsäure sublimiert bei oder knapp über 200 °C ohne Zersetzung, aber bei Erhitzung über 230 °C zersetzt sie sich und bildet Maleinsäureanhydrid, Wasser und eine beträchtliche Menge an Rückständen. Die Anwesenheit von Phosphorpentoxid katalysiert die Bildung von Maleinsäureanhydrid.
Fumarsäure ist das Transisomer von Maleinsäure und hat viele chemische Eigenschaften mit ihr gemeinsam. Allerdings verlaufen Reaktionen bei Fumarsäure im Allgemeinen langsam, was teilweise auf ihre geringere Wasserlöslichkeit zurückzuführen ist.
Im Gegensatz zu Maleinsäure kann Fumarsäure ein Säurechlorid bilden. (Weitere Einzelheiten zu den Reaktionen finden Sie im Artikel über Maleinsäure.)
3. Herstellung von Fumarsäure
Fumarsäure wird hauptsächlich durch Isomerisierung von Maleinsäure oder Maleinsäureanhydrid hergestellt (Abbildung 1). Diese Ausgangsstoffe stammen häufig aus Waschwasserströmen, die bei der Herstellung von Maleinsäureanhydrid oder Phthalsäureanhydrid entstehen, mit einer bevorzugten Mindestmaleinsäurekonzentration von 30 %.
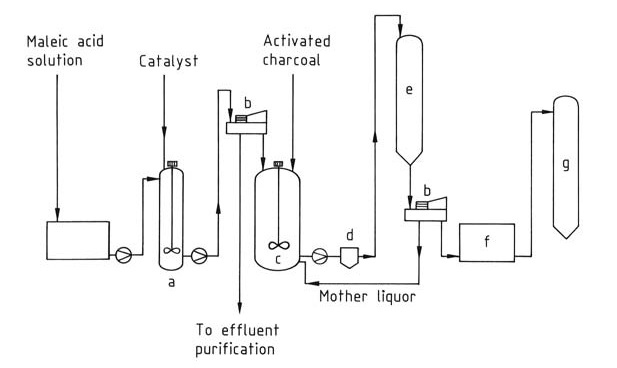
a) Isomerisierungsbehälter; b) Zentrifuge; c) Lösebehälter; d) Filter; e) Kristallisator; f) Trockner; g) Silo
Der Isomerisierungsprozess wandelt Maleinsäure nahezu quantitativ in die weniger lösliche Fumarsäure um, die dann durch Filtration abgetrennt wird. Diese Umwandlung kann durch Wärmebehandlung oder mithilfe von Katalysatoren erreicht werden. Es wurden mehrere Katalysatoren untersucht, darunter:
- Mineralsäuren (z. B. Salzsäure)
- Schwefelbasierte Verbindungen wie Thiocyanate, Thiazole, Thiosemicarbazide und Thioharnstoffe
- Bromverbindungen kombiniert mit Peroxiden (z. B. Persulfat)
Unter diesen ist Thioharnstoff der in der Industrie am häufigsten verwendete Katalysator.
Das Waschwasser aus dem Ausgangsmaterial kann Verunreinigungen enthalten, die die Produktqualität und den Ertrag beeinträchtigen. Dieses Problem kann vermieden werden, indem das Waschwasser thermisch vorbehandelt wird, Harnstoff neben Thioharnstoff als Katalysator zugegeben wird oder Sulfite oder Schwefeldioxidgas und anschließend Mineralsäuren zugegeben werden.
Die gewonnene Rohfumarsäure wird durch Umkristallisation aus Wasser und Behandlung mit Aktivkohle gereinigt. Diese Reinigungsprozesse führen zu einem Produktverlust von etwa 10 %.
Die Produktion von Fumarsäure erfolgt normalerweise chargenweise, obwohl es auch kontinuierliche Prozesse gibt. Es wird empfohlen, korrosionsbeständige Geräte aus austenitischem Stahl zu wählen, insbesondere wenn im Prozess keine Salzsäure verwendet wird.
Die Entsorgung der übrig gebliebenen Mutterlauge aus der Isomerisierungsstufe stellt aufgrund der Anwesenheit löslicher Verunreinigungen und des verbrauchten Katalysators eine Herausforderung dar. Die Verbrennung ist eine mögliche Lösung für diesen Abfallstrom.
Eine alternative Produktionsmethode, die in den USA angewendet wird, verwendet die Fermentation von Monosacchariden oder Stärke mit bestimmten Pilzstämmen wie Mucor, Aspergillus und Rhizopus.
4. Verwendung von Fumarsäure
Fumarsäure ist ein gängiger Lebensmittelzusatzstoff (E297), der als Säuerungsmittel oder Säuerungsmittel verwendet wird, um den Geschmack von Produkten wie Getränken, Backwaren (insbesondere Roggen- und Sauerteigbrot) und Füllungen zu verbessern. Darüber hinaus wirkt es als Konservierungsmittel, indem es die Haltbarkeit von Produkten wie Weizentortillas verlängert.
Fumarsäure wurde in oralen Medikamenten verwendet und wird auf ihre potenzielle Rolle bei der Behandlung von Psoriasis untersucht.
Sie wird als Zwischenprodukt bei der Herstellung verschiedener Chemikalien und in Kosmetika (z. B. Badesalzen und Zahnprothesenreinigern) verwendet.
Fumarsäure wird häufig gegenüber Maleinsäure zur Herstellung von Polyestern und Copolymeren bevorzugt. Während des Herstellungsprozesses dieser Produkte führt die Isomerisierung zu einer nahezu gleichmäßigen Mischung aus trans- und cis-Isomeren der Dicarbonsäuren, unabhängig vom Ausgangsmaterial (Maleinsäure oder Fumarsäure).
Fumarsäure wird jedoch aufgrund ihres Sicherheitsprofils (unschädliche Natur) bevorzugt. In einigen Fällen kann die Verwendung von Fumarsäure zu bestimmten Effekten führen, wie z. B. einer erhöhten Härte bestimmter Harze.
Fumarsäure (Fumaril) und Eisen(II)-fumarat werden als spezielle Zusatzstoffe in Tierfutter verwendet.
5. Toxikologie von Fumarsäure
Fumarsäure ist ein natürlich vorkommendes Produkt mit einem günstigen Sicherheitsprofil (nicht toxisch), basierend auf verschiedenen Studien.
Tierstudien weisen auf eine geringe akute Toxizität hin. Die oralen LD50-Werte bei Ratten übersteigen 10 g/kg Körpergewicht, und die dermale Anwendung bei Kaninchen bis zu 20 g/kg war nicht tödlich.
Die langfristige Verabreichung von Fumarsäure in einer Dosierung von 8 mg/kg Körpergewicht pro Tag über ein Jahr beim Menschen verursachte keine Veränderungen in Blut, Urin oder Leberfunktion.
In Experimenten wurden keine Hinweise auf genotoxische Effekte (DNA-Schäden), Karzinogenität (krebserregend) oder Reproduktionstoxizität beobachtet.
Fumarsäure kann jedoch lokal reizend wirken. Sie wird als leicht reizend für die Haut und mäßig reizend für die Augen und Schleimhäute bei Kontakt eingestuft.
Referenzen
- Maleic and Fumaric Acids; ULLMANN’S Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_053
- https://pubchem.ncbi.nlm.nih.gov/compound/Fumaric-Acid
