Benzidin: Herstellung, Reaktionen und Verwendungen
Benzidin ist eine Diphenylbase, die häufig als Zwischenprodukt bei der Herstellung von Azofarbstoffen und -pigmenten verwendet wird. Es wird auch als Vernetzungsmittel in Polyurethan-Kunststoffen sowie als analytische und diagnostische Reagenzien verwendet.
Benzidin kann mit einer Vielzahl von Substanzen reagieren, darunter Kationen, Anionen, organische Verbindungen und Oxidationsmittel. Diese Vielseitigkeit macht sie zu wertvollen Werkzeugen für ein breites Anwendungsspektrum.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Benzidin
Benzidin, eine zweisäurehaltige Verbindung mit der chemischen Formel C12H12N2 und einer Molmasse von 184,24 g/mol, weist die folgenden physikalischen Eigenschaften auf:
| Eigenschaft | Wert |
|---|---|
| Aussehen | Weißes Pulver |
| Schmelzpunkt | 128 °C (grobe Stäbchen), 122-125 °C (metastabile Modifikation) |
| Siedepunkt | 400-401 °C |
| Dichte | 1,25 g/cm³ |
| Löslichkeit in Wasser | 1 Gewichtsteil in 2447 Teilen Wasser bei 12 °C, 106,5 Teile Wasser bei 100 °C |
| Löslichkeit in organischen Lösungsmitteln | Schwer löslich in Ether (45 Teile) und absolutem Ethanol (13 Teile) bei 20 °C |
| Säuregehalt | Diazid (kann in Lösung zwei Protonen abgeben) |
| Dissoziationskonstanten (bei 30 °C) | K1 = 9,3 x 10⁻¹⁰, K2 = 5,6 x 10⁻¹¹ |
| Neutralisationswärme | 106,5 kJ/mol |
| Dampfdruck | < 0,1 mmHg bei 25 °C |
| Brechungsindex | 1,652 bei 25 °C |
| Flammpunkt | 205 °C |
| Selbstentzündungstemperatur | 300 °C |
2. Chemische Reaktionen von Benzidin
Benzidin zeigt die folgenden chemischen Reaktionen:
- Lufteinwirkung: Benzidin verfärbt sich, wenn es der Luft ausgesetzt wird.
- Wasserbeständigkeit: Benzidin ist wasserbeständig.
- Farbreaktionen: Benzidin bildet blaue, grüne oder rote Färbungen und fällt mit Oxidationsmitteln aus. Diese Reaktionen sind wertvoll für den Nachweis von Oxidationsmitteln.
- Chlorierung und Bromierung: Benzidin wandelt sich in 3,3′,5,5′-Tetrachlorbenzidin bzw. Tetrabrombenzidin um.
- Nitrierung und Sulfonierung: Benzidinsulfat ergibt durch Nitrierungsreaktionen 2-Nitrobenzidin, 2,2′-Dinitrobenzidin und 2,3′-Dinitrobenzol. Unter Sulfonierungsbedingungen können Sulfonsäuren und Sulfone des Benzidins gebildet werden.
- N-Acetylierung: Benzidin reagiert mit Essigsäureanhydrid unter Bildung von N-Acetylierungsprodukten wie N-Acetylbenzidin und N,N‘-Diacetylbenzidin. Diese Verbindungen kommen auch als Metaboliten in der Verdauung von Tieren vor.
- Diazotierung: Benzidin kann zu Tetrazoniumverbindungen diazotiert werden. Die erste Diazoniumgruppe koppelt heftig, während die zweite langsamer reagiert. Dies ermöglicht die Herstellung asymmetrischer Diazofarbstoffe.
- Salzbildung: Benzidin bildet mit Säuren Salze wie Benzidinmonohydrochlorid, Benzidindihydrochlorid und Benzidinsulfat.
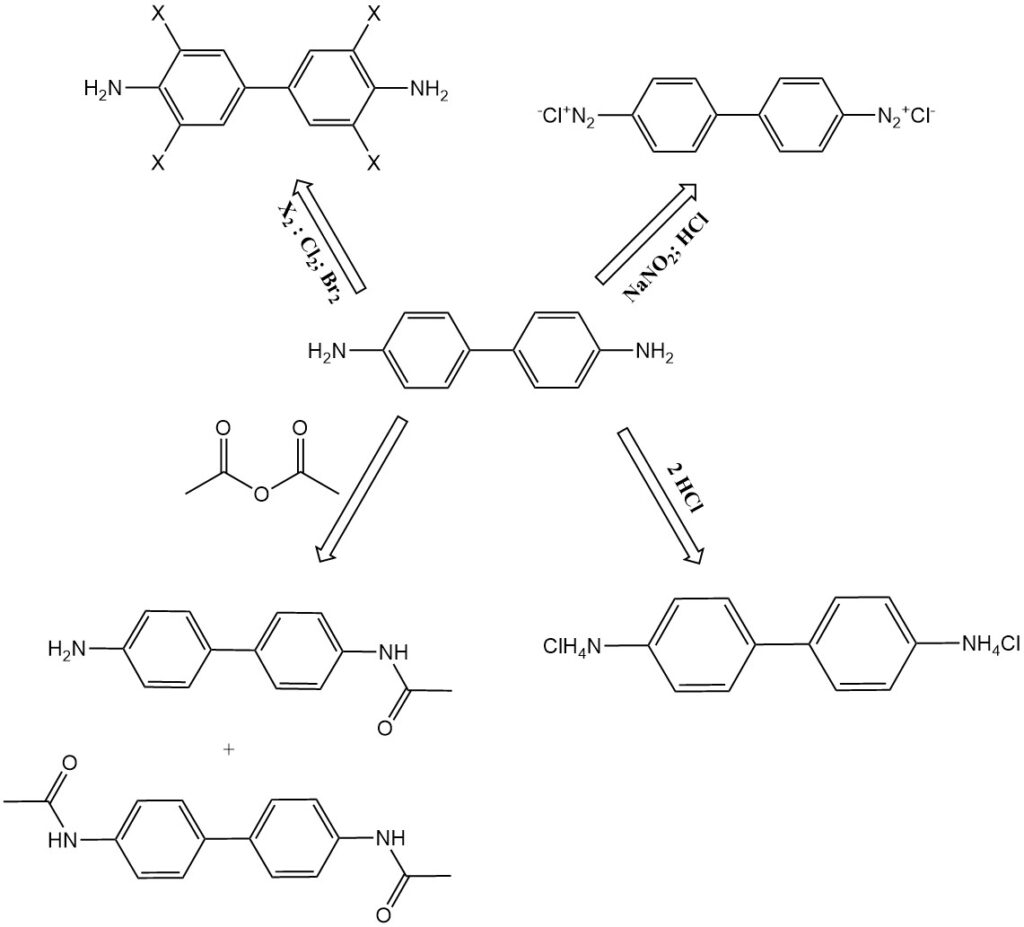
3. Herstellung von Benzidin
Benzidin wird in drei Stufen hergestellt:
- Reduktion von Nitrogruppen zur Bildung von Hydrazoverbindungen
- Benzidin-Umlagerung
- Basisisolation
Benzidin wird seit dem späten 19. Jahrhundert industriell aus Nitrobenzol hergestellt. Zu den gängigen Produktionsmethoden gehören die alkalische Eisenreduktion, die Amalgamreduktion und die elektrochemische Reduktion.
Das entstehende Hydrazobenzol wird beim Abkühlen mit Salzsäure oder Schwefelsäure umgelagert und das Produkt als Benzidinhydrochlorid oder Benzidinsulfat isoliert. Um das Risiko einer chronischen Toxizität zu minimieren, wird die Umwandlung dieser Salze in die freie Base nach Möglichkeit vermieden.
3.1. Reduktion von Nitrobenzol
Die Reduktion von Nitrobenzol zu Hydrazobenzol kann durch die folgende Gleichung dargestellt werden:
2 C6H5NO2 + 10 H → C6H5NH-NHC6H5 + 4 H2O
Dieser Reduktionsprozess ist als Haber-Prozess bekannt und verläuft in mehreren Stufen, wobei eine Zwischenkondensation einer Nitrosoverbindung mit einer Hydroxylaminverbindung zur Azoxyverbindung erfolgt.
Diese Methode führt zur Bildung symmetrischer Hydrazoverbindungen. Das erzeugte primäre Nebenprodukt ist das monozyklische primäre Amin wie Anilin, das der ursprünglichen Nitroverbindung entspricht. Dieses Nebenprodukt entsteht sowohl bei der weiteren Reduktion des Phenylhydroxyamins als auch bei der Disproportionierung der instabilen Hydrazoverbindung.
In industriellen Anwendungen werden verschiedene Reduktionstechniken eingesetzt, darunter:
1. Reduktion mit Zinkstaub: Bei dieser Methode werden aromatische Nitroverbindungen mit Zinkstaub in einer alkalischen Umgebung reduziert. Die Reaktion ist gegeben durch:
2 C6H5NO2 + 5 Zn + 10 NaOH → C6H5NH-NHC6H5 + 5 Na2ZnO2 + 4 H2O
Industriell wird das Nitrobenzol in einem hochsiedenden Lösungsmittel gelöst und Zinkstaub in der Lösung suspendiert. Natronlauge wird emulgiert und die Reduktion findet statt. Eine sorgfältige Kontrolle der Reaktionstemperatur ist erforderlich und der Prozess ist abgeschlossen, wenn die rote Farbe der Azostufe verschwindet.
2. Reduktion mit Eisen: Die Reduktion mit Eisen und Natriumhydroxidlösung ist in der präparativen Chemie weniger verbreitet, wurde jedoch für die kommerzielle Produktion untersucht. Die Reduktionsgleichung lautet:
2 C6H5NO2 + 4 Fe + 6 H2O → C6H5NH-NHC6H5 + 2 Fe(OH)2 + 2 Fe(OH)3
Bei diesem Verfahren werden verschiedene Formen von Eisen verwendet, beispielsweise Gusseisenspäne oder Eisenpulver. Die Reduktion wird in einem Molverhältnis von 1:2:4 für Nitrobenzol, Eisen bzw. Natriumhydroxid durchgeführt.
3. Reduktion mit Natriumamalgam: Natriumamalgam wird zur Reduktion von Nitrobenzol bei erhöhten Temperaturen eingesetzt. Die Reduktion erfolgt in einer emulgierten Mischung aus Nitrobenzol in Wasser oder Natriumhydroxid und es entsteht das Azobenzolprodukt. Während dieses Prozesses kann es jedoch zu einer gewissen Überreduktion zu monozyklischen Aminen kommen.
4. Elektrolytische Reduktion: Die elektrochemische Reduktion im kommerziellen Maßstab ist eine weitere Methode zur Reduktion von Nitro zu Hydrazoverbindungen. Dabei kommen Elektrolysezellen mit Kathoden, Diaphragmen und Anoden zum Einsatz und die Reaktion lässt sich wie folgt darstellen:
2 C6H5NO2 + 10 H+ + 10 e- → C6H5NH-NHC6H5 + 4 H2O
Die Reduktion wird bei erhöhten Temperaturen und spezifischen Stromdichten durchgeführt, wobei der Prozess durch die Steuerung der Zugabe von Reaktanten reguliert wird.
5. Katalytische Reduktion: Nitrobenzol kann durch katalytische Hydrierung in Gegenwart eines Palladium-Kohlenstoff-Katalysators zu Hydrazobenzol reduziert werden. Diese Methode kann verdünnten Alkohol, eine Base sowie erhöhte Temperatur- und Druckbedingungen umfassen.
In der präparativen Chemie werden auch andere Reduktionsmittel verwendet, beispielsweise verschiedene Metalle, Amalgame und organische Reduktionsmittel wie Methanol, Formaldehyd und Glucose, die je nach spezifischen Reaktionsanforderungen eingesetzt werden.
3.2. Benzidin-Umlagerung
Die Benzidin-Umlagerung ist ein Schlüsselschritt bei der Herstellung von Diaminodiphenylverbindungen. Diese Verbindungen entstehen durch Umlagerung aromatischer Hydrazoverbindungen, die zunächst durch Reduktion aromatischer Nitroverbindungen mit einer alkalischen Lösung entstehen.
Der Umlagerungsprozess, der typischerweise durch Mineralsäuren katalysiert wird, führt zur Bildung der Diaminodiphenylverbindungen (1), (2) und (3) sowie der Aminodiphenylaminverbindungen (4) und (5).

- Ortho-Umlagerungen erzeugen geringe Mengen an o-Benzidin (2,2′-Diaminodiphenyl) (2) und Diphenylin (2,4′-Diaminodiphenyl) (3).
- Durch partielle Umlagerungen entstehen o-Semidin (2-Aminodiphenylamin) (4) und p-Semidin (4-Aminodiphenylamin) (5).

Art und Menge der Umlagerungsprodukte werden durch die chemische Struktur des Ausgangsmaterials beeinflusst, können aber durch Variation der Reaktionsbedingungen nur geringfügig angepasst werden. Einige Nebenprodukte wie Diphenylin (3) fallen in Mengen von bis zu 15 % an, haben aber keinen kommerziellen Wert.
Die Benzidin-Umlagerung ist eine echte intramolekulare Reaktion, was bedeutet, dass aus Mischungen verschiedener Hydrazoverbindungen keine gemischten Benzidine entstehen. Stattdessen entsteht ausschließlich das entsprechende unsymmetrische Benzidin aus unsymmetrisch substituierten Hydrazobenzolen.
Bei industriellen Verfahren beginnt die Benzidinumlagerung mit der heißen Lösung, die durch die Reduktion des Nitrobenzols zum Hydrazobenzol entsteht. Während eine Zwischenisolierung des Hydrazobenzols nicht immer notwendig ist, ist sie in bestimmten Fällen, beispielsweise bei Amalgamreduktionen, ratsam.
Um den Azogehalt des Hydrazobenzols zu reduzieren, können vor der Umlagerung einige Reduktionsmittel wie Natriumhydrosulfit (Natriumdithionit) oder Zinkstaub zugesetzt werden.
Die Reaktion findet statt, wenn die Hydrazobenzollösung mit einer geeigneten Mineralsäure, typischerweise 10 – 30 %iger Salzsäure, 20 – 80 %iger Schwefelsäure oder einer Mischung aus beiden, gemischt wird.
Die optimale Temperatur für die Umlagerung liegt für die Diphenylbasen bei 100 °C. Es ist wichtig, die Temperaturen im angemessenen Bereich zu halten, da übermäßige Hitze den Ertrag verringern kann, der typischerweise bei 70–95 % angestrebt wird.
3.3. Isolierung des reinen Produkts
Der wichtigste Schritt der Benzidin-Umlagerung ist die Bildung des Salz- oder Schwefelsäuresalzes von Benzidin. Dieses Salz kann entweder direkt isoliert werden, beispielsweise durch Aussalzen mit Natriumchlorid oder Natriumsulfat, oder zunächst mit einer verdünnten Lauge, beispielsweise Natronlauge oder Ammoniaklösung, in die freie Base umgewandelt werden.
Die Nebenprodukte, insbesondere Anilin und Diphenylin, können aufgrund ihrer besseren Löslichkeit abgetrennt werden. Das Azobenzol ist die einzige Verbindung, die nach der Säureextraktion im inerten Lösungsmittel verbleibt und in den Reduktionsprozess zurückgeführt werden kann.
4. Verwendung von Benzidin
Benzidin hat mehrere Anwendungen, darunter:
- Farbstoffherstellung: Benzidin wird zur Herstellung von Azofarbstoffen für Wolle, Baumwolle und Leder verwendet. Allerdings ist seine Verwendung in dieser Funktion aufgrund seiner Karzinogenität zurückgegangen.
- Quantitative Bestimmung von Schwefelsäure: Benzidin kann zur Bestimmung der Schwefelsäurekonzentration verwendet werden.
- Nachweis und Bestimmung von Anionen und Metallionen: Mit Benzidin können verschiedene Anionen und Metallionen nachgewiesen und quantifiziert werden.
- Nachweis von freiem Chlor oder Pyridin: Benzidin kann zum Nachweis von Spuren von freiem Chlor oder Pyridin im Trinkwasser verwendet werden.
- Blutnachweis: Benzidin kann zum Nachweis von Blut anhand seines Farbumschlags von Grün nach Blau in Gegenwart von Wasserstoffperoxid und Peroxidasen verwendet werden.
- Gummiherstellung: Benzidin wird als Vernetzungsmittel bei der Herstellung von Gummiprodukten wie Reifen und Schläuchen verwendet.
- Kunststoffherstellung: Benzidin wird bei der Herstellung einiger Kunststoffe als Stabilisator verwendet.
- Pharmazeutische Produktion: Benzidin wird als Zwischenprodukt bei der Herstellung einiger Arzneimittel verwendet, beispielsweise Antihistaminika und Antispasmodika.
Benzidin ist eine hochgiftige Verbindung, wird jedoch weiterhin in verschiedenen chemischen Synthesen und Anwendungen verwendet.
5. Toxikologie von Benzidin
Akute orale Toxizität: LD50 bei Ratten = 1,57 g/kg
Subakute ernährungsbedingte Exposition: Zu den Nebenwirkungen bei Mäusen zählen trübe Schwellung der Leber, vakuoläre Degeneration der Nierentubuli, Hyperplasie myeloischer Elemente im Knochenmark und Veränderungen der Lymphzellen in Thymus und Milz.
Haut- und Lungenresorption: Es liegen nur begrenzte Informationen vor, aber systemische Manifestationen von Toxizität deuten darauf hin, dass es zu einer erheblichen Resorption kommen kann.
Intravenöse Injektion und Metabolismus: Benzidin wird in N-Acetylbenzidin und N,N‘-Diacetylbenzidin umgewandelt, die weiter in N-Hydroxy-N,N‘-diacetylbenzidin und 3-Hydroxy-N,N‘-diacetylbenzidin umgewandelt werden. Letztere Verbindung bindet an Nukleinsäuren.
Ergebnisse des Ames-Tests: Benzidin wurde im Ames-Test positiv getestet, und es wurde auch gezeigt, dass seine Metaboliten Mutationen auslösen.
DNA-Effekte: Benzidin führt zu DNA-Strangbrüchen und Zelltransformationen. Es induziert eine außerplanmäßige DNA-Synthese in HeLa-Zellen und Rattenhepatozyten.
Karzinogene Eigenschaften: Es wurde gezeigt, dass Benzidinhydrochlorid bei Mäusen hepatozelluläre Karzinome und bei Ratten, Hamstern und Menschen andere Krebsarten auslöst.
Benzidin ist ein starkes Karzinogen bei Tieren und Menschen. Es wird von der MAK-Kommission als Gruppe A1 und von der ACGIH als Gruppe A1b eingestuft.
Referenz
- Benzidine and Benzidine Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a03_539
