Aziridin: Herstellung, Reaktionen und Verwendungen

Aziridin ist eine gesättigte Dreiringverbindung mit einem einzelnen Stickstoffatom. Im Handel erhältliche Aziridine und ihre Derivate werden aus Ethylenimin oder Propylenimin hergestellt.
Ethylenimin, auch Aziridin genannt, wurde erstmals 1888 von Gabriel synthetisiert, damals jedoch fälschlicherweise als Vinylamin bezeichnet. Ethylenimin wird durch Reaktion von 2-Bromethylaminhydrobromid mit Silberoxid oder Kaliumhydroxid synthetisiert.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von Aziridin
Ethylenimin ist eine klare, farblose Flüssigkeit mit aminartigem Geruch. Es ist mit Wasser und den meisten organischen Flüssigkeiten mischbar. Bei Lagerung über festem Natriumhydroxid ist es unbegrenzt stabil.
Weitere Eigenschaften von Ethylenimin sind in Tabelle 1 aufgeführt.
| Eigenschaft | Wert |
|---|---|
| Molekulargewicht (g/mol) | 43,07 |
| Dichte bei 25 °C (g/ml) | 0,832 |
| Siedepunkt (Siedepunkt) (°C) | 57 |
| Schmelzpunkt (Fp.) (°C) | -74 |
| Dampfdruck bei 25 °C (kPa) | 28,5 |
| Brechungsindex (25 °C) | 1.4123 |
| Viskosität bei 25 °C (mPa·s) | 0,418 |
| Flammpunkt (geschlossener Tiegel) (°C) | -11 |
2. Chemische Reaktionen von Aziridin
Aziridin ist eine hochreaktive Verbindung, die zwei Hauptreaktionstypen eingehen kann: ringerhaltende und ringöffnende Reaktionen.
Ringerhaltende Reaktionen umfassen Prozesse wie die Alkylierung oder Acylierung des Stickstoffatoms im Ring. Ringöffnungsreaktionen beginnen mit der Protonierung des Stickstoffatoms im Ring, gefolgt von einem nukleophilen Angriff auf eines der Kohlenstoffatome.
Aziridin ist oft die kostengünstigste und effizienteste Möglichkeit, eine Ethylamingruppe in ein Polymer oder komplexes organisches Molekül einzubauen.
2.1. Homopolymerisation
Polyethylenimin (PEI) wird durch Homopolymerisation von Ethylenimin synthetisiert, katalysiert durch Säuren, Lewis-Säuren oder Haloalkane. Die Reaktion wird typischerweise bei 90–110 °C in Wasser oder organischen Lösungsmitteln durchgeführt. Das resultierende PEI hat eine durchschnittliche Molekularmasse von 10.000–20.000.
Um höhermolekulare PEIs zu erhalten, können difunktionelle Alkylierungsmittel wie Chlormethyloxiran oder 1,2-Dichlorethan zugesetzt werden, oder PEIs mit breiter Massenverteilung können ultrafiltriert werden. PEIs mit niedrigerem Molekulargewicht können durch Einarbeitung eines Amins mit niedrigem Molekulargewicht wie 1,2-Ethandiamin während der Polymerisation erhalten werden.
Dies ergibt einen Molekularmassenbereich von 300 bis 106. Die PEI-Polymerisation in organischen Lösungsmitteln mit Vernetzung führt zu festen PEIs. Die PEI-Polymerisation kann auch auf den Oberflächen organischer oder anorganischer Materialien durchgeführt werden, wodurch das PEI am Träger verankert wird.
Alle mit diesen Methoden erzeugten PEIs weisen stark verzweigte Strukturen mit einer annähernd kugelförmigen Form auf. Die Verteilung der Amine in diesen Polymeren beträgt etwa 30 % primär, 40 % sekundär und 30 % tertiär, wie durch 13C-NMR-Spektroskopie bestimmt.
Spezielle Polymerisationstechniken können zu lineareren oder stärker verzweigten PEI-Strukturen führen. Darüber hinaus können PEIs durch polymeranaloge Reaktionen leicht modifiziert werden, um ihre Leistung in bestimmten Anwendungen zu verbessern.
2.2. Aziridin-modifizierte Polymere
Pfropfcopolymere von Aziridin können durch Reaktion von Ethylenimin mit Polymeren synthetisiert werden, die Carboxylgruppen oder Amine in ihrer Struktur aufweisen. Dadurch wird die Haftung des Polymers auf anionischen Oberflächen oder Oberflächen mit Hydroxylgruppen verbessert.

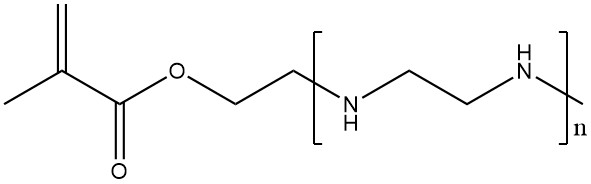
Eine weitere Methode, Seitenketten vom Polyethylenimin-Typ in andere Polymere einzuführen, besteht in der (Co-)Polymerisation von Monomeren, die mit Oligoethylenimin-Seitenketten funktionalisiert sind. Dieser Ansatz führt zu Polymeren mit hohen Ladungsdichten, ohne dass Carbonsäuren erforderlich sind.
2.3. Polyfunktionelle Aziridine
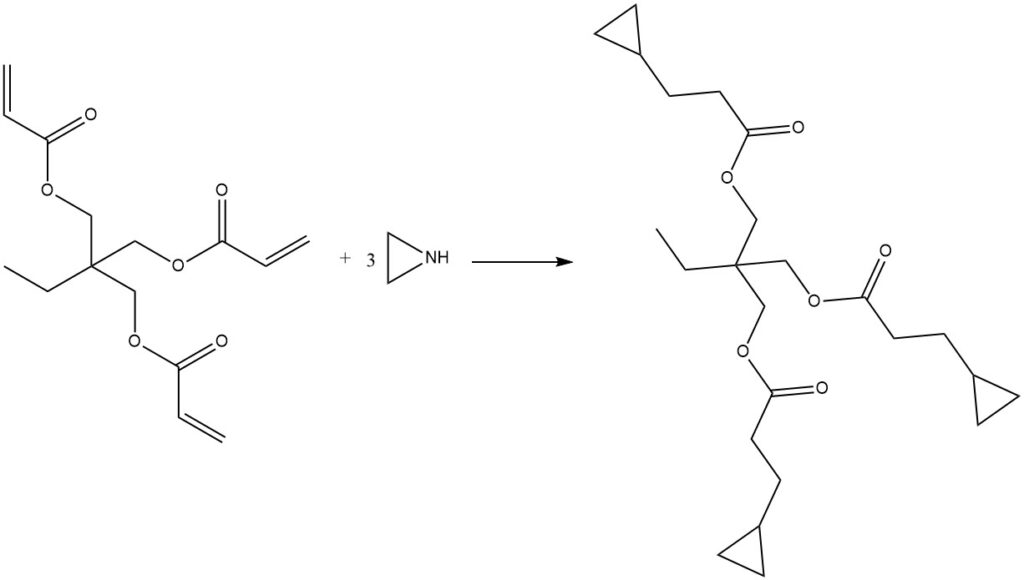
Ethylenimin kann mit trifunktionellen Acrylaten wie 2-Ethyl-2-(hydroxymethyl)-1,3-propandioltriacrylat oder 2,2-Bis(hydroxymethyl)-1,3-propandioltriacrylat reagieren, um trifunktionelle Aziridine herzustellen. Diese Reaktion findet typischerweise ohne Lösungsmittel oder Katalysator statt und die resultierenden Produkte sind klare, leicht viskose Flüssigkeiten.
2.4. Andere Reaktionen von Aziridin
Ethylenimin kann mit Schwefelwasserstoff unter Bildung von Thiolen und mit Thiolen unter Bildung von Aminoethylsulfiden reagieren. Diese Reaktion wird kommerziell zur Herstellung von Cysteamin, einem Rohstoff für die Synthese von Pharmazeutika, und 2,2′-Thiobisethylamin genutzt.

Aziridin kann auch mit 2-Mercaptoethanol reagieren, um 2-[(2-Aminoethyl)thio]ethanol, ein Zwischenprodukt für die Farbstoffproduktion, zu produzieren, und mit schwefeliger Säure, um Taurin zu produzieren, einen wesentlichen Zusatzstoff für die Ernährung von Säugetieren.
Dies sind nur einige Beispiele für industriell relevante Ringöffnungsreaktionen von Ethylenimin mit Schwefelnukleophilen.
Ethylenimin kann auch mit Aminen reagieren, um asymmetrisch substituierte Ethylendiamine zu erzeugen. Durch diese Reaktion kann beispielsweise N,N-Dimethyl-1,2-ethandiamin hergestellt werden.

Aziridin kann mit Oxiranen reagieren und dabei den Oxiranring öffnen, während der Aziridinring intakt bleibt. Diese Reaktion kann beispielsweise zur Herstellung von 1-Aziridin-Ethanol genutzt werden.
Eine weitere kommerzielle Anwendung von Ethylenimin ist die Reaktion mit Isocyanaten zu Iminoharnstoffen. Beispielsweise kann Aziridin mit 1,6-Diisocyanatohexan zu einem Polyharnstoff reagieren.

3. Herstellung von Aziridin
In der Literatur wurden vier verschiedene industrielle Methoden zur Herstellung von Ethylenimin (Aziridin) dokumentiert:
- Der Beta-Chlorethylamin-Prozess
- Der Dow-Prozess
- Das Wenker-Verfahren der BASF
- Der katalytische Dehydratisierungsprozess von 2-Aminoethanol von Nippon Shokubai
Derzeit werden nur noch die beiden letztgenannten Prozesse aktiv genutzt. Im Jahr 2006 wird die weltweite jährliche Produktionskapazität für Ethyleniminmonomer auf etwa 9.000 Tonnen geschätzt.
Aufgrund der Toxizität und hohen Reaktivität des Monomers vermarkten die beiden Hauptproduzenten BASF und Nippon Shokubai das Monomer nicht direkt, sondern wandeln es in ungiftige Polymere und Zwischenprodukte um.
3.1. Der β-Chlorethylamin-Prozess
Von 1938 bis 1963 wurde Ethylenimin in Deutschland kommerziell durch die Reaktion von 2-Chlorethylaminhydrochlorid mit Natriumhydroxid hergestellt. Dieses Verfahren weist, ähnlich wie das Dow-Verfahren, die Nachteile auf, dass ein ätzendes Chlorid-Nebenprodukt entsteht und das Risiko besteht, dass das Ethyleniminprodukt mit β-Chlorethylamin verunreinigt wird.
β-Chlorethylamin kann HCl leicht eliminieren, was eine unkontrollierte Polymerisation von Ethylenimin auslösen kann. Daher muss diese Kontamination sorgfältig vermieden werden.
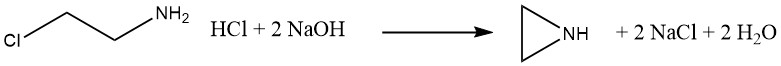
3.2. The Dow Process
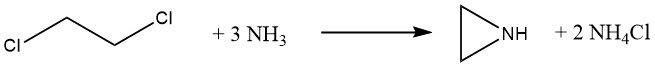
Dow Chemical entwickelte 1963 eine neue Methode zur Herstellung von Ethylenimin. Bei dieser Methode wurden 1,2-Dichlorethan und ein Überschuss an Ammoniak verwendet, was eine deutliche Reduzierung der Rohstoffkosten versprach. Dow stellte die Produktion jedoch 1978 aufgrund folgender Herausforderungen ein:
- Verunreinigungen im Ethyleniminprodukt
- Erhöhte Korrosionsraten
- Management von Abfallströmen
3.3. Der Wenker-Prozess
Das 1935 entwickelte Wenker-Verfahren ist heute die Grundlage für die meisten kommerziellen Aziridinproduktionen. BASF nutzte das Wenker-Verfahren über 30 Jahre lang ohne technische Probleme.
Der Wenker-Prozess besteht aus zwei Schritten. Zunächst reagiert 2-Aminoethanol mit Schwefelsäure zu 2-Aminoethylhydrogensulfat:

Dieses Produkt ist ein wasserlöslicher, nichtflüchtiger Feststoff mit ähnlichen Eigenschaften wie eine Aminosäure.
Dadurch wird sichergestellt, dass Ethylenimin im Gegensatz zu den β-Chlorethylamin- und Dow-Verfahren unverunreinigt bleibt. Zweitens reagiert 2-Aminoethylhydrogensulfat mit wässrigem Natriumhydroxid unter Bildung von Ethylenimin. Die Cyclisierung erfolgt vorzugsweise unter Druck bei erhöhten Temperaturen.
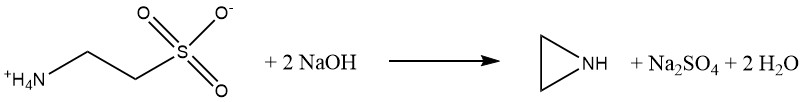
Anfangs betrugen die Erträge nur 26 %, heute werden Erträge von 85-90 % erreicht. Der Hauptvorteil dieses Verfahrens ist die Herstellung von reinem Ethylenimin mit minimalen Problemen bei der Abfallentsorgung. Der Nachteil sind jedoch die relativ hohen Rohstoffkosten.
3.4. Katalytische Dehydratisierung von 2-Aminoethanol
Seit den 1970er Jahren versuchen Forscher, eine direkte industrielle Synthese für Aziridin aus 2-Aminoethanol zu entwickeln. Der Schlüssel dazu war die Suche nach einem geeigneten Katalysator, was viele Jahre dauerte. Im Jahr 1990 entwickelte Nippon Shokubai ein industrielles Verfahren zur Herstellung von Ethylenimin durch katalytische Dehydratisierung von 2-Aminoethanol.
Die Reaktion wird bei 350–450 °C, vorzugsweise unter vermindertem Druck, unter Verwendung eines Katalysators mit schwach sauren und schwach basischen Zentren, wie beispielsweise mit Barium, Cäsium und Phosphor dotiertes SiO2, durchgeführt. Bei dieser Gasphasenreaktion können Selektivitäten bis zu 90 % bei Umsätzen von 40–80 % erzielt werden. Nicht umgesetztes 2-Aminoethanol wird aus der Produktmischung recycelt und als Einsatzstoff verwendet.
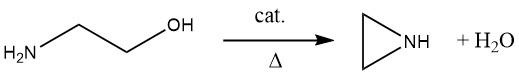
Der Vorteil des Gasphasenverfahrens gegenüber anderen industriellen Verfahren besteht darin, dass es sich um eine salzfreie, direkte einstufige Synthese auf Basis von 2-Aminoethanol handelt. Allerdings gibt es einige Nachteile:
- Zur Abtrennung von Ethylenimin von Nebenprodukten und zur Rückführung von 2-Aminoethanol ist eine mehrstufige Destillation erforderlich.
- Der Prozess erfordert viel Energie.
- Der Katalysator muss aufgrund der Koksablagerung und des Verlusts von Phosphorverbindungen wiederholt regeneriert werden.
4. Verwendung von Aziridinen
Aziridine werden in einer Vielzahl von Branchen eingesetzt, darunter Beschichtungen, Papierherstellung, Wasseraufbereitung, Erdöl, Textilien, Metalloberflächenbehandlung, Luftreinigung sowie Öl und Gas.
Beschichtungen: Polyfunktionelle Aziridine werden verwendet, um Polymere mit Carboxylgruppen zu vernetzen, wodurch vernetzte Polymere entstehen, die in Hochleistungsbeschichtungen verwendet werden, wie sie beispielsweise auf Holzplatten im Außenbereich aufgetragen werden.
Polyethylenimine werden als Haftklebstoffe und Haftvermittler bei der Herstellung von Verbundfolien aus Materialien wie Polypropylen verwendet. Sie sind außerdem wirksame Pigmentdispergiermittel und Grundierungen, insbesondere für Klebstoffe auf Acrylatbasis. Darüber hinaus werden Polyethylenimine als Aminkomponenten in Epoxid- und Polyurethanharzen verwendet.
Papierherstellung: Polyethylenimin und Aziridin-modifizierte Polymere werden als Retentions- und Entwässerungshilfsmittel verwendet und ihre Rolle hat aufgrund des zunehmenden Papierrecyclings und geschlossener Wasserkreisläufe in der Industrie immer mehr an Bedeutung gewonnen. Polyethylenimine werden auch als Fixiermittel für lösliche und unlösliche Verunreinigungen, allgemein als „Stickies“ bezeichnet, verwendet.
Wasseraufbereitung: Polyethylenimine spielen eine entscheidende Rolle bei der Wasseraufbereitung als Klärhilfsmittel und wirksame Kieselsäure-Antikalkmittel. Sie können als Chelatbildner für verschiedene Schwermetallionen fungieren, darunter Kupfer, Rhodium, Quecksilber und Zink.
Durch Carboxymethylierung kann ihre Komplexierungsfähigkeit auf andere Schwermetalle und Erdalkalimetalle ausgeweitet werden. Polyethylenimine werden in Verfahren zur Anreicherung von Schwermetallen eingesetzt, wobei häufig Membrantechnologie zum Einsatz kommt.
Textilien: Polyethylenimine werden in der Vor- und Nachbehandlung des Färbens eingesetzt, um die Farbstofffixierung und Farbechtheit zu verbessern. Sie verbessern außerdem die antistatischen Eigenschaften hydrophober Fasern und tragen zur Schrumpffestigkeit bei.
Metalloberflächenbehandlung: Polyethylenimine werden als Glanzmittelkomponenten in galvanischen Bädern für Metalle wie Zink, Zinn, Kupfer und verschiedene Legierungen verwendet. Sie sind auch an Passivierungs- und Veredelungsprozessen beteiligt.
Luftreinigung: Polyethylenimine fungieren als Adsorbentien für saure Gase, Ozon und Aldehyde.
Öl und Gas: Polyethylenimine sind ein wesentlicher Bestandteil der Bohr-, Fertigstellungs- und Ölproduktionsprozesse in der Öl- und Gasindustrie. Sie werden mit sulfonierten Polymeren kombiniert, um den Flüssigkeitsverlust aus Bohrlochzement zu verhindern, und sie dienen als selektive Flockungsmittel in Bohrflüssigkeiten und Demulgatoren für bestimmte Rohölemulsionen.
Andere Anwendungen: Eine neue Technologie beinhaltet die Verwendung von Polyethylenimin zur Immobilisierung von Enzymen, ein Prozess mit verschiedenen Anwendungen. Die starke Affinität von Polyethylenimin zu Proteinen, wie sie beispielsweise in Haaren oder Haut vorkommen, öffnet Türen für Anwendungen in der Kosmetik und Körperpflege.
Die ursprünglich hohe Ladungsdichte von Polyethyleniminen kann durch chemische Modifikationen, beispielsweise Alkoxylierung, auf das gewünschte Niveau eingestellt werden. Schließlich werden Polyethylenimine als Zusatzstoffe in Waschmitteln verwendet.
5. Toxikologie von Aziridin
Ethylenimin ist eine hochgiftige Chemikalie, die auf allen Expositionswegen schädlich für Mensch und Tier sein kann. Beispielsweise liegt der LD50-Wert (oral, Ratte) bei nur 14 mg/kg, der LD50-Wert (Haut, Kaninchen) bei 13 mg/kg und der LC50-Wert (10-minütige Inhalation, Maus) bei 2236 ppm.
Einatmen: Die Einwirkung hoher Konzentrationen von Ethylenimin kann zu einer sofortigen Reizung der Nase und der Augen führen, gefolgt von Ödemen und Lungenschäden. Der Tod kann innerhalb weniger Tage eintreten.
Hautkontakt: Ethylenimin ist ein Hautallergen und kann schwere Reizungen verursachen. Es kann auch über die Haut aufgenommen werden und das zentrale Nervensystem, die Leber und die Nieren schädigen. Es wurden zwei Todesfälle durch Einatmen und Hautkontakt mit Ethylenimin gemeldet.
Einnahme: Auch Ethylenimin ist bei Einnahme hochgiftig.
Augenkontakt: Ethylenimin reizt stark die Augen.
Mutagenität und Karzinogenität: Ethylenimin hat sich bei Bakterien und Fruchtfliegen als mutagen erwiesen. Es hat sich auch bei Mäusen als krebserregend erwiesen, es gibt jedoch keine Hinweise auf eine Karzinogenität beim Menschen.
Vorschriften: Ethylenimin wird von der OSHA als krebsverdächtiger Stoff eingestuft und unterliegt strengen Vorschriften zur Verhinderung einer Exposition. Die ACGIH empfiehlt einen Schwellenwert (TLV) von 0,5 ppm und betont, wie wichtig es ist, Hautkontakt zu vermeiden.
Die DFG stuft Ethylenimin als Karzinogen der Klasse A 2 und als Keimzellmutagen der Kategorie 2 ein, was besondere Schutzmaßnahmen und eine laufende Überwachung erfordert.
Referenz
- Aziridines; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a03_239.pub2
