4-Méthyl-2-pentanone: production, réactions et utilisations

La 4-méthyl-2-pentanone est un liquide incolore avec une odeur de cétone moins prononcée. La 4-méthyl-2-pentanone est peu soluble dans l’eau mais miscible avec les solvants organiques courants.
Il forme un azéotrope avec l’eau et avec un grand nombre de solvants. Par exemple, l’azéotrope avec de l’eau (Eb 87,9 °C) contient 75,7 % en poids de 4-méthyl-2-pentanone, et celui avec du n-butanol (Eb 114,4 °C) 70 % en poids de 4-méthyl-2-pentanone.
Table des matières
1. Production de 4-méthyl-2-pentanone
La 4-méthyl-2-pentanone peut être produite industriellement à partir d’acétone ou d’alcool isopropylique selon les procédés suivants :
1.1. En trois étapes de l’acétone via l’alcool diacétonique et l’oxyde de mésityle, avec hydrogénation ultérieure
Dans ce processus, l’acétone subit une condensation catalysée par un alcali dans la première étape pour former de l’alcool diacétonique.
La déshydratation de ce dernier en oxyde de mésityle a lieu en phase liquide à 90 – 130 °C sur un catalyseur acide, tel que l’acide phosphorique ou sulfurique, avec une sélectivité élevée.
L’hydrogénation sélective de la double liaison carbone-carbone dans l’oxyde de mésityle pour donner la 4-méthyl-2-pentanone peut être effectuée à la fois en phase liquide et en phase gazeuse avec divers catalyseurs, de préférence le palladium. La sélectivité est excellente.
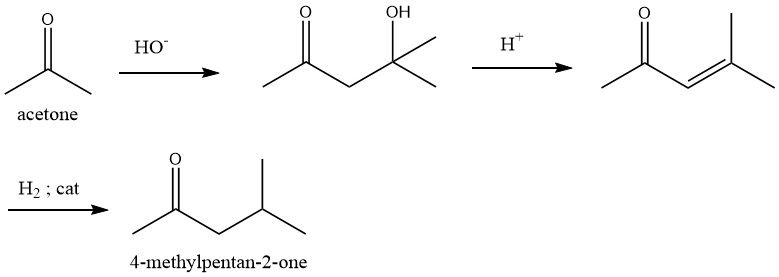
La déshydratation et l’hydrogénation peuvent également être combinées en une seule étape de procédé.
1.2. En deux étapes de l’acétone via l’oxyde de mésityle
Le procédé en deux étapes est moins important industriellement.
L’acétone est convertie en une seule étape en oxyde de mésityle, qui est ensuite hydrogéné en 4-méthyl-2-pentanone dans une deuxième étape.
Des catalyseurs tels que le chromite de cuivre ou le phosphate de zirconium sont utilisés pour la condensation, et le palladium sur oxyde d’aluminium pour l’hydrogénation.
Le 4-méthyl-2-pentanol est formé comme sous-produit.
1.3. En une seule étape à partir d’acétone et d’hydrogène
Pour la production en une seule étape de 4-méthyl-2-pentanone à partir d’acétone et d’hydrogène, une combinaison d’un échangeur de cations avec du palladium est généralement utilisée comme catalyseur.
L’acétone est alimentée en hydrogène sur le catalyseur chargé de palladium à 130 °C et 0,5 – 5,0 MPa. Une sélectivité > 95 % pour une conversion < 50 % est ainsi atteinte.
En raison de la production croissante d’acétone par déshydrogénation de l’alcool isopropylique, la production de 4-méthyl-2-pentanone comme sous-produit dans ce procédé devient plus importante.
2. Réactions chimiques de la 4-méthyl-2-pentanone
La 4-méthyl-2-pentanone subit une auto-oxydation pour former un peroxyde : après évaporation de mélanges 4-méthyl-2-pentanone-eau en présence d’air, une concentration dangereuse et croissante de peroxyde dans la phase aqueuse a été signalée.
Le peroxyde peut également être obtenu directement par oxydation avec du peroxyde d’hydrogène à 50 % en présence d’acides.
Dans les réactions de condensation avec des composés carbonylés tels que l’acétone, le groupe a-méthyle réagit généralement.
Seul le formaldéhyde est capable de subir des réactions de condensation avec le groupe a-méthylène. Les réactions industrielles usuelles telles que l’hydrogénation et l’amination réductrice peuvent être réalisées avec le groupement céto.
3. Utilisations de la 4-méthyl-2-pentanone
La principale application de la 4-méthyl-2-pentanone est celle de solvant pour les résines vinyliques, époxy et acryliques, pour les résines naturelles et pour la nitrocellulose.
Une autre utilisation est comme solvant pour les colorants dans l’industrie de l’imprimerie.
La 4-méthyl-2-pentanone est également un agent d’extraction polyvalent, par exemple pour la production d’antibiotiques ou l’élimination des paraffines de l’huile minérale pour la production d’huiles lubrifiantes.
L’importance de la 4-méthyl-2-pentanone en tant qu’intermédiaire de synthèse est relativement faible. Le produit le plus important est le 4-méthyl-2-pentanol, obtenu par hydrogénation de la cétone.
Le peroxyde de 4-méthyl-2-pentanone a une certaine importance en tant qu’initiateur de polymérisation pour l’éthylène et pour le durcissement des résines de polyester insaturé.
Référence
- Ketones; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a15_077
