Tetraidrofurano (THF): proprietà, reazioni, produzione e usi
Il tetraidrofurano (THF), noto anche come ossolano, è un etere ciclico con formula chimica C4H8O. Ha un’ampia applicazione nell’industria chimica.
Sommario
1. Proprietà fisiche del tetraidrofurano
Il tetraidrofurano (THF) è un liquido polare, volatile e incolore disponibile in commercio con una purezza minima del 99,9% in peso (quando distillato). Possiede un caratteristico odore simile all’acetone. Il THF è completamente miscibile con acqua, alcoli, eteri e altri solventi comuni.
La tabella 1 presenta alcune proprietà fisiche del THF.
| Proprietà | Valore |
|---|---|
| Massa molare | 72,1 g/mol |
| Punto di ebollizione | 66 °C |
| Punto di fusione | -108,5 °C |
| Temperatura critica | 267 °C |
| Pressione critica | 5,19 MPa |
| Densità critica | 0,322 g/cm3 |
| Densità a 20 °C | 0,886 |
| Indice di rifrazione a 20 °C | 1,4073 |
| Capacità termica specifica | 1,765 J g-1 K-1 |
| Calore di vaporizzazione (66 °C, 101,3 kPa) | 435 J/kg |
| Calore di combustione | -35.141 kJ/kg |
| Limiti di esplosività in aria (25 °C) | 1,5 vol% (inferiore), 12,0 vol% (superiore) |
| Punto di infiammabilità (Abel-Pensky) | -22 °C |
| Momento di dipolo | 5,84 × 10-30 C.m |
| Costante dielettrica (20 °C) | 7,6 |
2. Reazioni chimiche del tetraidrofurano
Il tetraidrofurano è un prezioso materiale di partenza per reazioni importanti. Queste includono la polimerizzazione cationica con contemporanea apertura dell’anello di THF per produrre eteri glicolici bifunzionali ad alto peso molecolare con varie lunghezze di catena.
Questi prodotti hanno un’importanza economica nella produzione di materie plastiche essenziali. Inoltre, le reazioni di scissione dell’anello del tetraidrofurano sono la base per la disidratazione a butadiene, l’ossidazione ad acido succinico e la carbossilazione ad acido adipico o γ-valerolattone.
Il THF è il mezzo di reazione preferito per condurre reazioni di Grignard o riduzioni usando reagenti come LiAlH4. Viene anche usato come legante nei complessi di coordinazione, come quelli occasionalmente impiegati nelle polimerizzazioni stereospecifiche.
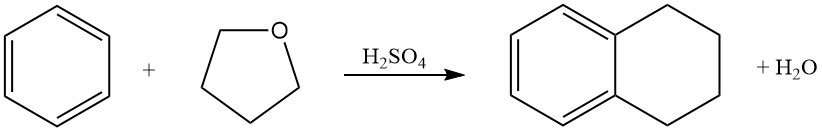
Il benzene reagisce con il tetraidrofurano in acido solforico per produrre tetralina (1,2,3,4-tetraidronaftalene).
Tuttavia, il THF reagisce facilmente con l’ossigeno (ad esempio, a contatto con l’aria), formando un idroperossido instabile come prodotto primario. L’aggiunta di idrochinone o 2,6-di-terz-butil-p-cresolo (BHT) (ad esempio, 250 mg/kg) può inibire la formazione di perossidi. La distillazione di tetraidrofurano contenente perossidi concentra i perossidi, portando a un elevato rischio di esplosione, anche su scala di laboratorio.
3. Produzione di tetraidrofurano
3.1. Produzione di tetraidrofurano da acetilene e formaldeide
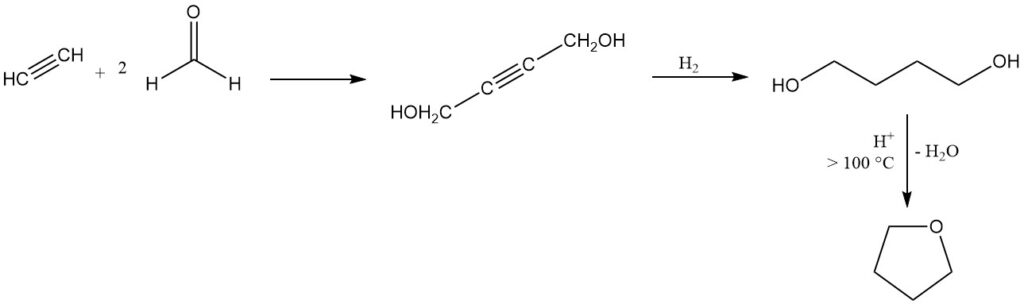
Il tetraidrofurano viene prodotto tramite il processo Reppe, sviluppato negli anni ’30, che rimane un metodo industriale dominante in Europa e negli Stati Uniti.
In questo processo, l’acetilene reagisce con la formaldeide per produrre 2-butino-1,4-diolo, seguito da idrogenazione a 1,4-butandiolo che poi subisce una ciclizzazione acido-catalizzata con l’eliminazione di acqua sopra i 100 °C per produrre THF.
Diversi catalizzatori sono adatti per questa ciclizzazione, tra cui acidi inorganici, alluminosilicati acidi e ossidi di metalli terrosi o terre rare. Una conversione quasi quantitativa e una resa prossima al 100% possono essere ottenute in un processo continuo a pressione atmosferica utilizzando l’allumina come catalizzatore.
Ciò richiede la distillazione continua del tetraidrofurano formato dalla miscela di reazione, alimentando contemporaneamente 1,4-butandiolo puro a un tasso di consumo corrispondente. Questo metodo ha un’elevata efficienza del catalizzatore, consentendo una significativa produzione di THF per unità di catalizzatore.
BASF ha sviluppato un processo a media pressione per la conversione selettiva del butandiolo grezzo in THF con un’energia aggiuntiva minima.
La miscela THF-vapore ottenuta dalla ciclizzazione viene prima rettificata per isolare l’azeotropo corrispondente (5,3% in peso di acqua, punto di ebollizione 62,3 °C), che viene trattato con idrossido alcalino, seguito da distillazione per ottenere THF anidro.
I processi industriali possono superare la formazione di miscele azeotrope mediante distillazione sotto pressione.
3.2. Produzione di tetraidrofurano mediante acetossilazione del butadiene
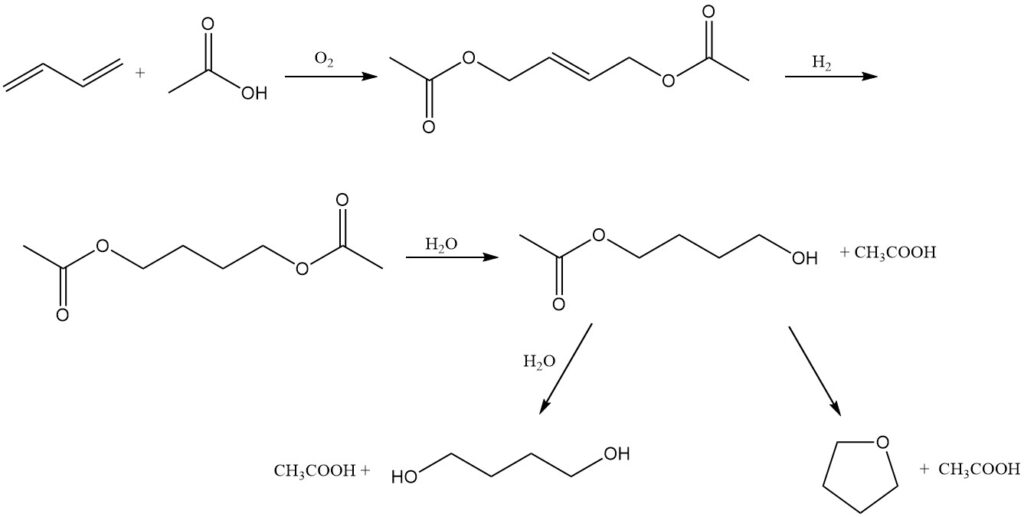
Mitsubishi-Kasei Corporation in Giappone offre un percorso alternativo per la coproduzione di 1,4-butandiolo e tetraidrofurano, utilizzando il butadiene come materiale di partenza. Questo processo può essere spiegato dalle seguenti reazioni:
Ossidazione: il butadiene subisce ossidazione a 3 MPa e 80 °C in presenza di un catalizzatore palladio-tellurio, acido acetico e una miscela azoto-ossigeno. Questa reazione produce 1,4-diacetossi-2-butene.
Idrogenazione: il 1,4-diacetossi-2-butene ottenuto viene quindi idrogenato per formare 1,4-diacetossibutano.
Idrolisi: infine, il 1,4-diacetossibutano viene idrolizzato a 1,4-butandiolo o THF.
3.3. Produzione di tetraidrofurano mediante processo di ossido di propilene
Arco produce 1,4-butandiolo tramite un processo che prevede i seguenti passaggi:
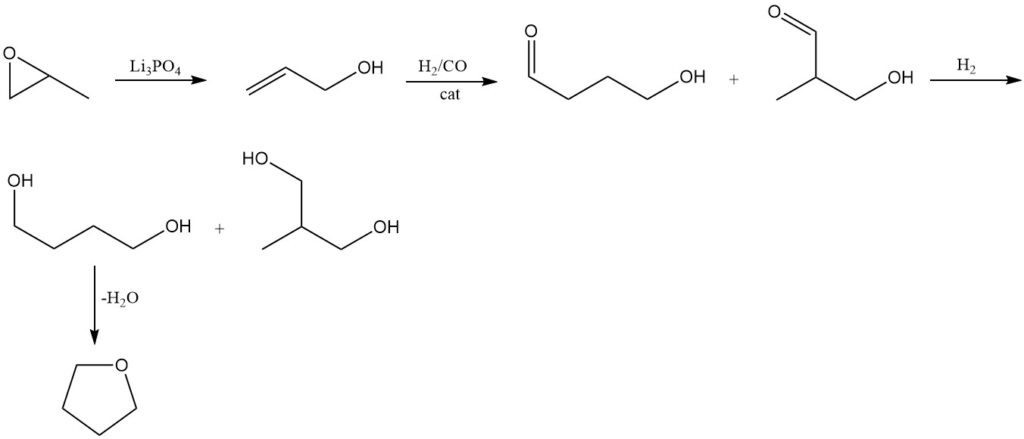
L’ossido di propilene viene isomerizzato in alcol allilico utilizzando metodi convenzionali a 250–300 °C e 1 MPa di pressione su un catalizzatore di trilitio ortofosfato (Li3PO4).
L’alcol allilico risultante subisce idroformilazione utilizzando il processo Kuraray. Questa reazione produce 4-idrossibutirraldeide come prodotto primario insieme a 3-idrossi-2-metilpropionaldeide come sottoprodotto.
La successiva idrogenazione delle aldeidi ottenute forma 1,4-butandiolo come prodotto principale, accompagnato dalla formazione di 2-metil-1,3-propandiolo.
Come nei metodi precedenti, il tetraidrofurano viene prodotto disidratando 1,4-butandiolo utilizzando un catalizzatore acido.
3.4. Produzione di tetraidrofurano mediante idrogenazione dell’anidride maleica
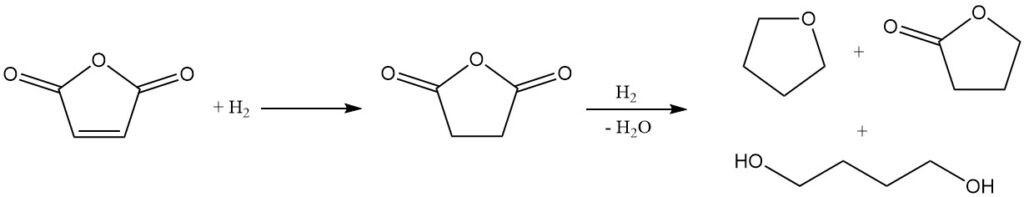
Grazie alla sua struttura chimica, l’anidride maleica è un promettente materiale di partenza per la sintesi di butandiolo, THF e γ-butirrolattone. Mitsubishi-Kasei ha originariamente sviluppato e implementato un processo su scala industriale utilizzando l’anidride maleica. Tuttavia, da allora ha abbandonato questo metodo in favore del suo più recente processo di acetossilazione del butadiene.
Diverse aziende, tra cui Davy-McKee Ltd., BP, Sohio e Shinwha Petrochemical, hanno adottato processi simili per la produzione di butandiolo e tetraidrofurano. Ad esempio, Shinwha Petrochemical in Corea del Sud gestisce un impianto basato sul processo McKee, con una capacità di 20.000 tonnellate di butandiolo all’anno.
Il passaggio iniziale di questo processo è l’idrogenazione in fase vapore del maleato di etile. Le condizioni di reazione possono essere manipolate per controllare il rapporto tra THF e butandiolo nella miscela di prodotti finali.
C’è un crescente interesse nell’uso dell’anidride maleica come materia prima per la produzione di tetraidrofurano, e sembra che stia guadagnando terreno come potenziale sostituto del processo Reppe.
3.5. Produzione di tetraidrofurano mediante processo n-butano-anidride maleica
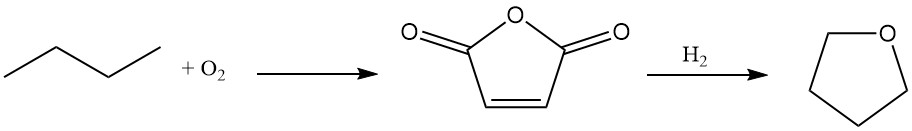
Du Pont offre un nuovo processo in due fasi per la sintesi del tetraidrofurano utilizzando n-butano come materiale di partenza.
L’n-butano viene ossidato ad anidride maleica con un’elevata resa (70-75%) utilizzando un catalizzatore di ossidazione unico, trasportabile e resistente all’abrasione.
La soluzione acquosa di acido maleico risultante subisce idrogenazione su uno speciale catalizzatore al palladio drogato con renio. Questa fase offre flessibilità, consentendo la produzione selettiva di butandiolo o THF in base ai requisiti del processo.
Il processo è stato sperimentato con successo ed è stato implementato nella provincia spagnola delle Asturie, con una capacità produttiva annuale di 45.000 tonnellate.
3.6. Produzione di tetraidrofurano mediante processi pentosano/furfurale
L’interesse per la produzione di tetraidrofurano dal furfurale è cresciuto grazie all’uso di risorse rinnovabili. I pentosani, abbondanti nei prodotti di scarto agricoli, sono i materiali di partenza.
Il processo per la produzione di THF dal furfurale prevede due fasi catalitiche:
- Il furfurale subisce una decarbonilazione catalitica per formare furano.
- Il furano viene quindi idrogenato per produrre THF.
4. Usi del tetraidrofurano
Il tetraidrofurano è utilizzato in vari settori, con il volume maggiore come monomero per il poli(tetrametilene ossido) (PTMO), noto anche come poli(tetrametilene etere glicole) (PTMEG) o politetraidrofurano (PTHF). PTMO è un componente importante nella produzione di:
- Poliuretani termoplastici
- Fibre elastiche
- Elastomeri stampati
- Copoliesteri
- Copoliammidi
- Rivestimenti in poliuretano
Il PTMO commerciale è disponibile con vari nomi commerciali, tra cui Terathane (DuPont), Polytetrahydrofuran (BASF) e Polymeg (Quaker Oats).
Una porzione più piccola di THF viene utilizzata come solvente per applicazioni quali rivestimenti, adesivi e vernici speciali basate su materiali come polivinilcloruro (PVC) o poliuretani e come cosolvente negli inchiostri da stampa, come agente di estrazione e come mezzo di reazione, in particolare per le sintesi organometalliche in chimica organica.
È anche un comune reagente di laboratorio e un intermedio nelle sintesi chimiche di prodotti di consumo e industriali come prodotti nutrizionali, farmaceutici e insetticidi.
5. Tossicologia del tetraidrofurano
Una ricerca approfondita dell’Industrial Hygiene and Pharmacology Institute della BASF suggerisce che il THF presenta una tossicità minima, paragonabile all’acetone, in contrasto con precedenti rapporti probabilmente basati su campioni impuri.
Studi sugli animali che comportano un’esposizione cronica (1 anno a 1000 ppm, 2 anni a 3000 ppm) al THF non hanno rivelato sintomi di avvelenamento significativi nei ratti, nei gatti o nei conigli. Tuttavia, queste concentrazioni (1000-3000 ppm) causerebbero gravi irritazioni delle mucose negli esseri umani.
Simile all’etanolo, il THF viene rapidamente metabolizzato dall’organismo.
Grazie alle sue forti proprietà solventi, il tetraidrofurano dissolve gli strati esterni di cheratina della pelle e delle mucose, penetrando rapidamente nei tessuti più profondi. Questa caratteristica provoca gravi irritazioni ma non causa sensibilizzazione (reazione allergica).
La formazione di perossido durante lo stoccaggio può esacerbare l’irritazione cutanea e il contatto con ferite o sotto le unghie può indurre un dolore significativo.
Il THF viene facilmente assorbito attraverso la pelle, simile al metanolo. Si dovrebbe evitare il contatto prolungato con la pelle e si raccomanda un’adeguata protezione delle mani.
Il limite di esposizione sul posto di lavoro stabilito per il tetraidrofurano è di 200 ppm (mL/m³). Questo valore è impostato per affrontare l’irritazione locale delle mucose causata dai vapori di THF, non i suoi effetti narcotici, che richiedono concentrazioni molto più elevate.
Riferimenti
- Tetrahydrofuran, Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a26_221.pub3
- Polyethers, Tetrahydrofuran and Oxetane Polymers; Kirk-Othmer Encyclopedia of Chemical Technology. – https://onlinelibrary.wiley.com/doi/10.1002/0471238961.2005201816182103.a01
- Tetrahydrofuran; Hamilton & Hardy’s Industrial Toxicology. – https://onlinelibrary.wiley.com/doi/10.1002/9781118834015.ch70
