Butanone: proprietà, reazioni, produzione e usi
Cos’è il butanone?
Il butanone, noto anche come metiletilchetone, è un chetone alifatico con formula chimica C4H8O. È un liquido incolore, a bassa viscosità e infiammabile con un caratteristico odore chetonico simile a quello dell’acetone.
Il butanone viene sintetizzato principalmente tramite il processo di deidrogenazione del 2-butanolo, simile alla produzione di acetone tramite deidrogenazione di alcol isopropilico gassoso utilizzando catalizzatori di rame, zinco o bronzo a temperature comprese tra 400 e 550 °C.
La conversione del 2-butanolo raggiunge l’80-95% e la selettività del butanone supera il 95%. I sottoprodotti includono buteni formati tramite disidratazione e chetoni superiori derivanti dall’autocondensazione. Nel 2005 la produzione mondiale di metiletilchetone ha raggiunto circa 1 milione di tonnellate.
Sommario
Dagli anni ’80, c’è stato un crescente interesse nell’utilizzare il 2-butanone come solvente in vernici e adesivi. Il metiletilchetone, in particolare, è visto come un concorrente dell’acetato di etile, specialmente quando usato come solvente bassobollente.
La sua versatilità come solvente si estende a varie applicazioni come nitrocellulosa, acetato di cellulosa-butirrato, etilcellulosa, resine acriliche, acetati di vinile e copolimero di cloruro di vinile-acetato di vinile, principalmente nella preparazione di rivestimenti superficiali sintetici.
La sua idoneità come solvente per lacche è attribuita alla sua bassa viscosità, all’elevata concentrazione di solidi e all’ampia gamma di diluenti compatibili.
La rimozione del metiletilchetone dall’elenco degli inquinanti atmosferici pericolosi (HAP) nel 2005 ha svolto un ruolo significativo nel mantenere la posizione di mercato del butanone negli Stati Uniti. Inoltre, il butanone trova utilità come attivatore nelle reazioni ossidative, come agente estrattivo selettivo, come solvente specializzato per la deceratura delle frazioni di olio minerale e come intermedio chimico.
1. Proprietà fisiche del butanone
Il butanone è un solvente a basso punto di ebollizione e a rapida evaporazione con un punto di ebollizione di 79,6 °C. È solo parzialmente miscibile con acqua, mentre è completamente miscibile con la maggior parte dei solventi organici.
Il metiletilchetone forma miscele azeotropiche binarie e ternarie in combinazione con acqua e diversi composti organici.
Le proprietà fisiche del butanone includono:
- Massa molare = 72,1 g/mol
- Punto di fusione = -86,7 °C
- Densità del liquido a 25 °C = 0,7995
- Indice di rifrazione a 25 °C = 1,736
- Viscosità del liquido a 25 °C = 0,395 mPa.s
- Solubilità a 20 °C in acqua = 27,5 %
2. Reazioni chimiche del butanone
In condizioni normali e in assenza di ossigeno atmosferico, il butanone è stabile. Bisogna fare attenzione dopo una conservazione prolungata perché il perossido di metiletilchetone si forma in presenza di ossigeno. Possono verificarsi esplosioni a causa della decomposizione istantanea dei perossidi.
Il 2-butanone è insaponificabile e resistente al calore e alla luce. Tuttavia si decompone dopo una prolungata esposizione ai raggi UV per dare etano, metano, monossido di carbonio, etilene e diacetile.
Il diacetile si forma per ossidazione del metiletilchetone con aria in presenza di catalizzatori speciali.
Il metiletilchetone perossido, un catalizzatore di polimerizzazione, si forma per ossidazione del butanone con una soluzione di perossido di idrogeno.
L’acido nitrico e altri forti ossidanti ossidano il butanone in una miscela di acido formico e acido propionico.
Il 2-butanolo si ottiene mediante riduzione catalitica del butanone con idrogeno, mediante riduzione elettrolitica in soluzione di acetato di sodio o riduzione con amalgama di ammonio o idruro di litio e alluminio.
Un altro prodotto di riduzione è il 3,4-dimetil-3,4-esandiolo che si ottiene mediante riduzione elettrolitica del metiletilchetone in un mezzo acido o mediante riduzione con amalgama di magnesio.
Il metil etil chetone mostra reattività verso acido cianidrico, sodio e potassio idrogeno solforato, con conseguente formazione di prodotti di addizione.
In condizioni alcaline, il 2-butanone subisce reazioni di condensazione con aldeidi, portando alla produzione di chetoni insaturi più elevati. In particolare, quando si utilizza formaldeide, il metil isopropil chetone viene prodotto come intermedio per le sintesi successive, presentando un’area di interesse specifica.
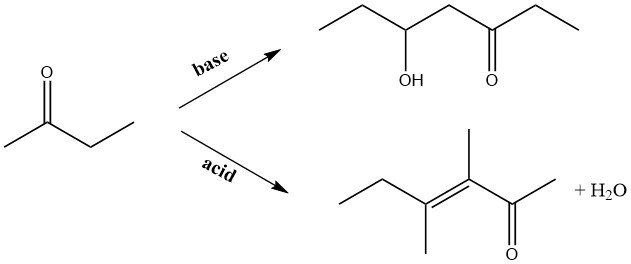
Durante l’autocondensazione catalizzata da basi in fase liquida o la condensazione in fase gassosa su catalizzatori di rame alcalinizzati, il gruppo carbonilico nella molecola reagisce con il gruppo metilico. Al contrario, nella condensazione catalizzata da acidi, il gruppo metilene adiacente al gruppo carbonilico diventa il sito di attacco.
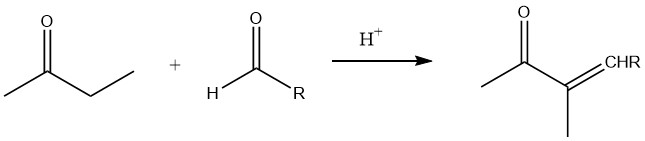
La condensazione di butanone e citrale determina la formazione di metilpseudoionone, che può successivamente subire ciclizzazione per produrre metilionone. Questo composto è impiegato nella produzione di profumi sintetici alla violetta.
In presenza di aldeidi a basso peso molecolare, in particolare durante l’aldolizzazione catalizzata da basi e da acidi, la posizione α del gruppo carbonilico è principalmente coinvolta nella reazione.
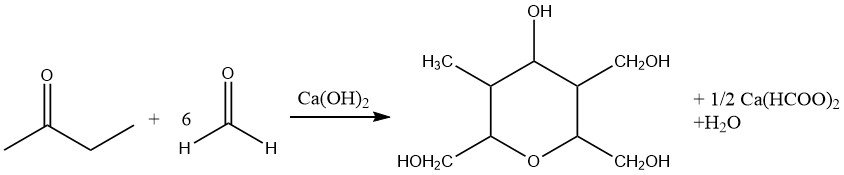
Pertanto, impiegando quantità inferiori a quelle stechiometriche di formaldeide nell’aldolizzazione catalizzata da basi si ottiene la formazione di 2-metil butano-1-ol-3-one. Inoltre, l’idrossimetilazione esaustiva accompagnata dalla riduzione del gruppo carbonilico (reazione di Cannizzaro incrociata) produce desossianidroeneaptite.
Quando il metil etil chetone reagisce con alcoli primari e secondari, produce chetoni più alti. La reazione con l’alcol sec-butile determina specificamente la formazione di etil amil chetone.
Il metiletilchetone mostra reattività verso composti poliossilici o epossidi, portando alla formazione di prodotti ciclici.
Il nitrito di amile attacca selettivamente il gruppo CH2 in posizione α rispetto al gruppo carbonilico, dando la monoossima del diacetile.
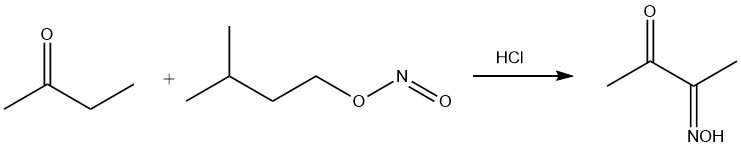
Il gruppo chetonico subisce una reazione con i gruppi amminici, con conseguente eliminazione di acqua. In combinazione con l’idrossilammina, questa reazione produce metil etil chetossima, un agente anti-pelle.
La condensazione del butanone con esteri alifatici e anidridi produce β-dichetoni.
I fenoli subiscono reazioni con il metil etil chetone, formando composti ossifenilenici. Quando reagisce con il fenolo, si ottiene il 2,2-idrossifenil butano, un omologo dell’idrossifenil propano (bisfenolo A). Il bisfenolo A è un materiale importante utilizzato nella produzione di resine sintetiche.
Il metil etil chetone può essere sottoposto ad alogenazione in posizione α. Inoltre, reagisce con i composti di Grignard, con conseguente formazione di alcoli terziari.
In presenza di acetilene e ammide di sodio, viene sintetizzato il 3-metil-1-pentin-3-olo. Combinando il 2-butanone con N-metilformammide, si può ottenere N-metil-formil-amminobutano. Inoltre, la reazione di Reformatzky consente la produzione di β-ossiesteri utilizzando esteri sostituiti con monobromo.
3. Produzione di butanone
Il metodo principale per la produzione di butanone prevede la deidrogenazione del 2-butanolo (alcol sec-butilico, SBA). Questa tecnica di processo è impiegata in circa il 92% delle capacità di produzione globali, come riportato nel 2006.
Il 2-butanolo può essere facilmente ottenuto tramite un processo in due fasi di idratazione di n-buteni derivati da C4-raffinati petrolchimici. L’acido solforico liquido è utilizzato come catalizzatore in questo processo. In alternativa, una procedura in un unico passaggio prevede l’aggiunta diretta di acqua a una resina a scambio ionico acida stabilizzata, che funge da catalizzatore.
Il restante 8% di metil etil chetone viene prodotto tramite un metodo di produzione fatale tramite sintesi di Fischer-Tropsch o tramite ossidazione catalitica di n-butano liquido, con conseguente produzione di acido acetico e metil etil chetone come sottoprodotto.
3.1. Produzione di butanone tramite deidrogenazione catalitica di alcol sec-butilico in fase gassosa
La deidrogenazione di alcol sec-butilico (SBA) utilizzando catalizzatori di rame, zinco o bronzo è una reazione endotermica con una variazione di calore (ΔH) di -51 kJ/mol. L’aumento della temperatura porta a un aumento della concentrazione di butanone nella miscela di reazione, che si stabilizza a circa 350 °C, supponendo che non si verifichino reazioni successive.
Nella deidrogenazione in fase gassosa, il rame è il catalizzatore preferito, mentre i catalizzatori di zinco o bronzo richiedono in genere temperature di deidrogenazione più elevate (400 °C).
I catalizzatori di ossido di zinco spesso mostrano una selettività inferiore a causa di una reazione collaterale che coinvolge la disidratazione di SBA in n-buteni. Per la deidrogenazione di SBA, sono consigliati catalizzatori come platino su allumina, rame o cromo e rame e zinco su allumina, soprattutto quando SBA contiene quantità significative di acqua.
I catalizzatori commerciali vengono riattivati tramite ossidazione con aria dopo 3-6 mesi di utilizzo. La riattivazione diventa necessaria quando il tasso di conversione dell’alcol diminuisce nel tempo a causa della contaminazione dei siti catalitici attivi da parte di acqua, depositi di oligomeri di butene ed etere di-sec-butile. Per rimuovere questi contaminanti vengono impiegate temperature più elevate e ossidazione.
In genere, i catalizzatori commerciali mostrano una durata di diversi anni o più. Deutsche Texaco ha sviluppato una tecnologia di processo per la produzione di metiletilchetone basata sulla deidrogenazione di alcol sec-butile anidro utilizzando un catalizzatore di precipitazione a base di rame a temperature di 240-260 °C a pressione normale.
In questa tecnologia, l’alcol sec-butile viene prodotto tramite l’idratazione diretta di n-buteni catalizzata da una resina a scambio ionico acida stabilizzata in temperatura. Nonostante questa procedura eterogenea migliorata, l’acido solforico concentrato rimane il principale catalizzatore al mondo per la produzione di SBA tramite una via indiretta.
Nella via indiretta, il mono- o di-sec-butil solfato intermedio risultante dal primo passaggio di reazione viene idrolizzato in un passaggio di reazione successivo.
L’alcol sec-butile liquido viene vaporizzato in un evaporatore e il flusso di alcol gassoso risultante viene diretto a un reattore multitubo, dove avviene la deidrogenazione su un catalizzatore di rame. Il flusso di prodotto gassoso esce dal reattore e, dopo il raffreddamento a temperatura ambiente, viene separato in una fase liquida di metil etil chetone grezzo e una fase di idrogeno gassoso.
Il flusso liquido contiene ancora un po’ di SBA non convertito, insieme a 5-metil-3-eptanone, chetoni superiori e acqua, oltre al metiletil chetone desiderato. La formazione di 5-metil-3-eptanone, chetoni superiori e acqua avviene tramite autocondensazione di due o più molecole di metiletil chetone.
Il 2-butanone viene purificato tramite tre fasi di distillazione consecutive a pressione atmosferica. Nella prima fase, un flusso azeotropico di butanone-acqua viene raccolto come prodotto di testa, che viene ulteriormente purificato in una colonna di distillazione batch separata.
La seconda colonna produce il metiletilchetone puro desiderato (tipicamente con una purezza superiore al 99%) insieme a SBA miscelato con chetoni superiori come prodotto di fondo. Nella fase di distillazione finale, l’SBA non convertito viene distillato come prodotto di testa e riportato al serbatoio di alimentazione del processo. I prodotti di fondo di questa fase sono costituiti dai chetoni superiori formati come sottoprodotti durante il processo di sintesi.
3.2. Butanone come sottoprodotto del processo carbone-liquido di Fischer-Tropsch
Nel processo Fischer-Tropsch, avviene una conversione catalitica di monossido di carbonio e idrogeno, nota come gas di sintesi, per produrre idrocarburi liquidi. Questo processo produce un’ampia gamma di lunghezze di catena di idrocarburi e una quantità significativa di vari sottoprodotti.
Originariamente sviluppato negli anni ’20 dai ricercatori tedeschi Franz Fischer e Hans Tropsch, il processo Fischer-Tropsch è stato utilizzato commercialmente e ulteriormente migliorato da SASOL Ltd., un’azienda sudafricana, dal 1955 per la produzione di combustibili sintetici dal carbone.
Il processo prevede una tecnica in due fasi. Inizialmente, il carbone minerale viene gassificato per generare gas di sintesi, che viene poi sottoposto a una purificazione completa tramite assorbimento in sistemi di lavaggio, utilizzando la tecnologia Rectisol. Il gas di sintesi purificato viene successivamente convertito cataliticamente in idrocarburi.
Oltre ai prodotti primari come olefine, combustibile sintetico e cere, viene prodotta un’ampia gamma di ossigenati idrosolubili come sottoprodotti, che rappresentano circa il 3-6% di selettività nel flusso d’acqua durante la reazione.
Le tecnologie di separazione tradizionali vengono impiegate per purificare questi ossigenati, che includono alcoli, acidi organici, aldeidi, butanone e altri chetoni, in prodotti solventi di alto valore.
3.3. Produzione di butanone mediante ossidazione in fase liquida di n-butano
Nell’ossidazione in fase liquida di n-butano ad acido acetico, il 2-butanone è un sottoprodotto della reazione. Questo processo comporta l’auto-ossidazione o l’ossidazione diretta di n-butano in fase liquida attraverso un percorso di reazione radicale.
L’ossidazione iniziale produce metiletilchetone come prodotto intermedio, che, in seguito a ulteriore ossidazione, forma idroperossido di metiletilchetone. L’idroperossido di metiletilchetone viene successivamente scisso in due molecole, dando origine all’acido acetico desiderato come prodotto finale.
Union Carbide Corp. ha sviluppato un processo a flusso continuo che consente la raccolta parziale del butanone intermedio. Questo processo comporta l’ossidazione in fase liquida non catalizzata a 180 °C e 5,3 MPa, con un po’ di retromiscelazione. Attraverso questo processo, si ottengono sia metiletilchetone che acido acetico.
In condizioni di ossidazione continua con flusso a pistone a 150 °C, 6,5 MPa e un tempo di residenza di 2,7 minuti, si formano metil etil chetone e acido acetico con rapporti di massa fino a 3/1.
Celanese Corp. utilizza l’acido acetico come solvente, impiegando un sistema di catalizzatore di ossidazione omogeneamente disciolto costituito da acetato di cobalto e acetato di sodio. Questo processo in lotti viene condotto a temperature comprese tra 160 e 165 °C e a una pressione di 5,7 MPa. I prodotti risultanti sono butanone e acido acetico, con un rapporto di massa di 0,4/1,0.
3.4. Produzione di butanone mediante ossidazione di sec-butilbenzene
La tecnologia SPAM di Hock Phenol Synthesis Shell, che combina fenolo, acetone e butanone, si basa sull’ossidazione di una miscela di sec-butilbenzene e cumene nei rispettivi composti idroperossidici. Questi idroperossidi vengono quindi scissi in modo convenzionale utilizzando un acido inorganico, preferibilmente acido solforico, con conseguente miscela di fenolo, metiletilchetone e acetone come prodotti desiderati.
Nel processo, il flusso di chetoni grezzi viene separato dal fenolo tramite distillazione e successivamente purificato per ottenere i componenti chetonici puri desiderati. La scissione catalitica di sec-butilbenzene idroperossido (sBHP) con un acido inorganico per produrre fenolo e butanone è un processo ben noto da molti anni.
Tuttavia, nonostante l’importanza industriale del 2-butanone rispetto all’acetone, questa via alternativa non è stata commercializzata a causa di una sfida importante incontrata durante la fase di ossidazione. La velocità di ossidazione autocatalitica del sec-butilbenzene è diverse volte più lenta di quella del cumene, portando a reazioni collaterali indesiderate che influenzano negativamente la resa complessiva dei prodotti desiderati.
Secondo la ricerca di Shell, la diminuzione della velocità di reazione durante l’ossidazione del sec-butilbenzene è attribuita alla formazione di prodotti scissi che agiscono come scavenger di radicali nella miscela di reazione, presenti in concentrazioni di parti per milione (ppm). Questi acidi scavenger includono acido formico, acido acetico e fenolo.
Per superare l’impatto negativo sulla velocità di reazione, sono state suggerite le seguenti opzioni:
- Utilizzo di una miscela di sec-butilbenzene e cumene per stabilire quantità iniziali di idroperossido di cumene nel primo passaggio di reazione, che agisce come iniziatore.
- Riduzione della formazione di metanolo o etanolo come prodotti scissi nei flussi di riciclo, riducendo così al minimo la produzione degli acidi scavenger sopra menzionati.
- Introduzione di una soluzione acquosa di ammoniaca in una certa misura, consentendo agli acidi di formare i loro sali di ammonio assicurandosi al contempo di evitare la divisione di fase.
3.5. Produzione di butanone mediante ossidazione diretta di n-buteni (processo Hoechst-Wacker)
Il processo Hoechst-Wacker prevede l’ossidazione diretta di n-buteni, in cui l’ossigeno viene trasferito in una fase omogenea utilizzando una coppia di sali redox, PdCl2/2 CuCl. Successivamente, la coppia di sali subisce una riossidazione.
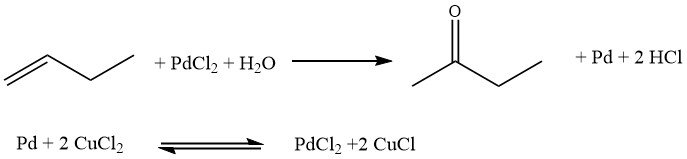
Tuttavia, questo processo presenta alcuni svantaggi. Porta alla formazione di butanoni clorurati e n-butanal, che sono sottoprodotti indesiderati. Inoltre, possono sorgere problemi di corrosione dovuti alla presenza di acidi liberi.
In questo processo, l’ossigeno viene trasferito utilizzando una soluzione acquosa di solfato di palladio e solfato ferrico. Principi simili di trasferimento dell’ossigeno sono stati impiegati in altri processi sviluppati dal Consortium for Electrochemistry e da Eastman Kodak.
4. Utilizzi del butanone
Il butanone, noto anche come metiletilchetone, è un solvente prezioso con proprietà simili all’acetone. Offre diversi vantaggi rispetto ad altri solventi con simili velocità di evaporazione:
- Elevato potere di dissoluzione: il butanone mostra una forte capacità di dissolvere varie sostanze.
- Elevato rapporto tra materia disciolta e viscosità: può dissolvere una grande quantità di materiale mantenendo una viscosità favorevole.
- Miscibilità con gli idrocarburi: il butanone può mescolarsi con numerosi idrocarburi senza influenzare il contenuto di solidi o la viscosità.
- Rapporto favorevole volume-massa: grazie alla sua bassa densità, fornisce un vantaggioso equilibrio tra volume e massa.
Il 2-butanone ha la capacità di dissolvere un’ampia gamma di sostanze naturali, plastiche e resine, tra cui colofonia, resine estere, nitrocellulosa, derivati della cellulosa (come acetato di cellulosa e acetobutirrato di cellulosa), resine epossidiche, resine alchidiche, fenoliche resine, polimeri di acetato di vinile e molti altri.
Tuttavia, non può sciogliere triacetato di cellulosa, acetato di cellulosa ad alto peso molecolare, poli(cloruro di vinile), poli(butirrale di vinile), gomma polisolfuro e gommalacca solo parzialmente.
Il solvente trova applicazioni in vari settori come la produzione di vernici, lacche e vernici, così come in diluenti per vernici, adesivi, cementi, sigillanti, nastri magnetici, pelle artificiale, carta trasparente, inchiostri da stampa, detergenti per apparecchiature elettroniche, cosmetici, prodotti farmaceutici, sgrassaggio di superfici metalliche e processi di estrazione.
Il butanone è anche usato come agente aromatizzante sintetico in alimenti e prodotti farmaceutici, come sterilizzatore per strumenti chirurgici e apparecchiature odontoiatriche e nella produzione di polvere senza fumo.
Sebbene il suo uso principale sia come solvente, il butanone ha un’importanza limitata come materia prima chimica. Tuttavia, può subire varie reazioni, come la condensazione con formaldeide per produrre metilisopropenilchetone, l’autocondensazione per formare etil amil chetone e la condensazione mista con acetone per ottenere metil amil chetone.
Il metil etil chetone è utilizzato nella produzione di profumi, antiossidanti, catalizzatori, perossidi e diacetali. Il metil etil chetossima in un’applicazione minore è impiegato come agente anti-pelle nelle lacche.
Inoltre, il perossido di butanone funge da iniziatore di polimerizzazione per poliesteri insaturi.
Nell’industria dei profumi, il 2-butanone reagisce con il citrale per produrre componenti di fragranze come il metilpseudoionone. Inoltre, è stato approvato come denaturante dell’alcol nella Repubblica Federale Tedesca dal 1962 (come decretato dalla Bundesmonopolverwaltung di Offenbach).
Riferimento
- 2-Butanone, Enciclopedia di chimica industriale di Ullmann. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a04_475.pub2
