Glutamate de sodium: production et utilisations
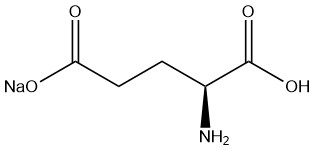
Le glutamate monosodique (MSG) est le sel de sodium de l’acide L-glutamique ; il est utilisé comme exhausteur de goût avec une production mondiale de 3 millions de tonnes en mars 2013 selon Nikkan Keizai Tsushinsha Co., Ltd. .
L’acide L-glutamique est l’un des acides aminés naturels les plus abondants et peut être trouvé lié à d’autres acides aminés en tant que constituant de protéines ou libre en solution en tant qu’acide aminé unique.
Il est utilisé dans les aliments commerciaux emballés et préparés, les soupes prêtes à l’emploi et comme assaisonnement de table.
L’acide L-glutamique a été isolé pour la première fois en 1866 par RITTHAUSEN à partir de l’hydrolysat acide de gluten de blé, et sa structure chimique a été identifiée par synthèse par WOLFF en 1890.
En 1908, KIKUNAE IKEDA a découvert la capacité du sel monosodique de l’acide glutamique à rehausser la saveur des aliments.
Table des matières
1. Production de glutamate de sodium
1.1. Processus classiques
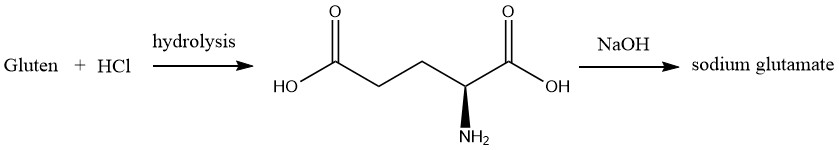
De 1909, date à laquelle la production industrielle de MSG a commencé, jusqu’en 1965, date à laquelle la production par le procédé d’extraction a cessé, le gluten de blé séparé de la farine de blé était la principale matière première.
Il a été utilisé en raison de sa teneur élevée en acide L-glutamique (environ 25% en poids). Après 1934, des flocons de soja dégraissés ont également été utilisés comme matière première, car ils ne produisaient pas d’amidon comme sous-produit.
La matière première a été hydrolysée par chauffage avec de l’acide chlorhydrique. Après concentration sous pression réduite et addition d’acide chlorhydrique concentré, l’hydrolysat est refroidi pour cristalliser le chlorhydrate d’acide L-glutamique.
L’acide L-glutamique peut être facilement séparé des autres acides aminés sous la forme de son chlorhydrate en raison de sa très faible solubilité dans l’acide chlorhydrique concentré.
Le chlorhydrate a été recueilli par filtration puis dissous dans de l’eau tiède et la solution filtrée pour éliminer les matières humiques insolubles, qui sont principalement formées par la réaction des acides aminés avec les glucides.
Le pH du filtrat a été ajusté à 3,2, le point isoélectrique de l’acide L-glutamique, avec de l’hydroxyde de sodium ou de l’ammoniac pour précipiter des cristaux d’acide L-glutamique.
Le rendement en acide L-glutamique était élevé en raison de sa faible solubilité dans l’eau (0,864 g pour 100 ml à 25°C). Les cristaux d’acide L-glutamique brut ont été mis en suspension dans de l’eau et neutralisés avec de l’hydroxyde de sodium.
La solution a ensuite été décolorée avec du charbon actif pour donner une solution limpide et concentrée pour cristalliser les cristaux de MSG.
Ensuite, les cristaux de MSG ont été séparés de la liqueur mère par centrifugation et séchés pour l’emballage.
1.2. Processus de fermentation

Au début des années 1950, DAGLEY et al. ont rapporté l’excrétion de petites quantités d’acides aminés dans le milieu de culture d’Escherichia coli. Ils ont découvert que l’ajout de sels d’ammonium en excès entraînait une augmentation de la production d’acides aminés.
En 1957, KINOSHITA et ses collègues ont découvert des bactéries qui accumulent de grandes quantités d’acide L-glutamique.
La méthode de KINOSHITA et al. ont donné des rendements d’acide L-glutamique d’environ 30% en utilisant Micrococcus glutamicus (rebaptisé plus tard Corynebacterium glutamicum), qui a été immédiatement appliqué à la production industrielle.
Les bactéries qui produisent de l’acide L-glutamique sont largement distribuées dans la nature, la plupart de ces bactéries sont Gram-positives, non sporulées, non mobiles et nécessitent de la biotine pour leur croissance.
Pour la production industrielle de MSG, la mélasse et l’hydrolysat d’amidon sont actuellement généralement utilisés comme matières premières. L’accumulation d’acide L-glutamique n’est pas gouvernée par sa biosynthèse dans les cellules bactériennes mais par sa sécrétion.
La biotine est l’une des vitamines essentielles à la croissance cellulaire, mais une concentration de biotine dans le milieu de culture suffisante pour la croissance cellulaire rend les membranes cellulaires imperméables au L-glutamate et entraîne une mauvaise accumulation.
La teneur critique en biotine des cellules pour la production d’acide L-glutamique est de 0,5 mg/g de cellules sèches. Ainsi, l’accumulation d’acide L-glutamique est maximale lorsque la concentration en biotine est sous-optimale pour une croissance maximale.
Par conséquent, les matières premières riches en biotine, telles que la mélasse de betterave et la mélasse de canne, ne pouvaient pas être utilisées avant la découverte des effets inhibiteurs de la biotine des esters d’acides gras polyoxyéthylène saturés en C16-C18.
On pense que la limitation de la quantité de biotine provoque une biosynthèse incomplète de l’acide oléique, ce qui entraîne une diminution des phospholipides dans la membrane cellulaire et rend la membrane perméable.
Les sels d’ammonium et l’urée sont utilisés comme sources d’azote pour la croissance microbienne et la formation de produits. Le milieu de culture devient acide du fait de l’assimilation des ions ammonium et de la formation d’acide L-glutamique.
L’ammoniac gazeux est avantageusement utilisé pour maintenir un pH neutre et éviter la dilution du bouillon, car il ne contient ni ions hydroxyles ni eau.
La biosynthèse de l’acide L-glutamique étant un processus aérobie, la pression d’oxygène dissous doit être strictement maintenue au-dessus de 1 kPa par aération et agitation dans le fermenteur.
Les progrès de la technologie de la fermentation ont permis d’augmenter l’accumulation et le rendement en acide L-glutamique au-dessus de 120 g/L et 63 %, respectivement.
Le pH du bouillon de fermentation est ajusté à 3,2 pour récupérer les cristaux d’acide L-glutamique, qui sont ensuite convertis en MSG par la même méthode que celle utilisée dans le processus d’extraction.
2. Propriétés du glutamate de sodium
Les groupes α-amino et γ-carboxyle de l’acide L-glutamique forment une liaison peptidique intramoléculaire lors de la déshydratation.
L’équilibre de cette réaction favorise la formation d’acide 2-pyrrolidone-5-carboxylique (PCA) lorsque le pH est faiblement acide ou faiblement basique. A pH neutre, la vitesse de déshydratation est minimale.
Dans des conditions fortement acides ou alcalines, l’équilibre favorise l’hydratation du PCA.
Dans des conditions normales de cuisson, il ne se produit ni racémisation ni déshydratation.
La valeur seuil (concentration minimale perceptible) du MSG est de 0,03 %, ce qui est inférieur à celui du chlorure de sodium (0,2 %) ou du saccharose (0,5 %).
L’activité d’amélioration de la saveur du MSG est augmentée de manière synergique en présence de 5′-inosinate et de 5′-guanylate.
L’acide L-glutamique est classé comme un acide aminé non essentiel. C’est une substance clé dans le métabolisme azoté des acides aminés.
L’azote inorganique est incorporé par amination réductrice du 2-oxoglutarate en L-glutamate, catalysée par la glutamate déshydrogénase.
Il existe de nombreux types d’aminotransférases dans divers organismes qui transfèrent un groupe amino d’un acide aminé à un acide 2-oxo, et beaucoup d’entre eux utilisent la paire glutamate/2-oxoglutarate comme donneur/accepteur d’amino.
Le L-glutamate est également le précurseur direct de la L-glutamine, du neurotransmetteur acide g-aminobutylique (GABA), du g-carboxyglutamate dans les protéines de liaison au calcium et du tripeptide glutathion.
3. Utilisations du glutamate monosodique
Assaisonnement
Le MSG est largement utilisé comme assaisonnement ou exhausteur de goût établi de longue date pour améliorer la palatabilité des aliments. L’effet du MSG est dû à son goût caractéristique, l’umami, qui est différent des quatre autres goûts de base, sucré, salé, acide et amer.
Depuis 2000, les progrès de la biologie moléculaire ont permis d’identifier les protéines qui fonctionnent comme des récepteurs du goût umami. Ils sont exprimés dans des cellules spécialisées des papilles gustatives sur la langue et à travers la cavité buccale.
Les glutamates sont omniprésents dans les aliments tels que le lait maternel, les tomates, le fromage, les algues, le poisson, la viande et les légumes. D’autres substances umami, c’est-à-dire les 5′-ribonucléotides tels que l’inosinate et le guanylate, se trouvent également dans la viande, le poisson et les champignons séchés.
Le glutamate monosodique fonctionne bien dans une grande variété d’aliments, notamment dans les viandes, les fruits de mer, les légumes, les soupes, les ragoûts et les chaudrées.
Les boissons alcoolisées, les fruits et les confiseries ne sont pas considérés comme améliorés par l’ajout de MSG.
L’effet du MSG sur l’odeur (ou l’arôme) est négligeable.
Utilisations industrielles
Selon le pH, l’acide glutamique peut être utilisé pour neutraliser des composés acides ou basiques.
Par exemple, le glutamate d’arginine est utilisé comme matière première pharmaceutique et cosmétique.
La réaction de l’acide glutamique avec l’acide chlorhydrique donne le chlorhydrate d’acide glutamique, qui est utilisé comme acidifiant gastrique.
Les propriétés de l’acide glutamique en tant qu’électrolyte amphotère sont exploitées dans les agents chélateurs, les tampons et les adjuvants pour détergents.
Le sel de sodium de l’acide pyroglutamique, qui est obtenu par déshydratation de l’acide glutamique suivie d’une neutralisation avec de l’hydroxyde de sodium, est très hygroscopique et est utilisé comme composant d’un facteur naturel d’hydratation de la peau humaine et comme numectant pour les cosmétiques.
Un polymère de glutamate de méthyle est utilisé comme agent de revêtement pour le cuir synthétique.
Un condensat avec du formaldéhyde est utile comme retardateur pour le plâtre.
Le composé N-acylé produit par réaction avec un acide gras à longue chaîne est un tensioactif anionique et est couramment utilisé pour les nettoyants pour la peau et les cheveux en raison de sa douceur et de sa grande sécurité.
Le dibutylamide de cet acide N-acylglutamique gélatinise les huiles non polaires et peut être utilisé comme agent de récupération des hydrocarbures marins déversés.
Références
Monosodium Glutamate; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_711.pub2
