Glutammato di sodio: produzione, proprietà e usi
Cos’è il glutammato di sodio?
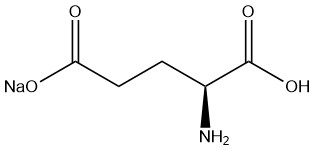
Il glutammato monosodico (MSG) è un sale sodico dell’acido L-glutammico, ampiamente utilizzato come esaltatore di sapore nell’industria alimentare. Secondo Nikkan Keizai Tsushinsha Co., Ltd., la produzione di MSG ha raggiunto i 3 milioni di tonnellate a marzo 2013.
L’acido L-glutammico è uno degli amminoacidi più abbondanti presenti in natura nelle proteine o come amminoacido libero in soluzione. È ampiamente utilizzato in alimenti commerciali come cibi confezionati e preparati, zuppe pronte e come condimento da tavola.
Nel 1866, RITTHAUSEN isolò l’acido L-glutammico dall’idrolizzato acido del glutine di frumento. Successivamente, nel 1890, WOLFF identificò la struttura chimica dell’acido L-glutammico attraverso mezzi sintetici.
KIKUNAE IKEDA scoprì le proprietà esaltatrici di sapore del sale monosodico dell’acido glutammico nel 1908.
Sommario
1. Produzione di glutammato di sodio
1.1. Produzione di glutammato di sodio mediante processi classici
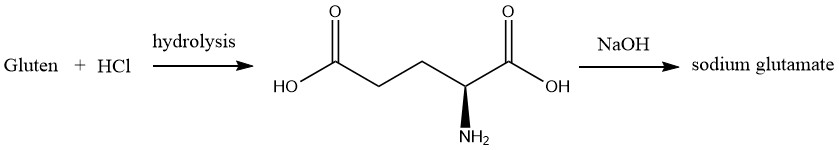
La produzione industriale di glutammato monosodico iniziò nel 1909 e continuò fino al 1965. Durante questo periodo, la principale materia prima utilizzata era il glutine di frumento che veniva separato dalla farina di frumento per il suo alto contenuto di acido L-glutammico (circa il 25% in peso).
Dopo il 1934, anche i fiocchi di soia sgrassati venivano utilizzati come materia prima perché non producevano amido come sottoprodotto.
L’idrolisi delle materie prime comportava il riscaldamento con acido cloridrico. Dopo la concentrazione a pressione ridotta e l’aggiunta di acido cloridrico concentrato, si formarono cristalli di cloridrato di acido L-glutammico raffreddando l’idrolizzato.
Grazie alla sua bassa solubilità in acido cloridrico concentrato, l’acido L-glutammico può essere facilmente separato dagli altri amminoacidi sotto forma di cloridrato.
I cristalli di cloridrato di acido L-glutammico sono stati raccolti tramite filtrazione, sciolti in acqua calda e la soluzione è stata filtrata per rimuovere eventuali materiali umici insolubili formati dalla reazione degli amminoacidi con i carboidrati.
Il pH del filtrato è stato regolato a 3,2, il punto isoelettrico dell’acido L-glutammico, con idrossido di sodio o ammoniaca per precipitare i cristalli di acido L-glutammico.
La resa di acido L-glutammico è stata elevata a causa della sua bassa solubilità in acqua (0,864 g per 100 mL a 25 °C). I cristalli grezzi di acido L-glutammico sono stati sospesi in acqua e neutralizzati con idrossido di sodio.
La soluzione è stata quindi decolorata con carbone attivo, ottenendo una soluzione limpida che è stata concentrata per cristallizzare il glutammato monosodico. I cristalli di glutammato monosodico sono stati separati dal liquore madre tramite centrifugazione ed essiccati per il confezionamento.
1.2.Produzione di glutammato di sodio mediante fermentazione

Nei primi anni ’50, DAGLEY e colleghi segnalarono la presenza di piccole quantità di amminoacidi nel terreno di coltura di Escherichia coli. Osservarono che l’aggiunta di sali di ammonio in eccesso determinava un aumento della produzione di amminoacidi.
Nel 1957, KINOSHITA et al. scoprirono batteri che accumulano quantità significative di acido L-glutammico. Il metodo di KINOSHITA et al. che utilizzava Micrococcus glutamicus (in seguito rinominato Corynebacterium glutamicum) forniva rese di acido L-glutammico di circa il 30%, che fu immediatamente applicato alla produzione industriale.
I batteri che producono acido L-glutammico sono ampiamente distribuiti in natura e la maggior parte di questi batteri sono Gram-positivi, non sporigeni, non mobili e necessitano di biotina per crescere. Per la produzione industriale di glutammato monosodico, melassa e idrolizzato di amido sono comunemente utilizzati come materie prime. L’accumulo di acido L-glutammico non è regolato dalla sua biosintesi nelle cellule batteriche, ma dalla sua secrezione.
La biotina è una delle vitamine essenziali per la crescita cellulare, ma una concentrazione di biotina nel mezzo di coltura sufficiente per la crescita cellulare rende le membrane cellulari impermeabili all’L-glutammato, con conseguente scarso accumulo.
Il contenuto critico di biotina delle cellule per la produzione di acido L-glutammico è di 0,5 mg/g di cellule secche. Pertanto, l’accumulo di acido L-glutammico è al massimo quando la concentrazione di biotina è subottimale per la crescita massima.
Pertanto, le materie prime ricche di biotina, come la melassa di barbabietola e la melassa di canna, non potevano essere utilizzate fino alla scoperta degli effetti inibitori della biotina degli esteri di acidi grassi poliossietilene saturi C16–C18.
Si ritiene che limitare la quantità di biotina causi una biosintesi incompleta dell’acido oleico, che si traduce in una diminuzione dei fosfolipidi nella membrana cellulare e rende la membrana permeabile.
I sali di ammonio e l’urea sono utilizzati come fonti di azoto sia per la crescita microbica che per la formazione del prodotto. L’assimilazione degli ioni ammonio e la formazione di acido L-glutammico causano l’acidità del terreno di coltura.
L’ammoniaca gassosa è utilizzata vantaggiosamente per mantenere un pH neutro ed evitare la diluizione del brodo perché non contiene né ioni idrossilici né acqua.
Poiché la biosintesi dell’acido L-glutammico è un processo aerobico, la pressione dell’ossigeno disciolto deve essere rigorosamente mantenuta al di sopra di 1 kPa mediante aerazione e agitazione nel fermentatore.
I progressi nella tecnologia della fermentazione hanno reso possibile aumentare l’accumulo e la resa dell’acido L-glutammico rispettivamente oltre 120 g/L e 63%.
Il pH del brodo di fermentazione viene regolato a 3,2 per recuperare i cristalli di acido L-glutammico, che vengono poi convertiti in glutammato monosodico con lo stesso metodo utilizzato nel processo di estrazione.
2. Proprietà del glutammato di sodio
L’acido L-glutammico subisce la formazione di legami peptidici intramolecolari tra i suoi gruppi α-ammino e γ-carbossilici in seguito a disidratazione. Questa reazione mostra una preferenza per la formazione di acido 2-pirrolidone-5-carbossilico (PCA) in condizioni di pH debolmente acido o debolmente basico.
A pH neutro, la disidratazione avviene a una velocità inferiore. Al contrario, condizioni fortemente acide o alcaline promuovono l’idratazione del PCA.
Le condizioni di cottura che si incontrano normalmente non determinano racemizzazione o disidratazione.
La concentrazione minima percettibile di glutammato di sodio è dello 0,03%, che è inferiore ai valori soglia del cloruro di sodio (0,2%) o del saccarosio (0,5%). L’attività di esaltazione del sapore del MSG aumenta sinergicamente in presenza di 5′-inosinato e 5′-guanilato.
L’acido L-glutammico è classificato come un amminoacido non essenziale e svolge un ruolo critico nel metabolismo dell’azoto degli amminoacidi. La glutammato deidrogenasi catalizza l’aminazione riduttiva del 2-ossoglutarato in L-glutammato per l’incorporazione di azoto inorganico.
Molti organismi possiedono una varietà di amminotransferasi che trasferiscono gruppi amminici dagli amminoacidi ai 2-ossoglutarato e molti di questi enzimi utilizzano la coppia glutammato/2-ossoglutarato come donatore/accettore di amminoacidi.
L-glutammato funge da precursore diretto per varie sostanze essenziali, tra cui L-glutammina, il neurotrasmettitore acido γ-amminobutirrico (GABA), γ-carbossiglutammato nelle proteine leganti il calcio e il tripeptide glutatione.
3. Utilizzi del glutammato monosodico
3.1. Condimento
Come condimento o esaltatore di sapore consolidato, il glutammato monosodico è ampiamente utilizzato per migliorare la gradevolezza degli alimenti. Il sapore caratteristico del glutammato monosodico, l’umami, lo distingue dagli altri quattro sapori di base: dolce, salato, acido e amaro.
Recenti progressi nella biologia molecolare hanno identificato le proteine che funzionano come recettori del gusto umami, che sono espressi in cellule specializzate delle papille gustative sulla lingua e attraverso la cavità orale.
I glutammati sono presenti in vari alimenti come latte umano, pomodori, formaggio, alghe, pesce, carni e verdure. Altre sostanze umami, come i 5′-ribonucleotidi come inosinato e guanilato, si trovano anche in carni, pesce e funghi secchi.
Il glutammato monosodico è efficace nell’esaltare il sapore di un’ampia varietà di alimenti, in particolare carni, frutti di mare, verdure, zuppe, stufati e zuppe di pesce.
Tuttavia, le bevande alcoliche, la frutta e i dolciumi non vengono migliorati dall’aggiunta di glutammato di sodio e il suo effetto sull’odore o l’aroma è trascurabile.
3.2. Usi industriali
L’acido glutammico viene utilizzato per applicazioni industriali, a seconda del pH. Ad esempio, l’arginina glutammato viene utilizzato come materia prima per prodotti farmaceutici e cosmetici.
L’acido glutammico cloridrato, prodotto dalla reazione dell’acido glutammico con l’acido cloridrico, viene utilizzato come acidificante gastrico.
Le proprietà elettrolitiche anfotere dell’acido glutammico vengono sfruttate in agenti chelanti, tamponi e builder per detergenti.
Il sale sodico dell’acido piroglutammico, ottenuto neutralizzando l’acido glutammico disidratato con idrossido di sodio, è molto igroscopico e viene utilizzato come componente di fattori idratanti naturali per la pelle umana e come umettante nei cosmetici.
Un polimero di metil glutammato funge da agente di rivestimento per la pelle sintetica.
Un condensato con formaldeide agisce come ritardante per l’intonaco.
Il composto N-acilato prodotto dalla reazione con un acido grasso a catena lunga è un tensioattivo anionico che è comunemente usato nei detergenti per la pelle e i capelli per la sua delicatezza e l’elevata sicurezza.
La dibutilamide di questo acido N-acilglutammico gelatinizza gli oli non polari e può essere usata come agente di recupero per l’olio marino versato.
Riferimento
- Monosodium Glutamate; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a16_711.pub2
