2-Metil-2-propanol: Propiedades, Producción y Usos
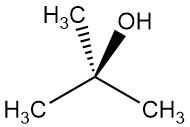
El 2-metil-2-propanol, también conocido como terc-butanol, es el alcohol terciario más simple con la fórmula química (CH3)3COH. Es un cristal sólido e incoloro a temperatura ambiente. Sin embargo, se derrite cerca de la temperatura ambiente (26 °C) para convertirse en un líquido viscoso con olor a alcanfor.
Tabla de contenido
1. Propiedades físicas del 2-metil-2-propanol
El 2-metil-2-propanol es un sólido incoloro a temperatura ambiente. Es completamente miscible con agua, etanol, éter dietílico y disolventes orgánicos comunes.
Las principales propiedades físicas características del 2-metil-2-propanol se presentan en la Tabla 1.
| Propiedad | Valor |
|---|---|
| Masa molar | 74,12 g/mol |
| Punto de fusión (p.f.) | 25,6 °C |
| Punto de ebullición (p.e.) | 82,55 °C |
| Densidad a 20 °C | 0,7867 g/cm³ |
| Índice de refracción a 20 °C | 1,3841 |
| Viscosidad a 20 °C | 5,5 mPa⋅s |
| Calor específico | 3,035 J g⁻¹ K⁻¹ |
| Calor de vaporización | 535,78 J/g |
| Calor de fusión | 91,61 J/g |
| Calor de combustión | 35,694 kJ/g |
| Presión crítica | 39,7 hPa |
| Temperatura crítica | 235 °C |
| Tensión superficial a temperatura ambiente. | 20,0 (25 °C) mN/m |
| Constante dieléctrica a temperatura ambiente. | 11.4 |
| Solubilidad en agua | miscible |
| Punto de inflamación | 11°C |
| Límites de ignición en el aire, % vol | 2,3 - 8 % |
| Temperatura de ignición | 470°C |
2. Reacciones químicas del 2-metil-2-propanol
El 2-metil-2-propanol se deshidrata fácilmente para formar 2-metilpropeno (isobuteno) con ácido sulfúrico diluido y calentamiento. Esta reacción no es importante industrialmente debido a la disponibilidad de 2-metilpropeno del petróleo craqueado.
No se puede deshidrogenar selectivamente debido a la división de moléculas en condiciones extremas.
El terc-butanol se puede utilizar en diversas reacciones de alquilación con amoníaco, aminas y compuestos aromáticos.
Se convierte en ésteres terc-butílicos con ácidos orgánicos e inorgánicos utilizando catalizadores ácidos, pero es menos reactivo que los alcoholes primarios y secundarios.
El 2-metil-2-propanol se desprotona con sodio o potasio metálico para producir el alcóxido correspondiente. El terc-butóxido de potasio es un ejemplo común de base no nucleofílica en química orgánica.
Elimina protones ácidos de sustratos básicos, pero su estructura voluminosa impide su participación en reacciones de sustitución nucleofílica como la síntesis del éter de Williamson o los procesos SN2.
El terc-butanol reacciona con cloruro de hidrógeno y ácido hipocloroso para producir cloruro de terc-butilo y hipoclorito de terc-butilo, respectivamente.

3. Producción de 2-Metil-2-propanol
El 2-metil-2-propanol se produce industrialmente mediante dos procesos principales:
- Hidratación con 2-metilpropeno
- Como subproducto de la producción de óxido de propileno y metil terc-butil éter
3.1. Producción de 2-metil-2-propanol mediante hidratación de 2-metilpropeno
El 2-metil-2-propanol se produce principalmente mediante la hidratación del 2-metilpropeno (isobuteno). Este proceso implica los siguientes pasos:

Preparación del reactivo: El isobuteno, la materia prima principal, a menudo se deriva del craqueo catalítico del petróleo o de la deshidrogenación del n-butano. El agua, que actúa como agente de hidratación, normalmente se suministra como agua purificada o se recicla de etapas anteriores. El propio terc-butanol puede estar presente en la materia prima o agregarse intencionalmente a la reacción.
Catálisis: las resinas de intercambio catiónico funcionalizadas con ácido sulfónico sirven como catalizadores preferidos debido a su alta actividad y selectividad hacia el formación de 2-metil-2-propanol y facilidad de regeneración. Las condiciones de reacción, incluida la temperatura (normalmente entre 30 y 120 °C) y la presión (atmosférica o ligeramente elevada), se controlan meticulosamente para optimizar la conversión y minimizar las reacciones secundarias indeseables.
Reacción y formación del producto: La reacción de hidratación, un proceso reversible, convierte el isobuteno y el agua en terc-butanol. A menudo se emplean reactores de múltiples etapas para utilizar eficientemente el catalizador y maximizar la conversión. El control preciso de las proporciones de reactivos, la temperatura y la carga de catalizador es crucial para garantizar una alta selectividad.
Separación del producto: la destilación separa eficazmente el producto de terc-butanol deseado del isobuteno sin reaccionar, los hidrocarburos inertes y el agua. El isobuteno y el agua que no han reaccionado se pueden reciclar nuevamente en el proceso para mejorar la eficiencia de los recursos.
3.2. Subproducto de la producción de óxido de propileno y metil terc-butil éter
El 2-metil-2-propanol se forma como un subproducto valioso en varios procesos industriales, particularmente aquellos que involucran óxido de propileno y metil terc-butil éter.
1. Producción de Óxido de Propileno:
Durante la fabricación de óxido de propileno a partir de 2-metilpropano (isobutano), se generan aproximadamente 1,2 toneladas de terc-butanol por tonelada de óxido de propileno producida. El proceso implica un paso intermedio en el que se forma hidroperóxido de t-butilo a partir de isobutano.
2. Procesamiento de metil terc-butil éter:
La división del metil terc-butil éter en 2-metilpropeno o 2-metil-2-propanol puro puede producir terc-butanol como subproducto. De manera similar, la síntesis de metil terc-butil éter con trazas de agua en la materia prima (metanol y olefinas C4) también genera t-BuOH como una sustancia no deseada. subproducto.
La presencia de t-BuOH como subproducto requiere pasos adicionales para la separación y purificación, lo que aumenta los costos de producción. Sin embargo, como ventaja, proporciona una fuente fácilmente disponible de 2-metil-2-propanol para aplicaciones posteriores, lo que minimiza la dependencia de métodos de producción dedicados y mejora la eficiencia del proceso.
Aunque no se utiliza comercialmente, el terc-butanol también se puede producir mediante la reacción de Grignard haciendo reaccionar acetona con cloruro de metilmagnesio.
4. Usos del 2-Metil-2-propanol
En comparación con otros butanoles, el 2-metil-2-propanol (t-BuOH) tiene una participación menor en el consumo mundial. Sin embargo, su uso ha aumentado constantemente desde 1990 antes de estabilizarse en los últimos años.
- El 2-metil-2-propanol encuentra su uso principal como disolvente debido a sus propiedades favorables, incluida la miscibilidad con agua y compuestos orgánicos.
- El terc-butanol se utiliza como reactivo para introducir el grupo terc-butilo en moléculas orgánicas. Esta modificación se emplea en diversas aplicaciones, como la síntesis de resinas solubles en aceite (p. ej., terc-butilfenol) y antioxidantes (p. ej., trinitro-terc-butiltolueno).
- También es un importante material de partida para la producción de peróxidos orgánicos, que sirven como catalizadores de polimerización esenciales en diversos procesos industriales.
- El 2-metil-2-propanol compite con el 2-propanol como aditivo en la gasolina para evitar la formación de hielo en el carburador. Su éter metílico surgió brevemente como refuerzo del octanaje y sustituto del plomo en las décadas de 1980 y 1990, experimentando un aumento significativo en su consumo (de 0,17 a 19 millones de toneladas entre 1982 y 1997). Sin embargo, las preocupaciones medioambientales llevaron a su eventual sustitución por la mezcla directa de bioetanol con gasolina.
5. Toxicología del 2-metil-2-propanol
2-Metil-2-propanol (t-BuOH) exhibe una toxicidad aguda relativamente baja. Los valores de LD50 más bajos documentados son 2740 mg/kg (oral, ratas) y 2000 mg/kg (cutánea, conejos).
Efectos de la exposición:
- Agudo: En niveles altos de exposición, el terc-butanol tiene un efecto narcótico, caracterizado por dolor de cabeza, náuseas, fatiga y mareos.
- Piel: El contacto prolongado con 2-metil-2-propanol en conejos no causó irritación de la piel. En humanos, puede producirse un ligero eritema e hiperemia tras el contacto con la piel.
- Tiene un olor distintivo y desagradable.
Límites de exposición:
- Valor límite umbral (TLV): 100 ppm (promedio ponderado en el tiempo), 150 ppm (límite de exposición a corto plazo).
- Valor MAK (Concentración máxima en el lugar de trabajo): 20 ml/m³.
- TRGS 900 (Regelwerk técnico alemán para sustancias peligrosas): 20 ml/m³.
Referencias
- Butanols; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a04_463.pub3
- Process for production of tertiary butyl alcohol. – https://patents.google.com/patent/US4307257A/en
- Process for the preparation of tert-butanol. – https://patents.google.com/patent/EP1431264A1/en
- https://en.wikipedia.org/wiki/Tert-Butyl_alcohol
