2-Metil-1-propanol: Propiedades, Producción y Usos
El 2-Metil-1-propanol, también conocido como isobutanol o alcohol isobutílico, es un compuesto orgánico con la fórmula química (CH3)2CHCH2OH. Es un líquido incoloro con un olor característico que se encuentra tanto en productos naturales como en aceites de fusel.
El isobutanol es un producto de la fermentación de la melaza (que comprende aproximadamente el 74% del contenido total de alcohol). Históricamente, el isobutanol se aislaba de los aceites de fusel. Sin embargo, el desarrollo de la síntesis de aceite de isobutilo, un proceso análogo a la síntesis de metanol a partir de monóxido de carbono e hidrógeno, permitió la producción a gran escala.
En la década de 2010, se produjo un cambio significativo: la hidroformilación de propileno (oxosíntesis) se convirtió en el método de producción dominante actual debido a su eficiencia y rentabilidad. Esto ha llevado a un aumento significativo en el tamaño del mercado de isobutanol.
Tabla de contenido
1. Propiedades físicas del 2-metil-1-propanol
El 2-metil-1-propanol (isobutanol) es un líquido incoloro con un olor característico. Sus vapores irritan las mucosas y pueden tener un efecto narcótico en concentraciones elevadas. Este alcohol es miscible con disolventes orgánicos comunes.
La Tabla 1 resume las propiedades físicas clave del 2-metil-1-propanol:
| Propiedad | Valor |
|---|---|
| Masa molar | 74,12 g/mol |
| Punto de fusión (pf) | -107,9 °C |
| Punto de ebullición (pb) | 107,9 °C |
| Densidad a 20°C (d20) | 0,8027 g/mL |
| Índice de refracción a 20°C (n20) | 1,3959 |
| Viscosidad a 20°C | 4,0 mPa·s |
| Calor específico (30-80°C) | 2.5263 J·g-1·K-1 |
| Calor de vaporización | 578,83 J/g |
| Calor de combustión | 35,981 kJ/g |
| Presión crítica | 48hPa |
| Temperatura crítica | 265 °C |
| Tensión superficial (temperatura ambiente) | 23,0 mN/m |
| Constante dieléctrica (temperatura ambiente) | 18.8 |
| Número de evaporación (éter = 1) | 24 |
| Solubilidad en agua |
20°C: 8,5% en peso 30°C: 7,5% en peso |
| Solubilidad del agua en isobutanol |
20°C: 15% en peso 30°C: 17,3% en peso |
| Punto de inflamación | 28 °C |
| Límites de ignición en el aire | 1,7-10,9% vol. |
| Temperatura de ignición | 430°C |
2. Propiedades químicas del 2-metil-1-propanol
2.1. Deshidratación
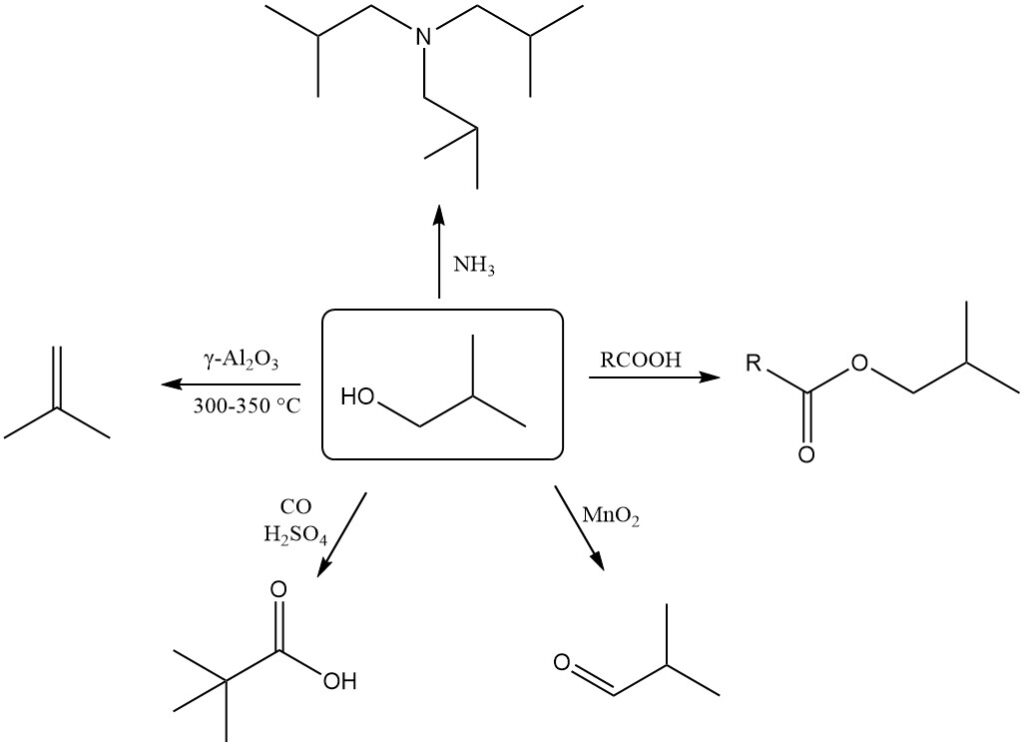
El 2-metil-1-propanol se deshidrata fácilmente para formar 2-metilpropeno (isobuteno). Esta reacción requiere un catalizador de γ-Al2O3 a 300-350°C y logra una conversión casi cuantitativa con más del 90% de selectividad para el isobuteno.
2.2. Oxidación
El 2-metil-1-propanol se puede deshidrogenar a 2-metilpropanal (isobutanal) utilizando agentes oxidantes como dióxido de manganeso o catalizadores adecuados a temperaturas más altas.
La reacción de Koch-Haaf convierte 2-metil-1-propanol en ácido trimetilacético en presencia de monóxido de carbono y ácido sulfúrico con un alto rendimiento (89%).
La oxidación del isobutanol con dicromato en presencia de ácido sulfúrico produce ácido isobutírico.
2.3. Alquilación
El 2-metil-1-propanol se puede utilizar para reacciones de alquilación con amoníaco o aminas para formar diversas alquilaminas.
2.4. Esterificación
El 2-metil-1-propanol reacciona con ácidos inorgánicos y orgánicos en presencia de catalizadores para formar ésteres de isobutilo, así como con cloruros y anhídridos de ácido.
3. Producción de 2-Metil-1-propanol
Tres procesos industriales importantes para producir 2-metil-1-propanol (isobutanol) son los siguientes:
- Hidroformilación de propeno (síntesis oxo)
- Hidrogenación catalítica de monóxido de carbono
- Reacción de homologación
3.1. Hidroformilación de propeno (síntesis oxo)
La oxosíntesis es el método más eficiente y rentable para la producción a gran escala de isobutanol. Implica hacer reaccionar propeno con gas de síntesis (una mezcla de monóxido de carbono e hidrógeno) a alta presión y temperatura, utilizando un catalizador adecuado como complejos de rodio o cobalto-carbonilo.
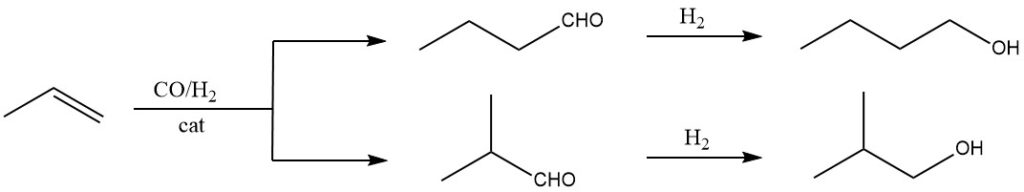
Forma una mezcla de alcoholes (1-butanol y 2-metil-1-propanol). Este es actualmente el método dominante para la síntesis de isobutanol debido a su alta eficiencia, rentabilidad y materiales de partida fácilmente disponibles.
Para obtener más información, consulte el artículo sobre el 1-butanol.
3.2. Hidrogenación catalítica de monóxido de carbono
Si bien la síntesis de metanol basada en CO-H2 logró un éxito comercial en la década de 1920, los procesos análogos para alcoholes superiores enfrentaron una adopción limitada. A pesar de la promesa inicial, estos procesos han desaparecido en gran medida del panorama industrial.
Entre estos intentos históricos, la síntesis de aceite de isobutanol de BASF tiene una importancia especial. Este proceso utilizó un catalizador de síntesis de metanol modificado con KOH a alta presión (30 MPa) y temperatura elevada (430 °C) para convertir CO y H2 en una mezcla de productos que contenía aproximadamente 50 % de metanol, 11-14 % de 2-metil-1- propanol (isobutanol) y otros componentes.
Sin embargo, BASF abandonó la síntesis de aceite de isobutanol en 1952 cuando surgieron alternativas más económicas. Las rutas de oxosíntesis y petroquímica ofrecieron una eficiencia y rentabilidad superiores tanto para el isobutanol como para su valioso producto secundario, el 2-metilpropeno.
3.3. Reacción de homologación
Este proceso implica extender la cadena de carbono de un alcohol más corto, como metanol, etanol o alcano, para producir isobutanol. Si bien son técnicamente posibles, las reacciones de homologación adecuadas para la producción de isobutanol no son muy eficientes ni comercialmente viables en comparación con la hidroformilación de propeno.
Los intentos de lograr la producción directa de butanol a partir de metanol y etanol fácilmente disponibles mediante reacciones de homologación no han arrojado resultados significativos. A pesar de los intensos esfuerzos de investigación, sólo se ha obtenido isobutanol en pequeñas cantidades como subproducto.
Otros procesos incluyen la hidratación de 2-metilpropeno con ácido sulfúrico al 65% para formar isobutanol.

4. Usos del 2-Metil-1-Propanol
El 2-metil-1-propanol a menudo se compara con el 1-butanol debido a sus aplicaciones similares y encuentra uso en diversas industrias debido a su menor costo y propiedades únicas.
Disolventes y aditivos:
- Sustituto rentable del 1-butanol: el 2-metil-1-propanol sirve como disolvente, diluyente y aditivo en nitrocelulosa y resinas sintéticas, agentes de limpieza y tintas de impresión.
- Compatibilidad con resinas: Es capaz de disolver resinas cetónicas, resinas de ftalatos, resinas de urea y resinas de melamina-formaldehído y se utiliza comercialmente, aunque es menos eficaz como disolvente para resinas de fenol-formaldehído en comparación con el 1-butanol.
Ésteres:
- Acetato de isobutilo: este éster se utiliza como disolvente para grasas, caucho clorado, poliestireno y resinas de cumarona.
- plastificantes: ésteres de los ácidos ftálico, adípico y dicarboxílico, así como el éster del ácido fosfórico del 2-metil-1-propanol, encuentran uso como plastificantes, particularmente para el PVC y sus copolímeros y para los derivados de la celulosa.
- Ésteres del ácido clorofenoxiacético: Los ésteres isobutílicos de los ácidos 2,4-dicloro y 2,4,5-triclorofenoxiacético tienen actividad herbicida.
Otras aplicaciones:
- Anticongelante de gasolina: el 2-metil-1-propanol posee propiedades anticongelantes en la gasolina.
- Extracción de fosfato de amonio: su uso como agente de extracción en la recuperación de fosfato de amonio aumenta su versatilidad.
5. Toxicología del 2-metil-1-propanol
El 2-metil-1-propanol muestra una toxicidad oral y dérmica aguda baja pero una toxicidad acuática moderada. Los efectos incluyen irritación de ojos y piel.
Toxicidad aguda:
- Baja toxicidad oral: la LD50 en ratas es 2460 mg/kg (la más baja publicada).
- Baja toxicidad dérmica: la LD50 en conejos es 3400 mg/kg.
- Toxicidad acuática moderada: la CL50 para peces es 1330 mg/L (96 h).
- Se observó narcosis en ratones con una alta exposición por inhalación (6400 ppm).
Efectos locales:
- Irritación ocular de moderada a grave en conejos.
- Irritación moderada de la piel en conejos (exposición de 24 horas).
Efectos crónicos:
- Estudios a largo plazo sugieren posible carcinogenicidad en ratas (datos limitados).
- Mutagénico en la bacteria E. coli.
Exposición humana:
- No se observa irritación ocular en humanos con una exposición por inhalación baja (100 ppm).
- La exposición a vapores mixtos (acetato de butilo y 2-metil-1-propanol) provocó queratitis vacuolar en los trabajadores (el agente causante no está claro).
- La aplicación cutánea provocó un ligero eritema e hiperemia en humanos.
Límites de exposición:
- TLV (Valor límite umbral): 50 ppm (TWA), 75 ppm (STEL) [ACGIH]
- MAK (Concentración máxima permitida): 100 ml/m³ [Alemania]
- TRGS 900 (límite de exposición laboral): 100 ml/m³ [Alemania]
Referencia
- Butanoles; Enciclopedia de química industrial de Ullmann. – https://onlinelibrary.wiley.com/doi/10.1002 /14356007.a04_463.pub3
