Pyrogallol: Herstellung, Reaktionen und Verwendungen

Pyrogallol, auch Pyrogallussäure genannt, wurde erstmals 1786 von SCHEELE durch Trockendestillation von Gallussäure (3,4,5-Trihydroxybenzoesäure) entdeckt. Pyrogallol-Derivate kommen natürlicherweise in mehreren Verbindungen vor, darunter Tannin, Anthocyan und Alkaloide.
Pyrogallol liegt in Form farbloser Nadeln oder Blättchen vor, die sich bei Einwirkung von Luft oder Licht allmählich dunkelgrau verfärben.
Inhaltsverzeichnis
1. Herstellung von Pyrogallol
Pyrogallolis wird kommerziell durch Decarboxylierung von Gallussäure hergestellt, die durch Hydrolyse von Tannin hergestellt wird.
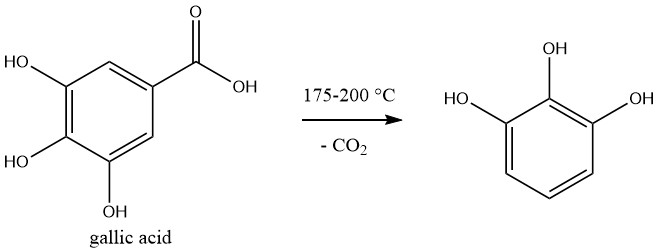
Die Reaktion wird diskontinuierlich durchgeführt. Eine 50 %ige wässrige Gallussäurelösung wird in einem Autoklaven auf 175–200 °C erhitzt und der Druck steigt während der Reaktion auf 1,2 MPa.
Nach Beendigung der Kohlendioxidentwicklung wird die Lösung abgekühlt. Die Reaktion verläuft quantitativ.
Nach Entfärbung des Reaktionsgemisches mit Aktivkohle wird ein Rohprodukt erhalten, das durch Sublimation oder Vakuumdestillation gereinigt wird.
Die Kosten für die Gewinnung von Pyrogallol sind relativ hoch, da der Ausgangsstoff Gallussäure aus einem Naturprodukt stammt, das nur begrenzt verfügbar ist. Daher wurde nach alternativen Methoden zur Herstellung von Gallussäure gesucht.
Basenkatalysierte Kondensation von Trimethylpropan-1,2,3-tricarboxylat mit dem Dimethylketal von Mesoxalsäure, gefolgt von Hydrolyse und Decarboxylierung, liefert Gallussäure in 74 % Ausbeute. Die Reaktion des Ketals und des Glutarsäureesters ergibt Pyrogallol, ohne dass Gallussäure entsteht.
Es wurden auch verschiedene andere Methoden zur Herstellung von Pyrogallol entwickelt, beispielsweise die Oxidation von Resorcin mit Wasserstoffperoxid, die Hydrolyse von 2,6-Diamino-4-butylphenol, die Demethylierung von 4-substituierten 2,6-Dimethoxyphenolen und die Oxidation von 2,6- Dimethylphenol, Hydrolyse von 2,2,6,6-Tetrachlorcyclohexanon, Desoximierung von 1,2,3-Cyclohexantrion-1,3-dioxim und Dehydrierung von 1,2,3-Trihydroxycyclohexan.
2. Chemische Reaktionen von Pyrogallol
Pyrogallol, ein Polyphenol, gilt als das stärkste Reduktionsmittel. Seine wässrige Lösung absorbiert schnell gasförmigen Sauerstoff und fällt eine dunkelbraune Substanz aus.
Aufgrund dieser Eigenschaft wird Pyrogallol häufig zur quantitativen Bestimmung von Sauerstoff eingesetzt.
Das chemische Verhalten von Pyrogallol ist vergleichbar mit dem von Phenolen. Mono-, di- und trisubstituierte Produkte können durch traditionelle Methoden wie Veresterung und Veretherung der Hydroxygruppen synthetisiert werden.
Beim Erhitzen mit wässrigem Kaliumbicarbonat ergibt Pyrogallol überwiegend Pyrogallol-4-carbonsäure (2,3,4-Trihydroxybenzoesäure), wobei Gallussäure als Nebenprodukt entsteht.
Pyrogallol kann eine Formylierung, Acylierung und Mannich-Reaktion eingehen, um als Primärprodukt 4-substituierte Cyclohexenonen zu bilden.
Die Bromierung mit Brom führt schließlich zu 1,2,6,6-Tetrabromcyclohexen-3,4,5-trion. Die Reaktion mit Phosgen ergibt Pyrogallolcarbonat und mit Thionylbromid entsteht 4,5,6-Tribrompyrogallol.
Die quantitative Analyse von Schwermetallionen erfolgt über die hochempfindlichen Farbreaktionen der wässrigen Pyrogallollösung mit ihnen. Edelmetallionen (z. B. Ag+, Au2+, Hg2+) werden zu elementaren Metallen reduziert.
Ein Katalysator für die alternierende Polymerisation von Kohlendioxid und Propylenoxid entsteht durch einen Komplex aus Diethylzink und Pyrogallol.
3. Verwendung von Pyrogallol
Pyrogallol ist eine vielseitige Verbindung, die in der Fotografie, Lithographie und Haarfärbetechnik Verwendung findet und in verschiedenen Anwendungen als Antioxidans und Stabilisator eingesetzt wird.
Der Einsatz von Pyrogallol im Kosmetik- und Arzneimittelbereich ist in jüngster Zeit zurückgegangen, was auf seine erhebliche Toxizität zurückzuführen ist.
Referenz
- Phenol Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a19_313
