2-Chlorphenol
2-Chlorphenol, auch ortho-Chlorphenol genannt, ist eine aromatische Verbindung, bei der Phenol durch ein Chloratom in ortho-Position ersetzt ist. Es ist eine Flüssigkeit mit der chemischen Formel C6H4ClOH und einem starken, unangenehmen Geruch.
Inhaltsverzeichnis
1. Physikalische Eigenschaften von 2-Chlorphenol
2-Chlorphenol ist eine farblose bis bernsteinfarbene Flüssigkeit (handelsübliche Proben können einen gelben Farbton aufweisen) mit einem starken, durchdringenden Geruch. Es ist in Wasser löslich und in Alkoholen, Ethern und Alkalilösungen gut löslich, da es eine schwache Säure ist. Wichtige physikalische Eigenschaften von 2-Chlorphenol sind in Tabelle 1 aufgeführt.
| Eigenschaft | Wert |
|---|---|
| CAS-Nummer | [95-57-8] |
| Molekulargewicht | 128,56 g/mol |
| Schmelzpunkt | 8,7 °C |
| Siedepunkt | 174,5 °C |
| pKa | 8,52 |
| Dichte bei 20 °C | 1,263 |
| Spezifische Wärme bei 20 °C, J.mol-1K-1 | 177 |
| Bildungswärme bei 50 °C, kJ/mol | 185 |
| Dampfdruck bei 25°C | 2,53 mmHg |
| Viskosität bei 50 °C, mPa.s | 2 |
| Brechungsindex | 1,55 |
| Löslichkeit in Wasser bei 20 °C | 28,5 g/L |
| Flammpunkt (geschlossener Tiegel) | 121 °C |
2. Chemische Reaktionen von 2-Chloophenol
2-Chlorphenol ist aufgrund der Reaktivität sowohl der Hydroxylgruppe als auch des aromatischen Rings ein wertvolles Ausgangsmaterial in verschiedenen chemischen Synthesen. Es ist sowohl an elektrophilen als auch nukleophilen Substitutionen und Oxidationsreaktionen beteiligt.
2.1. Reaktivität der Hydroxylgruppe
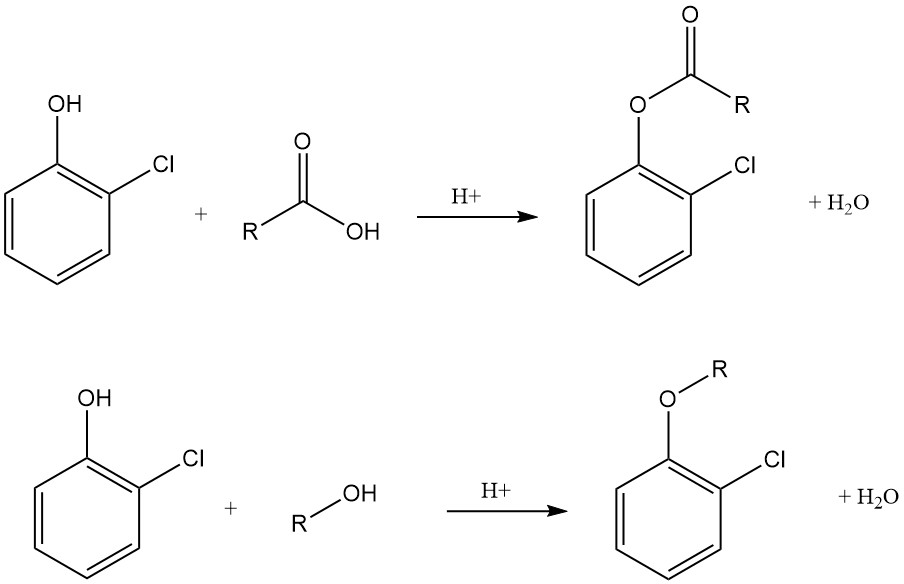
Im Vergleich zu Phenol ist 2-Chlorphenol saurer und bildet mit Alkali- und Erdalkalimetallhydroxiden, -carbonaten oder -aminen stabile und wasserlösliche Salze. Es bildet leicht Ester mit organischen und anorganischen Säuren, einschließlich des weit verbreiteten 2-Chlorphenylphosphats, Carbamats, Chlorformiats, Carbonats und Laurats.
2-Chlorphenol wird einer O-Alkylierung unterzogen, um eine Vielzahl von Ethern zu erzeugen, die aus aliphatischen, aromatischen und heterozyklischen Verbindungen abgeleitet sind.
2.2. Elektrophile aromatische Substitution
Das Vorhandensein eines Chloratoms am aromatischen Ring von 2-Chlorphenol erleichtert elektrophile Substitutionsreaktionen. Daher kann es an Standardreaktionen wie Alkylierung, Acylierung, Nitrierung, Sulfonierung, Halogenierung, Carboxylierung und Kondensation mit Aldehyden wie Formaldehyd, Chloral und Glyoxylsäure teilnehmen.
2.3. Nukleophile aromatische Substitution
Die nukleophile Substitution des Chloratoms in 2-Chlorphenol wird immer noch in der chemischen Synthese eingesetzt, hauptsächlich zur Herstellung von Brenzcatechin durch Reaktion mit Natriumhydroxid. 2-Chlorphenol reagiert auch mit Ammoniak unter Bildung von 2-Aminophenol.
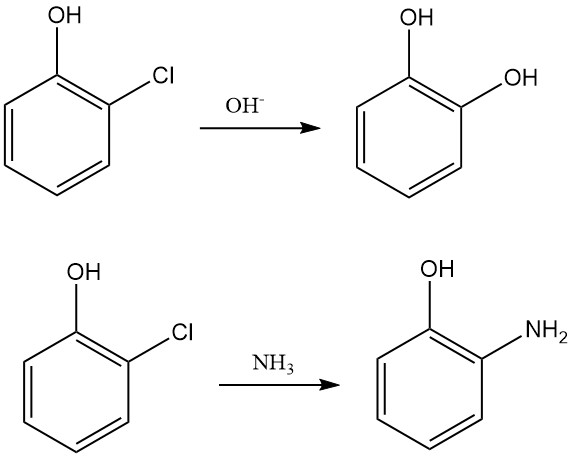
Dieser Reaktionstyp ist besonders nützlich für die Herstellung verschiedener substituierter Diphenylether, die wirksame Herbizide sind.
2-Chlorphenol kann durch Reaktion mit Chlor in wässriger Essigsäure in polychlorierte alicyclische Ketone wie „Hexachlorphenol“ (ein Pestizid) umgewandelt werden. In Gegenwart eines sauren Katalysators wie Schwefelsäure hydrolysiert Hexachlorphenol zu Chloranil.
2.4. Oxidation
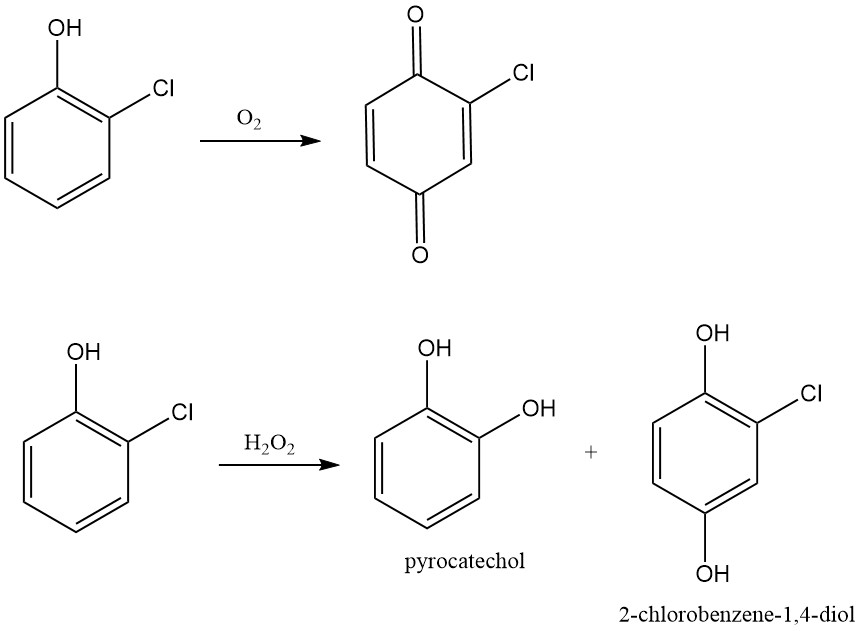
Ähnlich wie andere Phenole unterliegt auch 2-Chlorphenol einer Oxidation. Luftoxidation führt zur Bildung von 2-Chlorchinon, während Wasserstoffperoxidoxidation die entsprechenden chlorierten Diphenole erzeugt. Die peroxidvermittelte Oxidation von 2-Chlorphenol mit Perpropionsäure in Benzol bei 80 °C ergibt Chlordiphenole (3-Chlorcatechol und Chlorhydrochinon) mit einer Ausbeute von 85 %.
3. Herstellung von 2-Chlorphenol
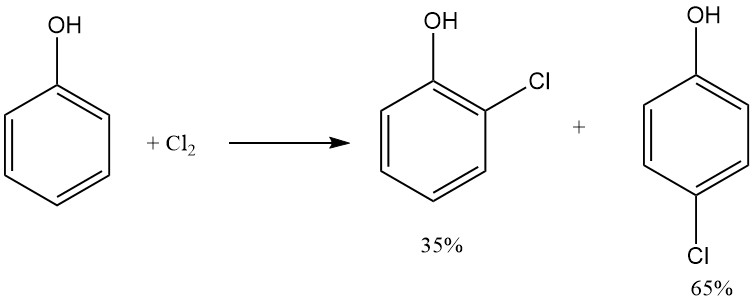
2-Chlorphenol wird durch direkte Chlorierung von geschmolzenem Phenol mit Chlorgas hergestellt. Dieser Prozess ergibt eine Mischung aus ortho- und para-Monochlorphenol mit 2-Chlorphenol zu 35 % und 4-Chlorphenol zu 65 % und ist nahezu temperaturunabhängig.
Um die Ausbeute an 2-Chlorphenol zu erhöhen, können folgende Modifikationen am Chlorierungsreagenz oder am Reaktionsmedium vorgenommen werden:
- Lösungsmittel: Aprotische unpolare Lösungsmittel wie Hexan, Tetrachlorkohlenstoff und Dichlorethan fördern die Bildung von 2-Chlorphenol.
- Temperatur und Konzentration: Höhere Temperaturen und niedrigere Phenolkonzentrationen begünstigen das Ortho-Isomer.
- Chlorierungsmittel: Bestimmte Reagenzien wie Diisopropylamin (0,01 Gew.-% in Perchlorethylen, 110 °C) ergeben ein sehr hohes O/P-Verhältnis ( 15).
- Die Chlorierung von Phenol mit Natriumhypochlorit (pH 10), Tert-Butylhypochlorit, Alkaliphenolaten in wasserfreien Medien und Chlor in Essigsäure mit Essigsäureanhydrid begünstigt die Bildung von 2-Chlorphenol.
4. Verwendung von 2-Chlorphenol
2-Chlorphenol wird derzeit nur begrenzt eingesetzt, da sicherere und wirksamere Alternativen verfügbar sind. Es gibt jedoch einige historische und potenzielle Anwendungen.
In der Vergangenheit wurde 2-Chlorphenol aufgrund seiner bakteriziden und keimtötenden Eigenschaften als Desinfektionsmittel eingesetzt. Seine potenziellen Gesundheitsrisiken führten jedoch dazu, dass es in den meisten Desinfektionsanwendungen nicht mehr eingesetzt wird.
Heutzutage wird 2-Chlorphenol hauptsächlich als Zwischenprodukt bei der Herstellung anderer Chemikalien verwendet. Es dient als Ausgangsmaterial für die Synthese verschiedener Verbindungen, darunter:
- Herbizide: Bestimmte Phenoxyherbizide wie Dichlorphenoxyessigsäure (2,4-D) können unter Verwendung von 2-Chlorphenol als Vorstufe hergestellt werden.
- Farbstoffe: Einige Farbstoffe, insbesondere Azofarbstoffe, verwenden 2-Chlorphenol als Ausgangsmaterial für ihre Synthese.
- Höher chlorierte Phenole, Catechol und Profenofos.
Derzeit wird an der Erforschung möglicher neuer Anwendungen für 2-Chlorphenol geforscht, insbesondere in Bereichen wie der Entwicklung neuer Fungizide oder Insektizide, der Produktion biobasierter Polymere und der Gewinnung von Schwefel- und Stickstoffverbindungen aus Kohle.
5. Toxikologie von 2-Chlorphenol
2-Chlorphenol weist eine erhebliche Toxizität auf und verursacht bei der Exposition verschiedene schädliche Wirkungen.
Hohe Dosen von 2-Chlorphenol lösen Krämpfe aus, die oft durch äußere Reize wie Berührung oder Geräusche ausgelöst werden. Weitere Symptome sind Unruhe, schnelles Atmen (Polypnoe), Muskelschwäche, Atemnot (Dyspnoe) und Koma, die möglicherweise zum Tod führen können. Wiederholte Exposition gegenüber toxischen Konzentrationen schädigt vor allem die Leber und die Nieren.
Bei Ratten betragen die oralen und perkutanen LD50-Werte 670 mg/kg bzw. 950 mg/kg.
Die Forschung zur Elimination und Metabolisierung von 2-Chlorphenol ist noch nicht schlüssig. Studien deuten darauf hin, dass Hunde es hauptsächlich im Urin ausscheiden, sowohl in freier als auch in konjugierter Form (87 %). Umgekehrt scheinen Kaninchen 2-Chlorphenol vor der Ausscheidung in Chlorbenzol umzuwandeln.
Derzeit gibt es keine Berichte über chronische Gesundheitsschäden bei Menschen, die niedrigen Dosen von 2-Chlorphenol ausgesetzt waren.
Referenzen
- Chlorophenols; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a07_001.pub2
- https://pubchem.ncbi.nlm.nih.gov/compound/2-Chlorophenol
