Crotonaldehyde: eigenschappen, reacties, productie en toepassingen
Wat is crotonaldehyde?
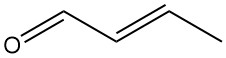
Crotonaldehyde [4170-30-3], ook bekend als 2-butenal, is een kleurloze vloeistof met een scherpe geur en sterke traanvorming. Het heeft een chemische formule van CH3CH=CHCHO en bestaat als twee stereo-isomeren: cis-crotonaldehyde [15798-64-8] en trans-crotonaldehyde [123-73-9].
Commercieel verkrijgbare crotonaldehyde bevat een mengsel van beide isomeren, waarbij de trans-isomeer de dominante vorm is (>95%) vanwege de grotere thermodynamische stabiliteit.
Crotonaldehyde komt van nature voor in verschillende planten en plantaardige producten, waaronder sperziebonen, koolzaadolie en sojaolie.
Inhoudsopgave
| Eigenschap | Waarde |
|---|---|
| Moleculaire massa | 70,09 g/mol |
| Kookpunt | 102,2 °C |
| Smeltpunt | -76 °C |
| Dichtheid (20 °C) | 0,852 g/cm3 |
| Breukindex (n20D) | 1,438 |
| Verdampingswarmte | 515 J/g |
| Crotonaldehyde-waterazeotroop | 24,8 gew.% H2O |
| Kookpunt azeotroop | 84 °C |
| Oplosbaarheid in water (20 °C) | 181 g/l |
| Oplosbaarheid van water in crotonaldehyde (20 °C) | 9,5 g/100 g |
| Dampspanning (bij 20 °C) | 4,3 kPa |
| Vlampunt | 13 °C |
| Zelfontbrandingstemperatuur | 165 °C |
| Explosiegrenzen in lucht |
Onder: 2,1 vol% Boven: 15,5 vol% |
2. Chemische reacties van crotonaldehyde
Crotonaldehyde is zeer reactief vanwege de aanwezigheid van zowel een carbonylgroep als een koolstof-koolstof dubbele binding in zijn structuur. Verontreiniging met sterke zuren of alkaliën initieert gemakkelijk exotherme condensatiereacties.
Blootstelling aan sterke zuren katalyseert de dimerisatie van crotonaldehyde tot dicrotonaldehyde (5,6-dihydro-2,6-dimethyl-2H-pyran-3-carboxaldehyde).
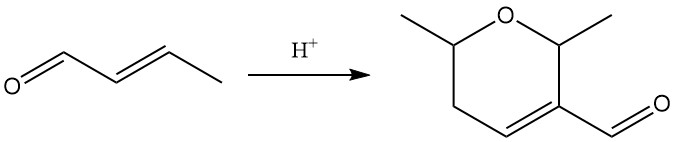
De primaire reacties van crotonaldehyde omvatten hydrogenering, reductie, oxidatie en additie.
Zowel de carbonylgroep als de C-C dubbele binding kunnen reductie ondergaan. Katalytische hydrogenering, doorgaans met nikkel- of koperkatalysatoren, biedt de meest economische aanpak.
Selectieve hydrogenering van de olefinische groep bij lagere reactietemperaturen en -drukken was een proces dat vroeger werd gebruikt voor de productie van n-butanal. Momenteel is hydroformylering van propeen de voorkeursmethode voor butyraldehydesynthese.
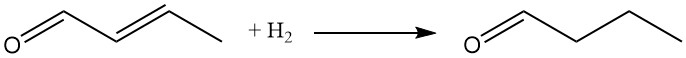
De hydrogenering van beide functionele groepen produceert n-butanol, dat tegenwoordig vaak wordt geproduceerd via n-butyraldehydehydrogenering.
Selectieve katalytische hydrogenering bij de carbonylgroep leidt tot crotylalcohol (CH3CH=CHCH2OH).

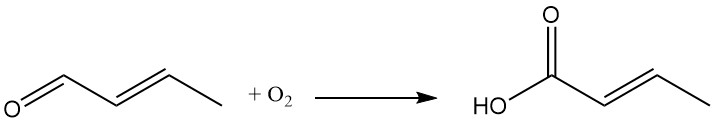
De oxidatie van crotonaldehyde resulteert in de vorming van crotonzuur.
De toevoeging van verschillende moleculen over de dubbele binding van crotonaldehyde maakt het een waardevol chemisch intermediair. Bijvoorbeeld, de toevoeging van alcoholen of thiolen aan de olefinische dubbele binding, gekatalyseerd door een basische katalysator, is belangrijk voor de synthese van 3-alkoxybutyraldehyden.
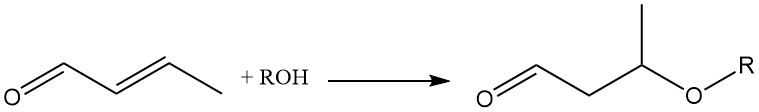
Door de toevoeging van methanol aan crotonaldehyde ontstaat het intermediair 3-methoxybutyraldehyde, dat achtereenvolgens hydrogenering en verestering ondergaat om speciale oplosmiddelen te produceren zoals 3-methoxybutanol (1) en 3-methoxybutylacetaat (2).

Crotonaldehyde kan ook worden gebruikt als een diënofiel in Diels-Alder-reacties.
3. Productie van Crotonaldehyde
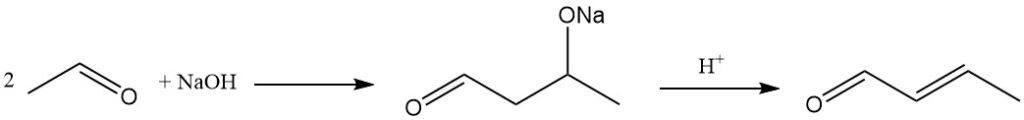
De dominante industriële methode voor de productie van crotonaldehyde is de aldolcondensatie van aceetaldehyde, gevolgd door dehydratatie van de resulterende aldol en daaropvolgende destillatie. Dit proces levert een product op met een zuiverheid van ongeveer 99%.
De aldolisatiereactie kan worden gekatalyseerd door een breed scala aan basische katalysatoren, waaronder alkali- of aardalkalimetaalkatalysatoren, ammoniumzouten, zeolieten, moleculaire zeven en kleiachtige materialen.
Azijnzuur, minerale zuren of zure kationenuitwisselingsharsen worden gebruikt als katalysatoren voor de dehydratatiestap die aldol omzet in crotonaldehyde.
Celanese Chemicals en Daicel zijn belangrijke commerciële producenten van crotonaldehyde. Een vereenvoudigde continue crotonaldehydeproductie-eenheid wordt geïllustreerd in Figuur 1.
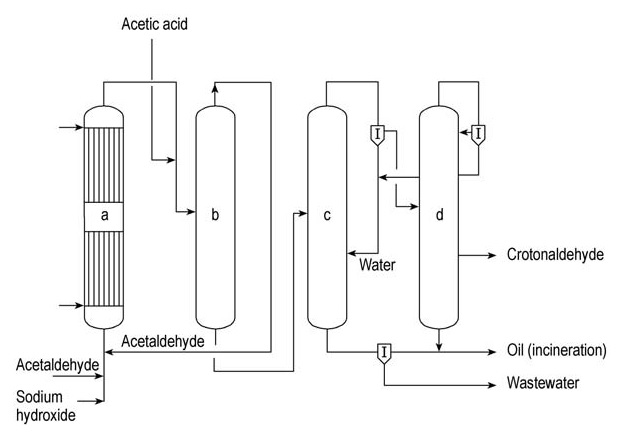
a) Aldolreactor; b) Acetaldehydestripkolom; c) Azeotroopdestillatiekolom; d) Rectificatiekolom
In dit proces ondergaat aceetaldehyde aldolisatie in een watergekoelde aldolreactor (a) met een waterige oplossing van natriumhydroxide als katalysator. Het product wordt vervolgens geneutraliseerd met azijnzuur voordat het in een stripkolom (b) wordt gevoerd.
Niet-gereageerde aceetaldehyde wordt boven in deze kolom teruggewonnen en teruggevoerd naar de aldolreactor (a). Het onderste product van kolom (b), de intermediaire aldol, wordt in de azeotroopdestillatiekolom (c) gevoerd. Hier ondergaat de aldol dehydratie en wordt de crotonaldehyde-waterazeotroop gedestilleerd.
Deze azeotroop wordt vervolgens gescheiden in water en een waterige crotonaldehydefase die ongeveer 10% water bevat. Het water wordt teruggevoerd naar de azeotroopkolom (c), waar het als bodemproduct naar buiten komt.
De waterige crotonaldehydestroom wordt vervolgens naar de rectificatiekolom (d) gevoerd, waar een andere crotonaldehyde-waterazeotroop wordt gevormd en boven het hoofd naar buiten komt. Deze azeotroop wordt gescheiden in water, dat wordt teruggevoerd naar de azeotroopkolom (c), en waterige crotonaldehyde, dat wordt teruggevoerd naar de rectificatiekolom (d).
Zuivere crotonaldehyde wordt verkregen als een zijstroom uit deze kolom.
Zware fracties worden verwijderd uit de bodem van de kolom (d) en gecombineerd met organische residuen uit de azeotroopkolom (c) voordat ze worden verbrand. Afvalwater dat uit kolom (c) wordt gegenereerd, wordt behandeld in een speciale afvalwaterzuiveringsinstallatie.
Alternatieve productiemethoden
Hoewel de aldolcondensatie van aceetaldehyde de dominante industriële methode blijft, zijn alternatieve technologieën onderzocht. Eén methode is de oxidatie van butadieen tot zijn mono-epoxide, gevolgd door isomerisatie tot crotonaldehyde.
Dit proces vertoont enige overeenkomsten met het Wacker-Hoechst-proces voor de productie van aceetaldehyde uit ethyleen. Het gebruik van paraldol als alternatief voor aldol voor de productie van cosmetische 1,3-butyleenglycol lijkt echter veelbelovender dan de toepassing ervan in de synthese van crotonaldehyde.
Andere methoden, zoals de katalytische oxidatie van olefinen, dehydrogenering van allylalcohol met aminen, hydratatie van acetyleen in de dampfase en enzymatische oxidatie van 2-buteen, hebben geen praktisch belang bereikt voor de productie van crotonaldehyde.
Crotonaldehyde kan ook worden gevormd als bijproduct tijdens de synthese van 1,3-butyleenglycol en bij de productie van azijnzuur via methanolcarbonylering. Bovendien genereren onvolledige verbrandingsprocessen, zoals die in auto-uitlaten, crotonaldehyde als een component van het uitlaatgas.
4. Toepassingen van crotonaldehyde
Crotonaldehyde wordt gebruikt als een precursor in de synthese van verschillende industriële producten.
Grote hoeveelheden crotonaldehyde worden gebruikt in de productie van sorbinezuur, een veelgebruikt conserveermiddel voor levensmiddelen. De synthese omvat condensatie van crotonaldehyde met keteen in aanwezigheid van organische zinkzouten, gevolgd door depolymerisatie van de resulterende polyester, hetzij thermisch of met behulp van een mineraalzuur.
α-Tocopherol, een van de acht natuurlijk voorkomende componenten met vitamine E-activiteit, wordt industrieel gesynthetiseerd via de condensatie van fytol met 2,3,6-trimethylhydrochinon dat wordt gevormd uit crotonaldehyde en di-ethylketon via een proces in vier stappen.
3-Methoxybutanol wordt geproduceerd door de toevoeging van methanol aan crotonaldehyde gevolgd door hydrogenering. Dit product en zijn acetaatester worden gebruikt als speciale oplosmiddelen, met name gewaardeerd om hun vermogen om viscositeit, drooggedrag en glans in lakken en vernissen te regelen.
Crotonaldehyde is een voorloper voor een breed scala aan chemische tussenproducten. Een primair voorbeeld is crotonzuur, verkregen door oxidatie van crotonaldehyde. Deze van crotonaldehyde afgeleide tussenproducten worden in verschillende sectoren gebruikt, waaronder:
- Farmaceutica en biocompatibele/medische producten
- Agrochemicaliën
- Harsen, polymere verdikkers
- Verven en coatings
- Kleurstoffen
- Rubbers en rubberantioxidanten
- Gelatineverharding
- Kleefstoffen
- Looien en lijmen van leer (leer en papier)
- Metaalverhelderingsmiddelen
- Smeermiddelen
- Corrosie-inhibitoren
5. Toxicologie van crotonaldehyde
Crotonaldehyde vormt een aanzienlijk gezondheidsrisico vanwege de sterke irriterende eigenschappen. Hier is een overzicht van de effecten:
Gevolgen voor de menselijke gezondheid
- Crotonaldehyde irriteert de ogen, huid en luchtwegen. Studies suggereren verschillende drempelwaarden voor irritatie, variërend van 0,035 ppm tot 0,56 ppm voor geurdetectie en irritatie, respectievelijk.
- Inademing kan brandende sensaties in de neus en luchtwegen, tranen, hoesten, bronchoconstrictie en mogelijk longoedeem of diepe longschade veroorzaken.
- Crotonaldehyde is aanwezig in tabaksrook, uitlaatgassen van motoren en houtverbranding. Het komt ook van nature voor in sommige voedingsmiddelen.
Beroepsmatige blootstellingslimieten
Bij gebrek aan specifieke beroepsmatige blootstellingsniveaus kunnen richtlijnen zoals AEGL’s (acute exposure guideline levels) en ERPG’s (emergency response planning guidelines) worden gebruikt voor risicobeoordeling tijdens ongelukken of noodsituaties.
Toxicologische gegevens
- Acute toxiciteit:
- Orale LD50 (rat): 174 mg/kg
- Inhalatie LC50 (rat, man, 4u): 336 mg/m³
- Dermale LD50 (cavia): 26 mg/kg
- Genotoxiciteit: Hoewel crotonaldehyde in vitro (in een laboratoriumomgeving) adducten vormt, is het bewijs voor in vivo mutageniteit minder duidelijk.
- Crotonaldehyde is geclassificeerd als mutageen volgens CLP-verordening (EG) nr. 1272/2008.
Effecten op dieren en micro-organismen
- Dieren:
- Vissen zijn de meest gevoelige soort voor crotonaldehyde, met een 96-uurs LC50 (dodelijke concentratie voor 50% van de populatie) van 0,65 mg/L voor regenboogforel.
- Crotonaldehyde irriteert de luchtwegen bij verschillende dieren, waarbij ratten het meest gevoelig zijn (4-uurs inhalatie LC50 van 120 ppm).
- Micro-organismen zijn minder gevoelig dan dieren, waarbij Pseudomonas putida een 18-uurs EC10 (effectconcentratie voor 10% van de populatie) van 10,4 mg/L vertoont.
Crotonaldehyde wordt geclassificeerd als een mariene verontreinigende stof ondanks zijn hoge biologische afbreekbaarheid (> 83%).
Referenties
- Crotonaldehyde and Crotonic Acid; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a08_083.pub2
- CROTONALDEHYDE; IARC MONOGRAPHS VOLUME 63. – https://publications.iarc.fr/81
